解题方法
1 . 已知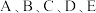 是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
(1)A的最高价氧化物是___________ 分子。(填“极性”或“非极性”)
(2)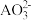 的空间结构为
的空间结构为___________ ,其中心原子的杂化方式为___________ 杂化。
(3)C的气态氢化物沸点是同族元素氢化物沸点中最高的,其原因是___________ 。
(4) 属于
属于___________ 区的元素,其基态原子的价层电子轨道表示式为___________ 。
(5) 的基态原子的电子排布式为
的基态原子的电子排布式为___________ ,在周期表中位置___________ 。
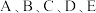 是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
是原子序数依次增大的前四周期元素,其元素性质或原子结构如表: | 原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
 | 原子最高能级的不同轨道都有电子,且自旋方向相同 |
 | 在周期表所有元素中电负性最大 |
 | 位于周期表中第4纵列 |
 | 基态原子 层全充满, 层全充满, 层只有一个电子 层只有一个电子 |
(2)
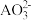 的空间结构为
的空间结构为(3)C的气态氢化物沸点是同族元素氢化物沸点中最高的,其原因是
(4)
 属于
属于(5)
 的基态原子的电子排布式为
的基态原子的电子排布式为
您最近一年使用:0次
解题方法
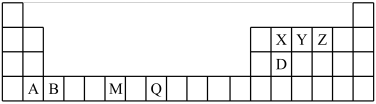
2 . 下表为元素周期表的一部分,请参照7种元素在表中的位置,回答下列问题: 的基态原子的核外电子排布图为
的基态原子的核外电子排布图为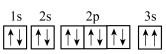 ,该电子排布图违背了
,该电子排布图违背了___________ 。
(2)在 的氢化物
的氢化物 分子的电子式
分子的电子式___________ , 原子轨道的杂化类型是
原子轨道的杂化类型是___________ 。
(3)单质 有两种同素异形体,其中
有两种同素异形体,其中___________ (填分子式)在水中的溶解度较大,原因是___________ 。
(4)基态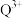 与
与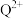 的未成对电子数之比为
的未成对电子数之比为___________ ;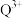 与
与 络合得到多种配合物,其中配位数为5的配离子为
络合得到多种配合物,其中配位数为5的配离子为___________ (填化学式)。
 的基态原子的核外电子排布图为
的基态原子的核外电子排布图为 ,该电子排布图违背了
,该电子排布图违背了(2)在
 的氢化物
的氢化物 分子的电子式
分子的电子式 原子轨道的杂化类型是
原子轨道的杂化类型是(3)单质
 有两种同素异形体,其中
有两种同素异形体,其中(4)基态
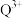 与
与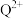 的未成对电子数之比为
的未成对电子数之比为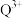 与
与 络合得到多种配合物,其中配位数为5的配离子为
络合得到多种配合物,其中配位数为5的配离子为
您最近一年使用:0次
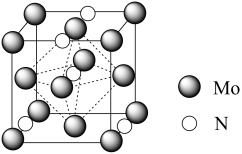
3 . 氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示,其中氮化钼晶胞参数为 。
。___________ 。
(2)晶体的密度为___________ g∙cm-3。
(3)每个钼原子周围与其距离最近的钼原子有___________ 个。
 。
。
(2)晶体的密度为
(3)每个钼原子周围与其距离最近的钼原子有
您最近一年使用:0次
4 . 下列说法错误的是
| A.水很稳定是因为水中含有大量氢键 |
| B.在同一能级上运动的电子,其运动状态不可能相同 |
| C.碘易溶于四氯化碳、甲烷难溶于水,二者都可用相似相溶原理解释 |
| D.M能层最多含3个能级 |
您最近一年使用:0次
解题方法
5 . 工业上常用反应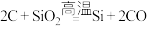 制备粗硅,若碳过量还会生成SiC,下列说法不正确的是
制备粗硅,若碳过量还会生成SiC,下列说法不正确的是
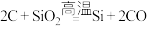 制备粗硅,若碳过量还会生成SiC,下列说法不正确的是
制备粗硅,若碳过量还会生成SiC,下列说法不正确的是| A.相对分子质量:C60>SiO2>SiC,因此熔沸点:C60>SiO2>SiC |
B. 中 中 的化合价为 的化合价为 价, 价, 中C的化合价为 中C的化合价为 价,因此 价,因此 还原性强于 还原性强于 |
C.Si原子间难形成双键而C原子间可以,是因为 的原子半径大于C,难形成 的原子半径大于C,难形成 键 键 |
| D.键能:Si-H<C-H,Si-Si<C-C,因此硅烷的种类和数量远不如烷烃的多 |
您最近一年使用:0次
解题方法
6 . 下列分子或离子的VSFPR模型与其空间结构不一致的是
A. | B. | C. | D. |
您最近一年使用:0次
7 . 以下说法中错误的是
| A.在①N、P、As和②Na、P、Cl中,元素的电负性随原子序数增大而递增的是② |
| B.同一原子中,2p、3p、4p能级的轨道依次增多 |
C.某元素原子的部分逐级电离能 分别为738、1451、7733、10540、13630,该元素可能在第三周期第ⅡA族 分别为738、1451、7733、10540、13630,该元素可能在第三周期第ⅡA族 |
| D.在共价键F-I、F-Cl和C-C,极性最强的是F-I |
您最近一年使用:0次
8 . 已知反应3A(g)+2B(g)≒C(g)+4D(g) ΔH<0。如图:a、b表示在一定条件下,D的体积分数D%随时间t的变化情况。若使曲线b变为曲线a ,可采取的措施是
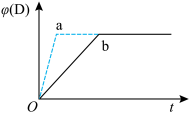
| A.只有⑤ | B.①③ | C.③⑤ | D.②③⑤ |
您最近一年使用:0次
9 . 一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g) CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。___________ (放热或吸热)。
(2)300℃时,将容器的容积压缩到原来的 ,在其他条件不变的情况下,对平衡体系产生的影响是
,在其他条件不变的情况下,对平衡体系产生的影响是___________ (填字母)。
a.c(H2)减少
b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加
d.重新平衡时c(H2)/c(CH3OH)减小
 CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。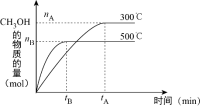
(2)300℃时,将容器的容积压缩到原来的
 ,在其他条件不变的情况下,对平衡体系产生的影响是
,在其他条件不变的情况下,对平衡体系产生的影响是a.c(H2)减少
b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加
d.重新平衡时c(H2)/c(CH3OH)减小
您最近一年使用:0次
10 . 回答下列问题。
(1)已知在K2Cr2O7的溶液中存在如下平衡:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,
(黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,___________ 色加深,在此基础上再滴加3~10滴浓H2SO4溶液,___________ 色加深。
(2)草酸与高猛酸钾在酸性条件下能够发生如下反应:2MnO +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
①如果研究催化剂对化学反应速率的影响,使用实验___________ 和___________ (用 ~
~ 表示,下同);如果研究温度对化学反应速率的影响,使用实验
表示,下同);如果研究温度对化学反应速率的影响,使用实验___________ 和___________ 。
②对比实验 和
和 ,可以研究
,可以研究___________ 对化学反应速率的影响。
(1)已知在K2Cr2O7的溶液中存在如下平衡:Cr2O
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,
(黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,(2)草酸与高猛酸钾在酸性条件下能够发生如下反应:2MnO
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
 | 2mL | 20 | |
 | 2mL | 20 | 少量MnSO4粉末 |
 | 2mL | 30 | |
 | 1mL | 20 | 1mL蒸馏水 |
 ~
~ 表示,下同);如果研究温度对化学反应速率的影响,使用实验
表示,下同);如果研究温度对化学反应速率的影响,使用实验②对比实验
 和
和 ,可以研究
,可以研究
您最近一年使用:0次



