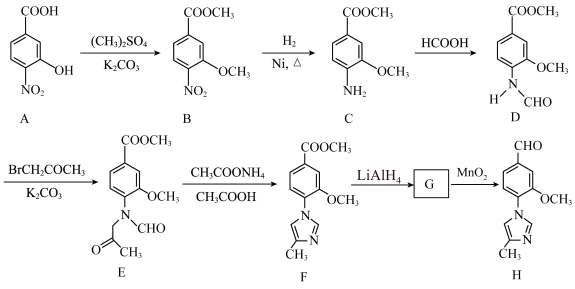
1 . 化合物H是一种合成药物的中间体,其合成路线流程图如图: 的名称为
的名称为___________ ;A中除羧基外还含有的官能团的名称为___________ 。
(2)B→C的反应类型为___________ 。
(3)写出D→E反应的化学方程式:___________ 。
(4)满足下列条件的C的同分异构体有___________ 种(不考虑立体异构)。
①苯环上有三个取代基,氨基与苯环直接相连;②含酯基且能发生银镜反应;③与氯化铁溶液能发生显色反应。
(5)G的分子式为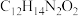 ,经氧化得到H,写出G的结构简式:
,经氧化得到H,写出G的结构简式:___________ 。
(6)已知: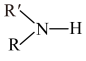
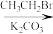
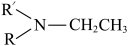 (R代表烃基,R′代表烃基或H)。请写出以
(R代表烃基,R′代表烃基或H)。请写出以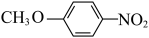 和
和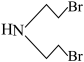 为原料制备的
为原料制备的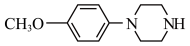 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)________ 。
 的名称为
的名称为(2)B→C的反应类型为
(3)写出D→E反应的化学方程式:
(4)满足下列条件的C的同分异构体有
①苯环上有三个取代基,氨基与苯环直接相连;②含酯基且能发生银镜反应;③与氯化铁溶液能发生显色反应。
(5)G的分子式为
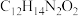 ,经氧化得到H,写出G的结构简式:
,经氧化得到H,写出G的结构简式:(6)已知:

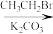
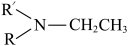 (R代表烃基,R′代表烃基或H)。请写出以
(R代表烃基,R′代表烃基或H)。请写出以 和
和 为原料制备的
为原料制备的 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
您最近一年使用:0次
解题方法
2 . 随着工业的发展,钴一钼系催化剂的用量越来越大,从废催化剂中回收贵金属不但能合理利用资源,而且可减少废弃物对环境的污染。对某品牌的废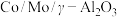 催化剂(含有石墨、S、Fe等杂质)的再回收处理工艺如图。
催化剂(含有石墨、S、Fe等杂质)的再回收处理工艺如图。 在常压下893K开始挥发,可溶于碱溶液,而Co的氧化物难溶于碱溶液。
在常压下893K开始挥发,可溶于碱溶液,而Co的氧化物难溶于碱溶液。
回答下列问题:
(1)为提高“焙烧”效率,可对废催化剂进行的操作为___________ 。
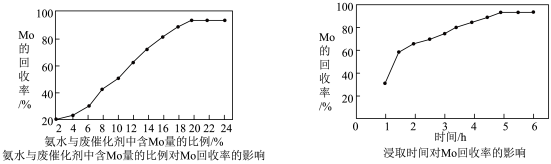
(2)用氨水进行“氨溶1”时,氨水与废催化剂中含Mo量的比例、浸取时间对Mo回收率的影响如图,选择氨水与废催化剂中含Mo量的比例为___________ ,浸取时间应控制在约___________ 小时。 开始与酸反应较慢,稀释后迅速反应,稀释后发生反应的离子方程式为
开始与酸反应较慢,稀释后迅速反应,稀释后发生反应的离子方程式为___________ 。
(4)“中和”时在不断搅拌下调pH为6.0~6.5的目的是___________ 。
(5)“中和”时加入过量氨水直至生成红色的钴氨配合物。
①Co、Mo离子能形成配合物的原因在于___________ 。
②钴氨配离子 中存在的化学键有
中存在的化学键有___________ (填标号)。
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
 催化剂(含有石墨、S、Fe等杂质)的再回收处理工艺如图。
催化剂(含有石墨、S、Fe等杂质)的再回收处理工艺如图。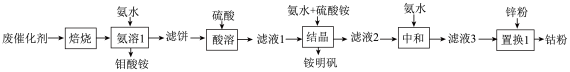
 在常压下893K开始挥发,可溶于碱溶液,而Co的氧化物难溶于碱溶液。
在常压下893K开始挥发,可溶于碱溶液,而Co的氧化物难溶于碱溶液。回答下列问题:
(1)为提高“焙烧”效率,可对废催化剂进行的操作为
(2)用氨水进行“氨溶1”时,氨水与废催化剂中含Mo量的比例、浸取时间对Mo回收率的影响如图,选择氨水与废催化剂中含Mo量的比例为
 开始与酸反应较慢,稀释后迅速反应,稀释后发生反应的离子方程式为
开始与酸反应较慢,稀释后迅速反应,稀释后发生反应的离子方程式为(4)“中和”时在不断搅拌下调pH为6.0~6.5的目的是
(5)“中和”时加入过量氨水直至生成红色的钴氨配合物。
①Co、Mo离子能形成配合物的原因在于
②钴氨配离子
 中存在的化学键有
中存在的化学键有A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
您最近一年使用:0次
解题方法
3 . 已知: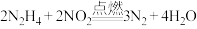 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
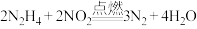 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.25℃、101 kPa下,11.2 L氮气中含有的π键数为NA |
| B.16 g N2H4中含有的质子数为9NA |
| C.0.1 mol H2O中含有的离子总数为0.2NA |
D.标准状况下,0.1 mol  溶于水得到的溶液中含有 溶于水得到的溶液中含有 的个数为0.1NA 的个数为0.1NA |
您最近一年使用:0次
4 . 不同催化剂作用下 催化转化为CO的过程中的能量变化如图(“
催化转化为CO的过程中的能量变化如图(“ ”表示组分X吸附在催化剂表面)。下列说法错误的是
”表示组分X吸附在催化剂表面)。下列说法错误的是
 催化转化为CO的过程中的能量变化如图(“
催化转化为CO的过程中的能量变化如图(“ ”表示组分X吸附在催化剂表面)。下列说法错误的是
”表示组分X吸附在催化剂表面)。下列说法错误的是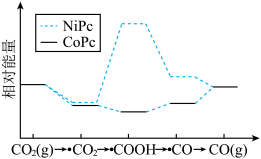
| A.在两种催化剂的作用下,上述过程总反应的能量变化相同 |
| B.反应过程中,没有极性共价键的断裂和形成 |
C.反应过程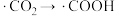 中, 中,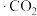 发生还原反应 发生还原反应 |
D. 在两种催化剂表面吸附均需放热 在两种催化剂表面吸附均需放热 |
您最近一年使用:0次
5 . 生产、生活中蕴含了丰富的化学知识,下列有关说法正确的是
| 选项 | 生产活动 | 化学原理 |
| A | 蒸馒头前,在和面过程中加入少量发酵粉 | 发酵粉的主要成分是 |
| B | 葡萄酒中添加 | 适量 可以起到防腐、抗氧化的作用 可以起到防腐、抗氧化的作用 |
| C | 用蘸有浓盐酸的玻璃棒检测氨气管道 | 氨气液化吸热 |
| D | 船员常在出海的轮船底部镶嵌锌块 | 利用了外加电流法减轻船体腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 已知反应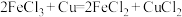 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
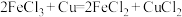 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.氯原子的结构示意图: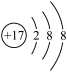 |
B.基态Fe²⁺的价层电子轨道表示式: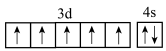 |
C.基态铜原子的电子排布式: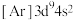 |
D.反应中每生成1 mol  ,转移的电子数为 ,转移的电子数为 |
您最近一年使用:0次
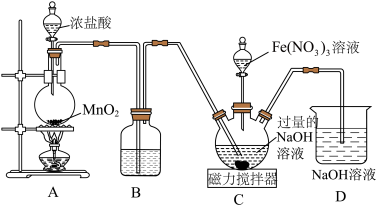
7 . 铁酸钾(K2FeO4)为暗紫色固体,是一种高效多功能的新型非氯绿色消毒剂,易溶于水,在KOH浓溶液中溶解度较低,在酸性或中性溶液中不稳定,在碱性溶液中较稳定且碱性越强越稳定。某实验小组设计如图装置制备Na2FeO4,再经过后续操作将Na2FeO4转化为K2FeO4.根据所学知识回答下列问题:_______ 。
(2)装置A中盛装浓盐酸的仪器名称为_______ ,装置B中盛装的液体为_______ 。
(3)向装置C中通入的Cl2不能过量,原因是_______ 。
(4)装置D中发生反应的化学方程式为_______ 。
(5)高铁酸钾(K2FeO4)是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成Fe(OH)3胶体,高铁酸钾用作水处理剂的理由是_______ 。
(6)二氧化氯是一种高效消毒剂。工业制备ClO2的反应为:2NaClO3+4HCl=ClO2↑+Cl2↑+2H2O+2NaCl
①用单线桥表示电子转移的方向和数目_______ 。
②常温常压下,若ClO2和Cl2在消毒时自身均被还原为Cl-,ClO2的消毒能力是等质量Cl2的_______ 倍(保留1位小数)。
(2)装置A中盛装浓盐酸的仪器名称为
(3)向装置C中通入的Cl2不能过量,原因是
(4)装置D中发生反应的化学方程式为
(5)高铁酸钾(K2FeO4)是水处理过程中的一种新型综合型的水处理剂。高铁酸钾具有强氧化性,在净水过程中可生成Fe(OH)3胶体,高铁酸钾用作水处理剂的理由是
(6)二氧化氯是一种高效消毒剂。工业制备ClO2的反应为:2NaClO3+4HCl=ClO2↑+Cl2↑+2H2O+2NaCl
①用单线桥表示电子转移的方向和数目
②常温常压下,若ClO2和Cl2在消毒时自身均被还原为Cl-,ClO2的消毒能力是等质量Cl2的
您最近一年使用:0次
8 . 下列实验操作和装置能达到相应实验目的的是
|
|
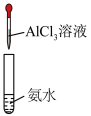
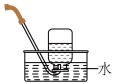
| A.制备Al(OH)3 | B.收集氯气 |
|
|
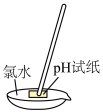
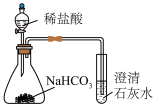
| C.准确测量氯水的pH | D.比较C和Cl的非金属性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . C、Si、Ge、Sn是同族元素,该族元素的单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)C、Si、Ge、Sn的第一电离能从大到小的顺序是______ (用元素符号表示);在基态Ge原子中,电子占据的最高能层的符号为______ ,该能层中有______ 种不同运动状态的电子。
(2) 有晶体和非晶体两种,可通过
有晶体和非晶体两种,可通过______ 方法鉴别二者。
(3)C、Si、Ge、Sn均能与卤素化合,已知 常温下为无色液体,遇水有白雾出现,发烟,则
常温下为无色液体,遇水有白雾出现,发烟,则 属于
属于______ (填“共价”“分子”或“离子”)晶体;遇水有白雾出现的化学方程式为____________ 。
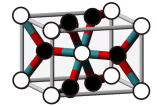
(4) 是一种优秀的透明导电材料,其晶胞结构如图所示。晶胞参数分别为a pm、a pm、c pm,晶胞中立方体的边长为a pm,阿伏加德罗常数的值为
是一种优秀的透明导电材料,其晶胞结构如图所示。晶胞参数分别为a pm、a pm、c pm,晶胞中立方体的边长为a pm,阿伏加德罗常数的值为 。
。______ (填元素符号)。
② 晶体的密度为
晶体的密度为______ g⋅cm 。
。
(1)C、Si、Ge、Sn的第一电离能从大到小的顺序是
(2)
 有晶体和非晶体两种,可通过
有晶体和非晶体两种,可通过(3)C、Si、Ge、Sn均能与卤素化合,已知
 常温下为无色液体,遇水有白雾出现,发烟,则
常温下为无色液体,遇水有白雾出现,发烟,则 属于
属于(4)
 是一种优秀的透明导电材料,其晶胞结构如图所示。晶胞参数分别为a pm、a pm、c pm,晶胞中立方体的边长为a pm,阿伏加德罗常数的值为
是一种优秀的透明导电材料,其晶胞结构如图所示。晶胞参数分别为a pm、a pm、c pm,晶胞中立方体的边长为a pm,阿伏加德罗常数的值为 。
。
②
 晶体的密度为
晶体的密度为 。
。
您最近一年使用:0次
10 . 硫酸锌是制造锌钡白和锌盐的主要原料,口服硫酸锌可纠正锌缺乏,恢复酶系统的功能。用锌白矿(主要成分为ZnO,还含有 、
、 、
、 等杂质)制备
等杂质)制备 的流程如图:
的流程如图: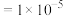 mol⋅L
mol⋅L 时视为沉淀完全):
时视为沉淀完全):
(1)基态锌离子的价层电子轨道表示式为______ 。
(2)“酸浸”前通常需要将锌白矿粉碎,其目的是______ 。
(3)滤渣1的主要成分为______ (填化学式)。
(4)加入 “氧化”时发生反应的离子方程式为
“氧化”时发生反应的离子方程式为____________ 。
(5)加入试剂X调节溶液的pH在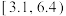 ,使铁元素转化为沉淀而除去,试剂X可以选用下列中的
,使铁元素转化为沉淀而除去,试剂X可以选用下列中的______ (填标号)。
A.ZnO B. C.
C.
根据题中数据计算常温下 的溶度积
的溶度积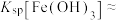
______ 。
(6)pH过大时,锌元素会以 形式存在,则
形式存在,则 中存在的作用力为______(填标号)。
中存在的作用力为______(填标号)。
 、
、 、
、 等杂质)制备
等杂质)制备 的流程如图:
的流程如图: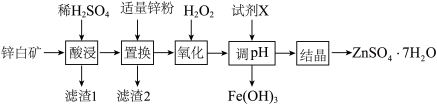
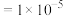 mol⋅L
mol⋅L 时视为沉淀完全):
时视为沉淀完全):| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
 | 1.1 | 3.1 |
 | 7.6 | 9.6 |
 | 6.4 | 8.0 |
(1)基态锌离子的价层电子轨道表示式为
(2)“酸浸”前通常需要将锌白矿粉碎,其目的是
(3)滤渣1的主要成分为
(4)加入
 “氧化”时发生反应的离子方程式为
“氧化”时发生反应的离子方程式为(5)加入试剂X调节溶液的pH在
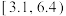 ,使铁元素转化为沉淀而除去,试剂X可以选用下列中的
,使铁元素转化为沉淀而除去,试剂X可以选用下列中的A.ZnO B.
 C.
C.
根据题中数据计算常温下
 的溶度积
的溶度积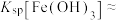
(6)pH过大时,锌元素会以
 形式存在,则
形式存在,则 中存在的作用力为______(填标号)。
中存在的作用力为______(填标号)。| A.离子键 | B.共价键 | C.σ键 | D.π键 |
您最近一年使用:0次