1 . 化学与生活紧密相关,下列有关说法不正确的是
| A.氧化铝可用于制造耐高温的容器 |
| B.FeSO4作补血剂时可与维生素C同时服用 |
| C.生铁的含碳量比钢的含碳量高,合金的熔点一般比其成分金属的熔点高 |
| D.漂白粉可用于漂白棉、麻、纸张等,其长期露置在空气中会失效 |
您最近一年使用:0次
解题方法
2 . 甲、乙两烧杯中分别盛有200mL浓度均为2mol/L的盐酸与NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得同温同压下生成气体的体积之比为2:5
| A.2.7g | B.3.6g | C.5.4g | D.9.0g |
您最近一年使用:0次
解题方法
3 . 将某质量的镁铝合金溶解在500 mL盐酸中,向反应后的溶液中逐滴加入2 mol/L NaOH溶液,产生沉淀质量与碱溶液体积的关系如图所示。请填写下列空白:
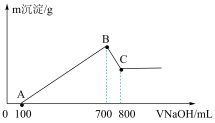
(1)写出BC段发生反应的化学方程式:_______ 。
(2)合金中铝的质量为_______ 。
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是_______ 。

(1)写出BC段发生反应的化学方程式:
(2)合金中铝的质量为
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是
您最近一年使用:0次
4 . 实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为_______ 。
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为_______ 克。
(3)此时,被氧化HCl的物质的量为_______ 。
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为
(3)此时,被氧化HCl的物质的量为
您最近一年使用:0次
5 . 已知常温下B、D、E、L为密度比空气大的气体,D、E为单质,其他为化合物。A是一种淡黄色固体,F、G均能与L的水溶液反应放出B.据如图反应框图填空。

(1)F的俗名是_______ ,B分子式为 _______ ,工业上利用反应③生产 _______ 。(填名称)
(2)反应④的离子方程式为_______ 。
(3)有一种单质能与H反应生成E,该反应的化学方程式为_______ 。
(4)某酸性氧化物气体M溶于水具有漂白作用,既有氧化性,又有还原性,与D在溶液中反应的离子方程式为_______ 。

(1)F的俗名是
(2)反应④的离子方程式为
(3)有一种单质能与H反应生成E,该反应的化学方程式为
(4)某酸性氧化物气体M溶于水具有漂白作用,既有氧化性,又有还原性,与D在溶液中反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 亚硝酸钠(NaNO2)有毒、有咸味,外形与食盐相似,人若误食会引起中毒。某兴趣小组欲研究亚硝酸钠,查阅资料得到如表信息。试根据信息回答下列问题:
(1)已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,则该反应中氧化剂是 _______ ;若有0.75mol电子发生转移,则被氧化的还原剂的粒子数为 _______ (用NA表示阿伏加德罗常数的值)。
(2)人若误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列说法错误的是 _______(填序号)。
(3)下列方法中,可用来区分NaNO2和NaCl的是 _______ (填序号)。
A.焰色反应
B.滴加酸化的FeSO4溶液和KSCN溶液
C.在酸性条件下加入淀粉KI溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式_______ 。
| 药品 | NaNO2(亚硝酸钠) |
| 性质 | 在酸性溶液中有较强氧化性,能将Fe2+氧化成Fe3+。 |
(2)人若误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列说法错误的是 _______(填序号)。
| A.NaNO2被还原 |
| B.维生素C具有还原性 |
| C.还原性:维生素C>Fe2+ |
| D.NaNO2是还原剂 |
A.焰色反应
B.滴加酸化的FeSO4溶液和KSCN溶液
C.在酸性条件下加入淀粉KI溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式
您最近一年使用:0次
7 . 喷泉实验装置如图所示。应用下列各组气体与溶液,能出现喷泉现象的是
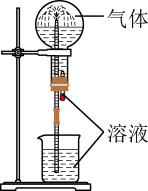

| 气体 | 溶液 | |
| A | CO | 稀盐酸 |
| B | HCl | 稀氨水 |
| C | NO | 水 |
| D | CO2 | 饱和NaI溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 将SO2分别通入下列四种溶液,根据实验现象所得结论正确的是
| 选项 | 溶液 | 现象 | 结论 |
| A | 溴水溶液 | 溴水褪色 | SO2具有漂白性 |
| B | H2S溶液 | 出现淡黄色浑浊 | SO2具有氧化性 |
| C | BaCl2溶液 | 无明显变化 | BaSO4能溶于水 |
| D | H2O2溶液 | 无明显变化 | SO2和H2O2溶液不反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 下列说法不正确的是
| A.玻璃、水泥、陶瓷是三大传统的无机非金属材料 |
B.工业上用焦炭还原石英砂制取粗硅原理:SiO2+2C Si+2CO↑ Si+2CO↑ |
| C.海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等 |
| D.绿色化学的核心思想就是先污染后用化学方法治理 |
您最近一年使用:0次
10 . 某化学教师为“氯气与金属钠反应”设计了如图装置的实验(夹持、加热装置已略),实验操作:先给钠预热,等钠熔融成圆球时,通入氯气,即可见钠着火燃烧
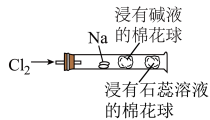

| A.反应生成大量白烟是因为生成氯化钠 |
| B.塞一团浸有碱液的棉球是用于吸收过量的氯气,以免其污染空气 |
| C.钠熔点高,所以先预热再反应 |
| D.可据浸有石蕊溶液的棉花球的颜色变化判断氯气是否被碱液完全吸收 |
您最近一年使用:0次



