解题方法
1 . 已知反应 ,若该反应的反应速率分别用
,若该反应的反应速率分别用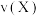 、
、 、
、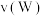 、
、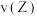 表示,则下列关系式正确的是
表示,则下列关系式正确的是
 ,若该反应的反应速率分别用
,若该反应的反应速率分别用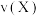 、
、 、
、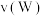 、
、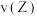 表示,则下列关系式正确的是
表示,则下列关系式正确的是A.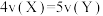 | B. | C. | D.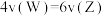 |
您最近一年使用:0次
解题方法
2 . 在生物实验室里,常用甲醛溶液保存动物标本,下列说法错误的是
A.甲醛的分子式: |
| B.甲醛与乙醛互为同系物 |
| C.甲醛溶液俗称福尔马林 |
D. 甲醛在纯氧中完全燃烧时,最多可消耗 甲醛在纯氧中完全燃烧时,最多可消耗 |
您最近一年使用:0次
名校
解题方法
3 . 完成下列问题。
(1)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
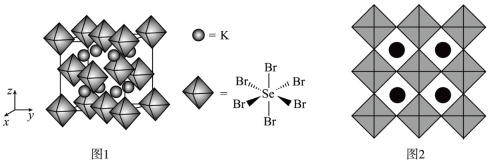
①X的化学式为___________ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为___________  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(2)由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
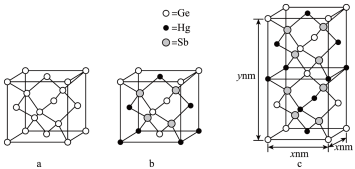
①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是___________ 。
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为___________ ;
③设X的最简式的式量为Mr,则X晶体的密度为___________ g/cm3(列出算式)。
(3)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe—F键长为r pm,则B点原子的分数坐标为
)。已知Xe—F键长为r pm,则B点原子的分数坐标为_______ ;晶胞中A、B间距离d=________ pm。

(1)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(2)由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。

①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为
③设X的最简式的式量为Mr,则X晶体的密度为
(3)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为(
 ,
, ,
, )。已知Xe—F键长为r pm,则B点原子的分数坐标为
)。已知Xe—F键长为r pm,则B点原子的分数坐标为
您最近一年使用:0次
名校
4 . 完成下列问题。
(1)硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所示,简要分析和解释下列有关事实:
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是___________ 。SiH4的稳定性小于CH4,更易生成氧化物,原因是___________ 。
(2)比较NH3和[Cu(NH3)4]2+中H−N−H键角的大小:NH3___________ [Cu(NH3)4]2+(填“>”或“<”),并说明理由:___________
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d
(4)苯胺( )与甲苯(
)与甲苯(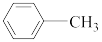 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
(5)硒的两种含氧酸的酸分别为 、
、 ,试比较其酸性强弱并说明原因:
,试比较其酸性强弱并说明原因:___________ 。
(6)在水中的溶解度,吡啶(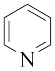 )远大于苯,主要原因是①
)远大于苯,主要原因是①_______ ,②_______ 。
(1)硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所示,简要分析和解释下列有关事实:
| 化学键 | C−C | C−H | C−O | Si−Si | Si−H | Si−O |
| 键能/ (kJ·mol-1) | 365 | 413 | 336 | 226 | 318 | 452 |
(2)比较NH3和[Cu(NH3)4]2+中H−N−H键角的大小:NH3
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
(4)苯胺(
 )与甲苯(
)与甲苯(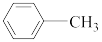 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(5)硒的两种含氧酸的酸分别为
 、
、 ,试比较其酸性强弱并说明原因:
,试比较其酸性强弱并说明原因:(6)在水中的溶解度,吡啶(
 )远大于苯,主要原因是①
)远大于苯,主要原因是①
您最近一年使用:0次
名校
5 . 有X、Y、Z、Q、E、M、G原子序数依次递增的七种元素,除G元素外其余均为短周期主族元素。X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素原子的外围电子层排布式为nsnnpn+1,Q的基态原子核外成对电子数是成单电子数的3倍,E与Q同周期,M元素的第一电离能在同周期主族元素中从大到小排第三位,G原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第ⅠA族元素。回答下列问题:
(1)写出第三周期基态原子未成对电子数与G相同且电负性最大的元素是___________ (填元素名称)。GQ受热分解生成G2Q和Q2,请从G的原子结构来说明GQ受热易分解的原因:_______ 。
(2)M元素的第一电离能在同周期主族元素中从大到小排第三位的原因是_____________ 。
(3)X与Q形成的化合物中沸点较高的物质的化学式为___________ 。
(4)Z、M、E所形成的简单离子的半径由大到小顺序为___________ (用离子符号表示)。
(5)X、Y、Z、Q的电负性由大到小的顺序为___________ (用元素符号表示)。
(1)写出第三周期基态原子未成对电子数与G相同且电负性最大的元素是
(2)M元素的第一电离能在同周期主族元素中从大到小排第三位的原因是
(3)X与Q形成的化合物中沸点较高的物质的化学式为
(4)Z、M、E所形成的简单离子的半径由大到小顺序为
(5)X、Y、Z、Q的电负性由大到小的顺序为
您最近一年使用:0次
名校
解题方法
6 . 完成下列问题。
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为___________ ,基态磷原子中,电子占据的最高能层符号为______ ;该能层能量最高的电子云在空间有_______ 个伸展方向,原子轨道呈___________ 形。
(2)锰的价层电子排布图为_________ 。在锰原子的核外电子中,有___________ 种运动状态不同的电子,有_________ 种空间运动状态的电子,锰元素位于元素周期表中________ 区。
(3)某同学推断Mg的基态原子的轨道表示式为 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为
(2)锰的价层电子排布图为
(3)某同学推断Mg的基态原子的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了
您最近一年使用:0次
名校
解题方法
7 . 按照要求写出下列离子方程式:
(1)用饱和FeCl3溶液制备Fe(OH)3胶体:___________ ;
(2)向氯化银悬浊液中加入过量氨水后溶液变澄清:___________ ;
(3)向Ce2(SO4)3溶液中加入NH4HCO3溶液生成Ce2(CO3)3·nH2O的离子方程式为________ ;
(4)向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液,两者物质的量之比为 n[NH4Al(SO4)2]∶n[Ba(OH)2]=2∶5___________ ;
(5)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2.上述制备I2的总反应的离子方程式为___________ 。
(1)用饱和FeCl3溶液制备Fe(OH)3胶体:
(2)向氯化银悬浊液中加入过量氨水后溶液变澄清:
(3)向Ce2(SO4)3溶液中加入NH4HCO3溶液生成Ce2(CO3)3·nH2O的离子方程式为
(4)向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液,两者物质的量之比为 n[NH4Al(SO4)2]∶n[Ba(OH)2]=2∶5
(5)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2.上述制备I2的总反应的离子方程式为
您最近一年使用:0次
名校
解题方法
8 . 对下列粒子组在指定溶液中能否大量共存的判断和分析均正确的是
| 选项 | 溶液与粒子组 | 判断和分析 |
| A | 使甲基橙变黄色的溶液:Na+、K+、 、 、 | 能大量共存,因为使甲基橙变黄色的溶液呈碱性,粒子与OH-不发生反应 |
| B | Na+、Al3+、Cl-、NH3·H2O | 不能大量共存,发生反应:Al3++4NH3·H2O= +4 +4 +2H2O +2H2O |
| C | 常温下水电离的c(H+)=1×10-12 mol·L-1的溶液:K+、 、 、 、Cl- 、Cl- | 不能大量共存,因为酸性溶液中会发生反应:2H++ =H2C2O4,碱性溶液中会发生反应: =H2C2O4,碱性溶液中会发生反应: +OH-=NH3·H2O +OH-=NH3·H2O |
| D | 透明溶液:Na+、K+、 、 、 | 不能大量共存,因为 呈紫红色 呈紫红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,pH=9的CH3COONa溶液中,水电离出的H+数为10-5 NA |
| B.常温下,1mol H2O中氢键的数目为2NA |
C.反应 + HCHO + H+ + HCHO + H+ Mn2+ + CO2 + H2O(未配平)中,氧化产物与还原产物的物质的量之比为5:4 Mn2+ + CO2 + H2O(未配平)中,氧化产物与还原产物的物质的量之比为5:4 |
| D.92 g C3H8O3分子中所含羟基数为3NA |
您最近一年使用:0次
名校
解题方法
10 . [Co(NH3)5Cl]Cl2是一种应用极其广泛的配位化合物,有关该配合物下列说法正确的是
| A.该配位化合物的配位数为5 |
| B.提供孤电子对的成键原子是N和Cl |
| C.[Co(NH3)5Cl]2+中存在配位键、共价键和离子键 |
| D.[Co(NH3)5Cl]Cl2中钴元素的化合价为+2价 |
您最近一年使用:0次



