名校
1 . 为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。
(1)已知: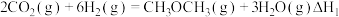


则反应 的
的 
_________ (用含 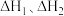 的代数式表示)
的代数式表示)
(2)化学反应的能量变化 与反应物和生成物的键能有关。键能可以简单地理解为断开(或形成)
与反应物和生成物的键能有关。键能可以简单地理解为断开(或形成) 化学键时所吸收(或放出)的能量。部分化学键的键能数据如表:
化学键时所吸收(或放出)的能量。部分化学键的键能数据如表:
反应 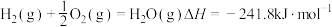 ,则
,则 
_____________ 。
(3)工业上用甲烷催化裂解可制备氢气,有关反应原理如下:
反应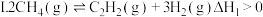 . 反应Ⅱ.
. 反应Ⅱ.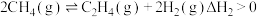 .
.
①实验测得反应Ⅰ的速率方程: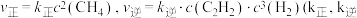 别为正、逆反应速率常数,只与温度、催化剂有关)。
别为正、逆反应速率常数,只与温度、催化剂有关)。 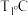 下反应达到平衡时
下反应达到平衡时 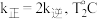 下反应达到平衡时
下反应达到平衡时 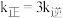 。由此推知,
。由此推知,
_________________  (填“>”、“<"或"=")。
(填“>”、“<"或"=")。
②在密闭容器中充入一定量 ,发生上述反应Ⅰ和反应Ⅱ。在不同催化剂
,发生上述反应Ⅰ和反应Ⅱ。在不同催化剂 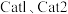 作用下,测得单位时间内
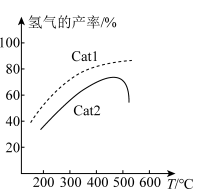
作用下,测得单位时间内  产率与温度的关系如图。其他条件相同时,催化效率较高的是
产率与温度的关系如图。其他条件相同时,催化效率较高的是_________________ (填 "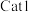 "或 "
"或 "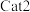 ")。在
")。在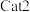 作用下,温度高于
作用下,温度高于 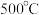 时,
时, 产率降低的可能原因是
产率降低的可能原因是_________________ 。(任写一条即可)。
(4)在一个体积为 的密闭容器中,高温下发生反应:
的密闭容器中,高温下发生反应: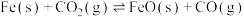 。其中
。其中 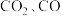 的物质的量
的物质的量 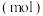 随时间
随时间 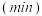 的变化关系如图所示。
的变化关系如图所示。

①反应在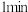 时第一次达到平衡状态,固体的质量增加了
时第一次达到平衡状态,固体的质量增加了 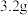 用
用  的浓度变化表示的反应速率
的浓度变化表示的反应速率 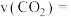
_____________________ 。
②反应进行至 时,若只改变温度,曲线发生的变化如图所示,
时,若只改变温度,曲线发生的变化如图所示, 时再次达到平衡,
时再次达到平衡,
_____________ 0(填“>”、“<"或"=")。
③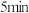 时再充入一定量的
时再充入一定量的  ,平衡发生移动。下列说法正确的是
,平衡发生移动。下列说法正确的是_____________ (填写编号)。
A. 先增大后减小 B.
先增大后减小 B. 先减小后增大
先减小后增大
C.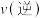 先增大后减小 D.
先增大后减小 D.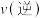 先减小后增大
先减小后增大
④表示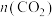 变化的曲线是
变化的曲线是_____________ (填写图中曲线的字母编号)。
(1)已知:
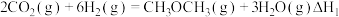


则反应
 的
的 
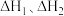 的代数式表示)
的代数式表示)(2)化学反应的能量变化
 与反应物和生成物的键能有关。键能可以简单地理解为断开(或形成)
与反应物和生成物的键能有关。键能可以简单地理解为断开(或形成) 化学键时所吸收(或放出)的能量。部分化学键的键能数据如表:
化学键时所吸收(或放出)的能量。部分化学键的键能数据如表:化学键 |
|
|
|
| 436 |
| 463 |
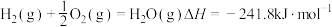 ,则
,则 
(3)工业上用甲烷催化裂解可制备氢气,有关反应原理如下:
反应
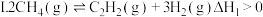 . 反应Ⅱ.
. 反应Ⅱ.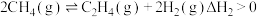 .
.①实验测得反应Ⅰ的速率方程:
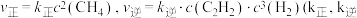 别为正、逆反应速率常数,只与温度、催化剂有关)。
别为正、逆反应速率常数,只与温度、催化剂有关)。 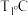 下反应达到平衡时
下反应达到平衡时 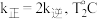 下反应达到平衡时
下反应达到平衡时 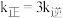 。由此推知,
。由此推知,
 (填“>”、“<"或"=")。
(填“>”、“<"或"=")。②在密闭容器中充入一定量
 ,发生上述反应Ⅰ和反应Ⅱ。在不同催化剂
,发生上述反应Ⅰ和反应Ⅱ。在不同催化剂 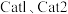 作用下,测得单位时间内
作用下,测得单位时间内  产率与温度的关系如图。其他条件相同时,催化效率较高的是
产率与温度的关系如图。其他条件相同时,催化效率较高的是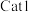 "或 "
"或 "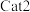 ")。在
")。在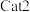 作用下,温度高于
作用下,温度高于 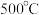 时,
时, 产率降低的可能原因是
产率降低的可能原因是
(4)在一个体积为
 的密闭容器中,高温下发生反应:
的密闭容器中,高温下发生反应: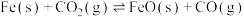 。其中
。其中 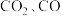 的物质的量
的物质的量 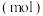 随时间
随时间 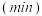 的变化关系如图所示。
的变化关系如图所示。
①反应在
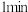 时第一次达到平衡状态,固体的质量增加了
时第一次达到平衡状态,固体的质量增加了 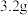 用
用  的浓度变化表示的反应速率
的浓度变化表示的反应速率 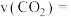
②反应进行至
 时,若只改变温度,曲线发生的变化如图所示,
时,若只改变温度,曲线发生的变化如图所示, 时再次达到平衡,
时再次达到平衡,
③
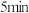 时再充入一定量的
时再充入一定量的  ,平衡发生移动。下列说法正确的是
,平衡发生移动。下列说法正确的是A.
 先增大后减小 B.
先增大后减小 B. 先减小后增大
先减小后增大C.
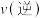 先增大后减小 D.
先增大后减小 D.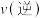 先减小后增大
先减小后增大④表示
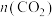 变化的曲线是
变化的曲线是
您最近一年使用:0次
名校
2 . 有四种短周期元素,它们的结构、性质等信息如下表所述:
完成下列填空:
(1)A的离子结构示意图是_____________ ,元素 D在周期表中的位置是_____________________ 。
(2)基态 A原子第一电离能_________ 基态 B原子第一电离能(填“>”、“<”或“=”),基态 C原子核外电子共有_________ 种空间运动状态。
(3)单质 C的结构式是_________ ,其化学性质稳定的原因是_____________________ 。
(4)C元素的简单气态氢化物中心原子的杂化方式为_________ ,分子构型为_________ ,与 H2S分子内共价键键角相比,较大的是_________ 。
(5)D元素的气态氢化物与 HF分子相比,沸点较大的是_________ ,请说明原因_____________________ 。
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | 与  同周期,其最高价氧化物的水化物呈两性 同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物是自来水生产过程中常用的消毒杀菌剂 |
(1)A的离子结构示意图是
(2)基态 A原子第一电离能
(3)单质 C的结构式是
(4)C元素的简单气态氢化物中心原子的杂化方式为
(5)D元素的气态氢化物与 HF分子相比,沸点较大的是
您最近一年使用:0次
3 . 已知: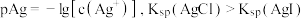 ,如图是向
,如图是向  溶液中逐渐加入
溶液中逐渐加入 的
的  溶液时,溶液的
溶液时,溶液的 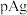 随着加入
随着加入  溶液的体积(单位:
溶液的体积(单位: )变化的图象(实线)。根据图象所得下列结论正确的是
)变化的图象(实线)。根据图象所得下列结论正确的是
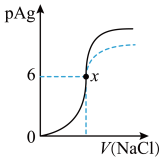
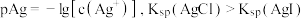 ,如图是向
,如图是向  溶液中逐渐加入
溶液中逐渐加入 的
的  溶液时,溶液的
溶液时,溶液的 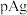 随着加入
随着加入  溶液的体积(单位:
溶液的体积(单位: )变化的图象(实线)。根据图象所得下列结论正确的是
)变化的图象(实线)。根据图象所得下列结论正确的是
A.原  溶液的物质的量浓度为 溶液的物质的量浓度为  |
B.图中  点的坐标为 点的坐标为 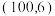 |
C.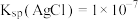 |
D.把  的 的  换成 换成  则图象在终点后变为虚线部分 则图象在终点后变为虚线部分 |
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式的书写符合要求的是
A.用惰性电极电解饱和 MgCl2溶液: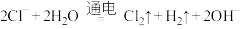 |
B.泡沫灭火器的反应原理: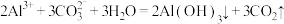 |
C.铅酸蓄电池的正极反应式: |
D.用  检验 检验 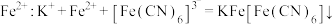 |
您最近一年使用:0次
名校
5 . 下列说法正确的是
| A.霓虹灯发光与原子核外电子跃迁有关,属于化学变化 |
| B.水垢中的硫酸钙,可先用碳酸钠溶液处理,再用醋酸除去 |
C.将  溶液和 溶液和  溶液分别加热、蒸干、灼烧,所得固体成分相同 溶液分别加热、蒸干、灼烧,所得固体成分相同 |
| D.配制FeSO4溶液时,将 FeSO4固体溶于稀盐酸中,然后稀释至所需浓度 |
您最近一年使用:0次
6 . 2-丁炔可发生如下转化,下列说法不正确 的是

| A.2-丁炔分子中最多有6个原子共面 |
| B.X与酸性KMnO4溶液反应可生成CH3COOH |
| C.Y可以发生银镜反应 |
| D.高分子Z可能存在顺式结构和反式结构 |
您最近一年使用:0次
2024-03-08更新
|
532次组卷
|
6卷引用:河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题
河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题浙江省温州市普通高中2024届高三上学期第一次适应性考试(一模)化学试题(已下线)专题02 元素化合物 有机化合物-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题06 有机化合物(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)河北省石家庄市第十七中学2023-2024学年高二下学期第一次月考化学试题浙江省部分学校2024届高三下学期模拟考试化学试卷
名校
7 . 某温度下,由H2CO3与HCl或NaOH配制一组总含碳微粒浓度为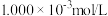 的混合溶液,混合体系中部分物种的浓度的负对数
的混合溶液,混合体系中部分物种的浓度的负对数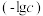 与pH关系如图所示。下列说法错误的是
与pH关系如图所示。下列说法错误的是

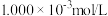 的混合溶液,混合体系中部分物种的浓度的负对数
的混合溶液,混合体系中部分物种的浓度的负对数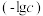 与pH关系如图所示。下列说法错误的是
与pH关系如图所示。下列说法错误的是
A.该溶液的温度为 |
B. 时,混合体系中浓度最高的含碳物种为 时,混合体系中浓度最高的含碳物种为 |
C.该条件下,H2CO3的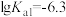 |
D. 的溶液中: 的溶液中: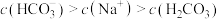 |
您最近一年使用:0次
2024-03-01更新
|
189次组卷
|
3卷引用:河南省沁阳一中2023—2024学年高二下学期开学考试 化学试卷
名校
8 . 下列有关乙醇的物理性质的应用不正确的是
| A.由于乙醇的密度比水小,故乙醇中的水可以通过分液的方法除去 |
| B.由于乙醇能够溶解很多有机物和无机物,故可用乙醇提取中药的有效成分 |
| C.由于乙醇能够以任意比溶解于水中,故酒厂可以勾兑各种浓度的酒 |
| D.由于乙醇容易挥发,故有“酒香不怕巷子深”的说法 |
您最近一年使用:0次
2024-03-01更新
|
512次组卷
|
5卷引用:河南省焦作市博爱县第一中学2023-2024学年高二下学期开学化学试题
名校
9 . 如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和电镀实验,其中乙装置中X为离子交换膜。请按要求回答相关问题:
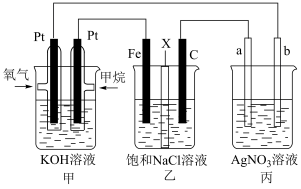
(1)甲烷燃料电池负极反应式是___________ 。
(2) 电极的电极反应式为
电极的电极反应式为___________ 。
(3)X选择___________ 离子交换膜(填“阴”或“阳”)。
(4)若在标准状况下,甲装置有112mL氧气参加反应,则乙装置中左侧极室的 为
为___________ 。(设该极室内溶液体积为 )
)
(5)若用丙装置给铜制品镀银,铜制品应放在___________ (填“a”或“b”)极,反应结束后 溶液的浓度
溶液的浓度___________ (填“变大”、“变小”或“不变”)。
(6)若a、b为惰性电极,写出图丙中电解总反应的离子反应方程式___________ 。

(1)甲烷燃料电池负极反应式是
(2)
 电极的电极反应式为
电极的电极反应式为(3)X选择
(4)若在标准状况下,甲装置有112mL氧气参加反应,则乙装置中左侧极室的
 为
为 )
)(5)若用丙装置给铜制品镀银,铜制品应放在
 溶液的浓度
溶液的浓度(6)若a、b为惰性电极,写出图丙中电解总反应的离子反应方程式
您最近一年使用:0次
2024-02-27更新
|
128次组卷
|
2卷引用:河南省沁阳一中2023—2024学年高二下学期开学考试 化学试卷
名校
解题方法
10 . 从炼锌厂废渣(含Zn、Co、Fe、ZnO、SiO2等)中回收钴并获得副产物ZnSO4的工艺流程如图:

已知:①常温下相关金属离子[c(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如表:
②酸浸后滤液中钴元素以Co2+形式存在
请回答下列问题:
(1)根据核外电子排布,钴元素位于周期表中___________ 区;酸浸过程中,提高“浸出率”的措施有___________ (任写一条);滤渣1的成分为___________ (填化学式)。
(2)向酸浸后的滤液中加入H2O2的目的是___________ ;调pH除铁选择的试剂X可以是___________ (填下面的字母);调节的pH范围是___________ 。
A.KOH B.Zn(OH)2 C.CoO D.Na2CO3
(3)操作1在实验室所用到的主要仪器为___________ ;该流程中可循环使用的物质是___________ 。
(4)除去Zn2+后,工业上也可利用碱性的次氯酸钠溶液氧化Co2+生成Co(OH)3沉淀,实现钴的回收,该反应的离子方程式为___________ 。
(5)已知Ksp(CoCO3)=1.5×10-13,Ksp(CoC2O4)=6.0×10-8,请判断能否利用如下反应CoCO3(s)+C2O (aq)
(aq) CoC2O4(s)+CO
CoC2O4(s)+CO (aq),将CoCO3转化为CoC2O4:
(aq),将CoCO3转化为CoC2O4:___________ (填“能”或“不能”),通过计算说明理由___________ 。

已知:①常温下相关金属离子[c(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如表:
| 金属离子 | Co2+ | Fe2+ | Fe3+ | Zn2+ |
| 开始沉淀的pH | 7.2 | 6.3 | 1.5 | 6.2 |
| 沉淀完全的pH | 9.2 | 8.3 | 2.8 | 8.2 |
请回答下列问题:
(1)根据核外电子排布,钴元素位于周期表中
(2)向酸浸后的滤液中加入H2O2的目的是
A.KOH B.Zn(OH)2 C.CoO D.Na2CO3
(3)操作1在实验室所用到的主要仪器为
(4)除去Zn2+后,工业上也可利用碱性的次氯酸钠溶液氧化Co2+生成Co(OH)3沉淀,实现钴的回收,该反应的离子方程式为
(5)已知Ksp(CoCO3)=1.5×10-13,Ksp(CoC2O4)=6.0×10-8,请判断能否利用如下反应CoCO3(s)+C2O
 (aq)
(aq) CoC2O4(s)+CO
CoC2O4(s)+CO (aq),将CoCO3转化为CoC2O4:
(aq),将CoCO3转化为CoC2O4:
您最近一年使用:0次
2024-02-27更新
|
384次组卷
|
2卷引用:河南省沁阳一中2023—2024学年高二下学期开学考试 化学试卷