1 . 25℃时, 的
的 和
和 各
各 分别加水稀释,
分别加水稀释, 随溶液体积变化如图所示。
随溶液体积变化如图所示。
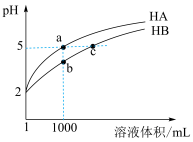
(1)属于强酸的是___________ 。
(2)溶液中的总酸量:a点___________ b点(填“>”或“<”)。
(3) 的电离程度:b点
的电离程度:b点___________ c点(填“>”或“<”)。
(4)将a点与b点两溶液同时升高温度,则 的值将
的值将___________ (填“增大”或“减小”)。
(5)常温下,若将HB溶液加水稀释则 的值将
的值将___________ (填“增大”“减小”或“无法判断”);若向
 的
的 溶液中逐滴滴入
溶液中逐滴滴入 的
的 溶液,所得溶液
溶液,所得溶液 及导电能力变化如图,则
及导电能力变化如图,则 两点水的电离程度:b
两点水的电离程度:b___________ c(填“>”“<”或“=”)。

(6)往 溶液中滴加
溶液中滴加 溶液至混合溶液显中性,则溶液中
溶液至混合溶液显中性,则溶液中
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(7)若已知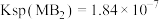 ,当
,当 离子完全沉淀时(即
离子完全沉淀时(即 离子浓度
离子浓度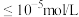 ),至少需要的
),至少需要的 离子浓度是
离子浓度是___________  (结果保留三位有效数字)。(已知
(结果保留三位有效数字)。(已知 )
)
 的
的 和
和 各
各 分别加水稀释,
分别加水稀释, 随溶液体积变化如图所示。
随溶液体积变化如图所示。
(1)属于强酸的是
(2)溶液中的总酸量:a点
(3)
 的电离程度:b点
的电离程度:b点(4)将a点与b点两溶液同时升高温度,则
 的值将
的值将(5)常温下,若将HB溶液加水稀释则
 的值将
的值将
 的
的 溶液中逐滴滴入
溶液中逐滴滴入 的
的 溶液,所得溶液
溶液,所得溶液 及导电能力变化如图,则
及导电能力变化如图,则 两点水的电离程度:b
两点水的电离程度:b
(6)往
 溶液中滴加
溶液中滴加 溶液至混合溶液显中性,则溶液中
溶液至混合溶液显中性,则溶液中
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(7)若已知
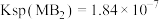 ,当
,当 离子完全沉淀时(即
离子完全沉淀时(即 离子浓度
离子浓度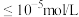 ),至少需要的
),至少需要的 离子浓度是
离子浓度是 (结果保留三位有效数字)。(已知
(结果保留三位有效数字)。(已知 )
)
您最近一年使用:0次
解题方法
2 . 回答下列问题:
(1)某基态原子的价层电子的轨道表示式为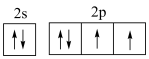
①s电子的电子云轮廓图是______________ 形
②有______________ 种空间运动状态不同的电子
③最外层有______________ 个电子
④有______________ 种能量不同的电子
(2)四种元素基态原子的电子排布式如下:①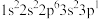 ;②
;② ;③
;③ ;④
;④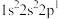
①第一电离能:①______________ ②(填“>”、“=”或“<”)
②电负性:③______________ ④(填“>”、“=”或“<”)
(1)某基态原子的价层电子的轨道表示式为

①s电子的电子云轮廓图是
②有
③最外层有
④有
(2)四种元素基态原子的电子排布式如下:①
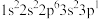 ;②
;② ;③
;③ ;④
;④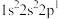
①第一电离能:①
②电负性:③
您最近一年使用:0次
解题方法
3 . 研究 对节能减排有重要意义,回答下列问题:
对节能减排有重要意义,回答下列问题:
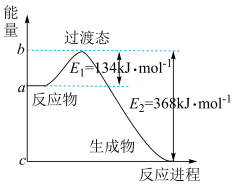
(1)如图是 和
和 反应生成
反应生成 和
和 过程中能量变化示意图,请写出
过程中能量变化示意图,请写出 和
和 反应的热化学方程式:
反应的热化学方程式:___________ ,若反应中转移了 ,则参加反应的
,则参加反应的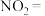
___________ g。
(2)已知反应: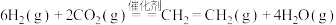 ,温度对
,温度对 的平衡转化率和催化剂催化效率的影响如图所示:
的平衡转化率和催化剂催化效率的影响如图所示:
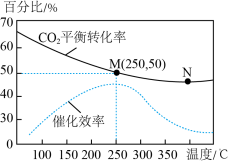
①此反应正反应为___________ 反应。
②化学平衡常数: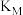
___________  (填“>”或“<”)。
(填“>”或“<”)。
③若初始投料比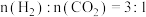 ,则图中
,则图中 点的乙烯体积分数约为
点的乙烯体积分数约为___________ 。
④ 时,
时,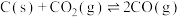 的平衡常数
的平衡常数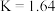 ,此反应的
,此反应的
___________ 0(填“>”或“<”),相同条件下测得高炉内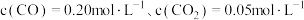 ,此时反应向
,此时反应向___________ (填“正”或“逆”)方向进行。
 对节能减排有重要意义,回答下列问题:
对节能减排有重要意义,回答下列问题:
(1)如图是
 和
和 反应生成
反应生成 和
和 过程中能量变化示意图,请写出
过程中能量变化示意图,请写出 和
和 反应的热化学方程式:
反应的热化学方程式: ,则参加反应的
,则参加反应的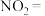
(2)已知反应:
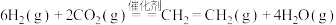 ,温度对
,温度对 的平衡转化率和催化剂催化效率的影响如图所示:
的平衡转化率和催化剂催化效率的影响如图所示:
①此反应正反应为
②化学平衡常数:
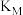
 (填“>”或“<”)。
(填“>”或“<”)。③若初始投料比
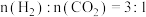 ,则图中
,则图中 点的乙烯体积分数约为
点的乙烯体积分数约为④
 时,
时,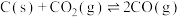 的平衡常数
的平衡常数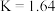 ,此反应的
,此反应的
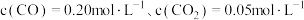 ,此时反应向
,此时反应向
您最近一年使用:0次
4 . 按要求回答问题:
(1)区分溶液与胶体最常用的方法______________ 。
(2)用量最大、用途最广的合金是______________ 。
(3)氡的放射性同位素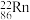 ,其原子中的质子数为
,其原子中的质子数为______________ 。
(4)用 溶液腐蚀印刷电路板的离子方程式
溶液腐蚀印刷电路板的离子方程式______________ 。
(5)只用一种试剂就可将 、稀
、稀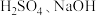 四种无色溶液区分开,该试剂是
四种无色溶液区分开,该试剂是______________ 。
(6)用 代表阿伏加德罗常数的值,
代表阿伏加德罗常数的值, 含有的电子数为
含有的电子数为______________  。
。
(7) 与足量
与足量 反应,转移的电子的物质的量为
反应,转移的电子的物质的量为______________  。
。
(8) 的结构式
的结构式______________ 。
(9)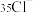 的结构示意图
的结构示意图______________ 。
(10)中子数为10的氟原子符号______________ 。
(11)甲烷分子的空间结构模型______________ 。
(1)区分溶液与胶体最常用的方法
(2)用量最大、用途最广的合金是
(3)氡的放射性同位素
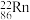 ,其原子中的质子数为
,其原子中的质子数为(4)用
 溶液腐蚀印刷电路板的离子方程式
溶液腐蚀印刷电路板的离子方程式(5)只用一种试剂就可将
 、稀
、稀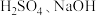 四种无色溶液区分开,该试剂是
四种无色溶液区分开,该试剂是(6)用
 代表阿伏加德罗常数的值,
代表阿伏加德罗常数的值, 含有的电子数为
含有的电子数为 。
。(7)
 与足量
与足量 反应,转移的电子的物质的量为
反应,转移的电子的物质的量为 。
。(8)
 的结构式
的结构式(9)
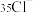 的结构示意图
的结构示意图(10)中子数为10的氟原子符号
(11)甲烷分子的空间结构模型
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题。
Ⅰ.写出下列反应的离子方程式
(1)醋酸与氢氧化钠溶液反应:___________ 。
(2)二氧化碳通入过量澄清石灰水中:___________ 。
(3)FeCl3腐蚀铜箔:___________ 。
(4)NH4HCO3与足量稀NaOH反应:___________ 。
Ⅱ.在标准状况下,有物质①4gH2,②33.6LCH4,③1molH2O,④ 个O2。
个O2。
(5)上述物质中,含分子数最多的是(填序号,下同)___________ ,含原子数最少的是___________ ,质量最大的是___________ 。密度由大到小的顺序为___________ 。
Ⅰ.写出下列反应的离子方程式
(1)醋酸与氢氧化钠溶液反应:
(2)二氧化碳通入过量澄清石灰水中:
(3)FeCl3腐蚀铜箔:
(4)NH4HCO3与足量稀NaOH反应:
Ⅱ.在标准状况下,有物质①4gH2,②33.6LCH4,③1molH2O,④
 个O2。
个O2。(5)上述物质中,含分子数最多的是(填序号,下同)
您最近一年使用:0次
名校
6 . 回答下列问题:
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
(2)磷的一种化合物叫亚磷酸(H3PO3)。已知:
Ⅰ.0.1mol/LH3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
①关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是___________ 。
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出H3PO3与过量NaOH溶液反应的离子方程式___________ 。
(3)H3PO2(次磷酸)是一元中强酸,H3PO2及NaH2PO2均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。
①NaH2PO2属于___________ (填“正盐”“酸式盐”或“碱式盐”)。
②利用H3PO2化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为___________ (写化学式)。
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
| A | B | C | D |
| 配制FeCl3溶液制备 | Fe(OH)3胶体 | 观察胶体的丁达尔效应 | 分离Fe(OH)3胶体与溶液 |
 |  |  | 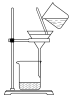 |
| A.A | B.B | C.C | D.D |
Ⅰ.0.1mol/LH3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
①关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出H3PO3与过量NaOH溶液反应的离子方程式
(3)H3PO2(次磷酸)是一元中强酸,H3PO2及NaH2PO2均可将溶液中的
 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。①NaH2PO2属于
②利用H3PO2化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
您最近一年使用:0次
名校
解题方法
7 . 铁及其重要化合物的“价类二维图”如图所示。
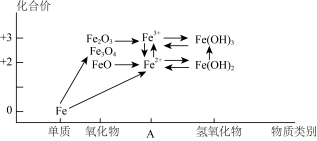
(1)该“价类二维图”中缺失的类别A应为_______ 。
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为________。
(3)要实现Fe转化为Fe3O4,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)_______ 。
(4)要实现Fe转化为Fe2+,可选用足量的_______ (填字母)
(5)为证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序:_______ 。
①加入适量的氯水 ②加入足量酸性KMnO4溶液 ③加入KSCN溶液
(6)氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是_______ 。

(1)该“价类二维图”中缺失的类别A应为
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为________。
| A.干垃圾 | B.湿垃圾 | C.有毒有害垃圾 | D.可回收垃圾 |
(3)要实现Fe转化为Fe3O4,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)
(4)要实现Fe转化为Fe2+,可选用足量的
| A.稀盐酸 | B.Fe2(SO4)3溶液 | C.稀硝酸 | D.浓硫酸 |
(5)为证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序:
①加入适量的氯水 ②加入足量酸性KMnO4溶液 ③加入KSCN溶液
| A.①③ | B.③② | C.③① | D.①②③ |
(6)氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是
| A.有铁无铜 | B.有铜无铁 | C.有铁有铜 | D.无铁无铜 |
您最近一年使用:0次
名校
8 . 回答下列问题:
(1)关于甲、乙、丙、丁四套装置的说法正确的是_______ 。

(2)以下物质(或粒子)与其用途之间关联正确的是_______ 。
(3)实验室制取Cl2的化学方程式:_______ 。浓盐酸表现的性质是_______ 。
(4)已知:在稀硫酸中,MnO 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。_______
(1)关于甲、乙、丙、丁四套装置的说法正确的是

| A.用装置甲制取氯气 | B.用丙装置可以较长时间看到白色Fe(OH)2白色沉淀 |
| C.用丁装置证明碳酸氢钠受热易分解 | D.用装置乙除去氢气中的少量氯化氢 |
| A.硬铝——制导线 | B.14C——测定文物年代 |
| C.锗——作半导体材料 | D.Ti-Fe合金——作不锈钢材料 |
(4)已知:在稀硫酸中,MnO
 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
您最近一年使用:0次
2023-09-24更新
|
325次组卷
|
4卷引用:天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题
天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题07 铁及其化合物 金属材料-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)(已下线)专项02 氧化还原反应的概念、规律及综合应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)山西运城盐湖五中2023-2024学年高一上学期化学期末练兵卷(三)
名校
解题方法
9 . 以下物质,按要求填序号。
①MgCl2 ②NH4Cl ③Na2O2 ④N2 ⑤H2S ⑥H2O2 ⑦CO2 ⑧CaO
只含有极性键的物质是_______ ;只含有非极性键的物质是_______ ;既含有极性键又含有非极性键的物质是_______ ;既含有共价键又含有离子键的物质是_______ ;只含有离子键的离子化合物的是______ 。
①MgCl2 ②NH4Cl ③Na2O2 ④N2 ⑤H2S ⑥H2O2 ⑦CO2 ⑧CaO
只含有极性键的物质是
您最近一年使用:0次
2023-09-24更新
|
411次组卷
|
3卷引用:天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题
天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题10 化学键-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)新疆巴楚县第一中学2023-2024学年高一上学期1月期末化学试题
名校
10 . 书写以下化学用语。
(1)CO2电子式:________ 。
(2)NaHSO4溶于水的电离方程式:________ 。
(3)铁与氯气在加热条件下的化学方程式:________ 。
(4)氯化铝溶液与过量氢氧化钠反应的离子方程式:_________ 。
(5)Fe3O4溶于稀硫酸的离子方程式:________ 。
(1)CO2电子式:
(2)NaHSO4溶于水的电离方程式:
(3)铁与氯气在加热条件下的化学方程式:
(4)氯化铝溶液与过量氢氧化钠反应的离子方程式:
(5)Fe3O4溶于稀硫酸的离子方程式:
您最近一年使用:0次



