名校
解题方法
1 . 下表为周期表的一部分,其中的编号代表对应的元素。请回答下列问题:
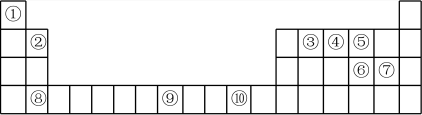
(1)表中属于d区的元素是_____ (填序号)。
(2)写出元素⑨的基态原子的核外电子排布式_____ ,元素⑩的价电子轨道表示式_____ 。
(3)表中所给元素中,原子半径最大的是_____ (填元素符号),元素⑥、⑦形成的简单离子半径更小的是_____ (填离子符号)。
(4)下列关于元素③、④分别与①形成的简单化合物的叙述正确的是_____(填序号)。
(5)元素④、⑤的第一电离更大的是_____ (填元素符号)。
(6)元素②与元素⑦形成的分子的空间结构为_____ 。

(1)表中属于d区的元素是
(2)写出元素⑨的基态原子的核外电子排布式
(3)表中所给元素中,原子半径最大的是
(4)下列关于元素③、④分别与①形成的简单化合物的叙述正确的是_____(填序号)。
| A.中心原子的价层电子对数相同 |
| B.中心原子的杂化方式不同 |
| C.分子的VSEPR模型相同,空间结构也相同 |
| D.④与①形成的分子的键角比③与①形成的分子的键角更大 |
(5)元素④、⑤的第一电离更大的是
(6)元素②与元素⑦形成的分子的空间结构为
您最近一年使用:0次
2023-12-12更新
|
594次组卷
|
2卷引用:天津市实验中学2023-2024学年高三上学期第二次阶段检测化学试题
2 . 尿素[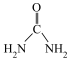 ]是一种中性的对土壤的破坏作用小的肥料,其合成方法有多种:其熔点、沸点分别为132.7℃、196.6℃,加热至150℃不稳定;其溶解度随温度升高而增大。
]是一种中性的对土壤的破坏作用小的肥料,其合成方法有多种:其熔点、沸点分别为132.7℃、196.6℃,加热至150℃不稳定;其溶解度随温度升高而增大。
(1)尿素分子中N原子杂化方式为___________ 。推测尿素常温下溶水性难易并阐述理由___________ 。
(2)十九世纪初,用氰酸银(AgOCN)与 在一定条件下反应可制得尿素和另一种产物A实现了由无机物到有机物的合成。A的化学式为
在一定条件下反应可制得尿素和另一种产物A实现了由无机物到有机物的合成。A的化学式为___________ ;假设该反应恰好反应完全,简述将尿素从产物样品中进行分离方法:___________ 。
(3)近年研究发现,电催化 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的 溶液通入
溶液通入 至饱和,在电极上反应生成
至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。

①电极X作电解池的___________ 极。
②右池溶液中每产生22.4L(标准状况下) 时,产生
时,产生
___________ mol。
③写出电解过程中生成尿素的电极反应式:___________ 。
(4)尿素样品含氮量的测定方法如下。
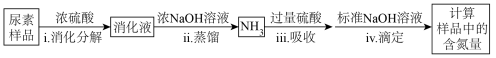
①消化液中的含氮离子是___________ ;
②步骤ⅱ的离子方程式为___________ 。
③重复步骤iv三次有效实验,消耗c mo/L的标准NaOH溶液的平均体积V L。计算样品含氮量时,还需要的实验数据有样品的质量、步骤ⅲ所加入 溶液的
溶液的___________ 。
 ]是一种中性的对土壤的破坏作用小的肥料,其合成方法有多种:其熔点、沸点分别为132.7℃、196.6℃,加热至150℃不稳定;其溶解度随温度升高而增大。
]是一种中性的对土壤的破坏作用小的肥料,其合成方法有多种:其熔点、沸点分别为132.7℃、196.6℃,加热至150℃不稳定;其溶解度随温度升高而增大。(1)尿素分子中N原子杂化方式为
(2)十九世纪初,用氰酸银(AgOCN)与
 在一定条件下反应可制得尿素和另一种产物A实现了由无机物到有机物的合成。A的化学式为
在一定条件下反应可制得尿素和另一种产物A实现了由无机物到有机物的合成。A的化学式为(3)近年研究发现,电催化
 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的 溶液通入
溶液通入 至饱和,在电极上反应生成
至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。
①电极X作电解池的
②右池溶液中每产生22.4L(标准状况下)
 时,产生
时,产生
③写出电解过程中生成尿素的电极反应式:
(4)尿素样品含氮量的测定方法如下。

①消化液中的含氮离子是
②步骤ⅱ的离子方程式为
③重复步骤iv三次有效实验,消耗c mo/L的标准NaOH溶液的平均体积V L。计算样品含氮量时,还需要的实验数据有样品的质量、步骤ⅲ所加入
 溶液的
溶液的
您最近一年使用:0次
解题方法
3 . 铁及其化合物在生产、生活中有着重要作用。按要求回答下列问题。
(1)基态Fe原子的价层电子排布式为___________ ;铁元素在元素周期表中的位置是___________ ,属于___________ 区。
(2)铁及其化合物A~E的分类分布及其转化关系如下图所示:
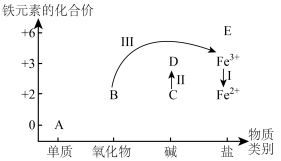
①从图中(A~E)选择反应物,实现Ⅰ的转化,写出反应Ⅰ的离子方程式:___________ 。
②预测物质E中铁元素具有___________ (填“氧化性”或“还原性”)。
③写出反应Ⅱ的化学方程式:___________ 。
④实现反应Ⅲ的转化,可选择含N元素的试剂为___________ 。
(3)探究铁盐X的组成与性质(忽略过程中氧气的参与)
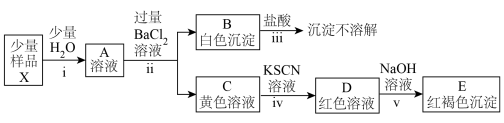
①由步骤ⅰ及其现象可推知铁盐X的物理性质:___________ 。
②由步骤ⅱ、ⅲ及其现象可推知该铁盐X中含有的阴离子为___________ 。
③C溶液呈黄色,不可能是因其体系中含有的___________ 、___________ 、___________ 、___________ (填离子符号)所致;
而可能是因其体系中含有的___________ 、___________ (填粒子的化学式)等所致。
④由步骤iv、v及其现象,体系中与 结合能力最强的离子是
结合能力最强的离子是___________ 。
(1)基态Fe原子的价层电子排布式为
(2)铁及其化合物A~E的分类分布及其转化关系如下图所示:

①从图中(A~E)选择反应物,实现Ⅰ的转化,写出反应Ⅰ的离子方程式:
②预测物质E中铁元素具有
③写出反应Ⅱ的化学方程式:
④实现反应Ⅲ的转化,可选择含N元素的试剂为
(3)探究铁盐X的组成与性质(忽略过程中氧气的参与)

①由步骤ⅰ及其现象可推知铁盐X的物理性质:
②由步骤ⅱ、ⅲ及其现象可推知该铁盐X中含有的阴离子为
③C溶液呈黄色,不可能是因其体系中含有的
而可能是因其体系中含有的
④由步骤iv、v及其现象,体系中与
 结合能力最强的离子是
结合能力最强的离子是
您最近一年使用:0次
4 . 物质类别和元素价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价—类”二维图,请回答下列问题:
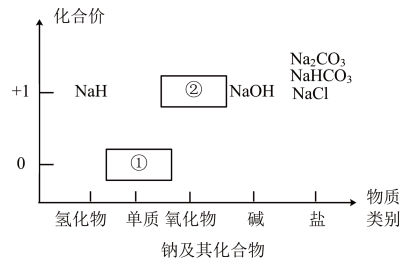
(1)①与水反应的离子方程式为______ ;通常将①的固体保存在______ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式为______ 。
(3)从元素价态的视角看, 中氢元素的化合价为
中氢元素的化合价为______ 价,从H的价态分析, 常用作
常用作______ (填“氧化剂”或“还原剂”), 与水反应生成一种强碱和可燃性气体,反应的化学方程式为
与水反应生成一种强碱和可燃性气体,反应的化学方程式为______ 。
(4)纯碱和小苏打都是重要的化工原料,根据不列三组实验,回答:
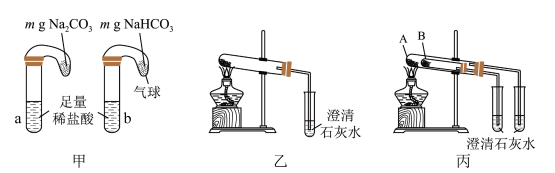
①甲组实验能鉴别纯碱和小苏打的实验现象是______ ;试管b中发生反应的离子方程式为______ 。
②乙、丙两组实验中,______ 组能更便捷的验证两者的热稳定性(填“乙”或“丙”),丙组实验中A处盛放的物质为______ (填化学式)。

(1)①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式为
(3)从元素价态的视角看,
 中氢元素的化合价为
中氢元素的化合价为 常用作
常用作 与水反应生成一种强碱和可燃性气体,反应的化学方程式为
与水反应生成一种强碱和可燃性气体,反应的化学方程式为(4)纯碱和小苏打都是重要的化工原料,根据不列三组实验,回答:

①甲组实验能鉴别纯碱和小苏打的实验现象是
②乙、丙两组实验中,
您最近一年使用:0次
5 . 牙膏是由粉状摩擦剂、湿润剂、表面活性剂、黏合剂、香料、甜味剂及其他特殊成分构成。下表列出了两种牙膏中的摩擦剂。
(1)摩擦剂碳酸钙的物质类别为______ (填“酸”、“碱”、“盐”或“氧化物”),推测上述两种摩擦剂都______ (填“可溶”或“难溶”)于水。
(2)已知二氧化硅的化学式为 ,能与
,能与 溶液反应硅酸钠和水,由此可知
溶液反应硅酸钠和水,由此可知 属于
属于______ (填“酸性”或“碱性”)氧化物。 也具有类似的性质,写出少量
也具有类似的性质,写出少量 与
与 溶液反应的化学方程式:
溶液反应的化学方程式:______ 。
| 牙膏 | Y牙膏 | Z牙膏 |
| 摩擦剂 | 碳酸钙 | 二氧化硅 |
(1)摩擦剂碳酸钙的物质类别为
(2)已知二氧化硅的化学式为
 ,能与
,能与 溶液反应硅酸钠和水,由此可知
溶液反应硅酸钠和水,由此可知 属于
属于 也具有类似的性质,写出少量
也具有类似的性质,写出少量 与
与 溶液反应的化学方程式:
溶液反应的化学方程式:
您最近一年使用:0次
6 . 物质的分类与转化思路建构是形成“证据推理与模型认知”素养的关键。
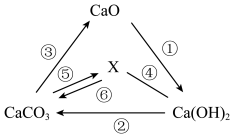
(1)部分含钙元素的物质之间转化关系如图所示,“______”表示物质之间能发生化学反应,“→”表示物质之间可以转化,其中X含两种元素。
①X的化学式为______ ;
②写出反应⑤的离子方程式______ 。
(2)某工厂要综合处理工业废气(主要含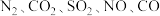 和含
和含 的废水,设计如图流程(已知亚硫酸钙难溶于水):
的废水,设计如图流程(已知亚硫酸钙难溶于水):
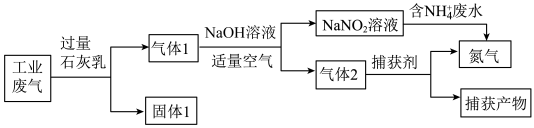
①在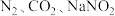 溶液、
溶液、 中属于电解质的是
中属于电解质的是______ 。(填化学式)。
②固体1中除含有 外,还含有
外,还含有______ 、______ 。
③生成 的反应为
的反应为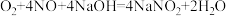
 用单线桥法标定反应中电子转移的方向和数目
用单线桥法标定反应中电子转移的方向和数目______ 。
④处理含 的废水时,若3.6g
的废水时,若3.6g 参加反应,需要
参加反应,需要 的质量为
的质量为______ g。

(1)部分含钙元素的物质之间转化关系如图所示,“______”表示物质之间能发生化学反应,“→”表示物质之间可以转化,其中X含两种元素。
①X的化学式为
②写出反应⑤的离子方程式
(2)某工厂要综合处理工业废气(主要含
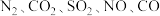 和含
和含 的废水,设计如图流程(已知亚硫酸钙难溶于水):
的废水,设计如图流程(已知亚硫酸钙难溶于水):
①在
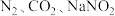 溶液、
溶液、 中属于电解质的是
中属于电解质的是②固体1中除含有
 外,还含有
外,还含有③生成
 的反应为
的反应为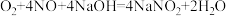
 用单线桥法标定反应中电子转移的方向和数目
用单线桥法标定反应中电子转移的方向和数目④处理含
 的废水时,若3.6g
的废水时,若3.6g 参加反应,需要
参加反应,需要 的质量为
的质量为
您最近一年使用:0次
7 . 某小组以盐酸、醋酸为例探究其酸性的强弱。按要求回答下列问题。
(1)取相同体积、相同浓度的盐酸和醋酸,分别测其pH和导电能力,对比分析,在下表填写空白。已知: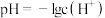
③此温度下,CH3COOH的电离平衡常数Ka=___________ (填计算式,不化简)。
(2)在上述醋酸溶液中加入如下表所示物质,分析其中粒子的变化等,填写空白。
(3)向两个锥形瓶中各加入0.06g镁条,塞紧橡胶塞,然后用注射器分别注入2mL 2mol/L盐酸、2mol/L醋酸。
①反应前n(Mg)=___________ mol;充分反应后,剩余的n(Mg)=___________ mol。
②两锥形瓶内气体n随时间变化,对比分析后,在如下坐标中将示意曲线补充完整。___________

(1)取相同体积、相同浓度的盐酸和醋酸,分别测其pH和导电能力,对比分析,在下表填写空白。已知:
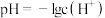
| 酸 | 0.1mol/L盐酸 | 0.1mol/L醋酸 | |
| pH(25℃) | 1 | 3 | |
| 导电能力 | 强 | 弱 | |
| 分析与结论 | ①微观解释(写出溶质在溶液中的存在形式,填粒子的化学式) | ||
| ②电离方程式 | |||
(2)在上述醋酸溶液中加入如下表所示物质,分析其中粒子的变化等,填写空白。
| 加入少量的物质 | 醋酸电离平衡移动方向 填“→”“←”或“不移动” | c(H⁺)/c(CH3COOH)比值变化 填“变大”“变小”或“不变” |
| ①CH3COONa(s) | ||
| ②水 |
(3)向两个锥形瓶中各加入0.06g镁条,塞紧橡胶塞,然后用注射器分别注入2mL 2mol/L盐酸、2mol/L醋酸。
①反应前n(Mg)=
②两锥形瓶内气体n随时间变化,对比分析后,在如下坐标中将示意曲线补充完整。

您最近一年使用:0次
8 . 乙烯的产量通常用来衡量一个国家的石油化工水平。请回答下列问题:
(1)乙烯的电子式___________ ,结构简式___________ 。
(2)鉴别甲烷和乙烯的试剂是___________(填序号)。
(3)下列物质中,可以通过乙烯加成反应得到的是___________(填序号)。
(4)聚氯乙烯(简称PVC),如果用于食品包装,会对食品的安全性有一定的影响。PVC可由氯乙烯(CH2=CH-Cl)在一定条件下发生加聚反应制得,PVC的结构可表示为___________ 。
(1)乙烯的电子式
(2)鉴别甲烷和乙烯的试剂是___________(填序号)。
| A.稀硫酸 | B.溴的四氯化碳溶液 | C.水 | D.酸性高锰酸钾溶液 |
| A.CH3CH3 | B.CH3CH2Br | C.CH3CH2OH | D.ClCH2CH2Cl |
您最近一年使用:0次
名校
解题方法
9 . 烷烃结构的性质与甲烷类似。请回答下列问题。
(1)相对分子质量为72的烷烃的分子式为___________ 。
(2)异丁烷与异戊烷的关系为___________(填字母)。
(3)写出乙烷和氯气反应的化学方程式(只写第一步)___________ 。
(4)标准状况下,等物质的量的甲烷和乙烷完全燃烧,消耗的氧气的物质的量之比为___________ 。
(5)标准状况下,等质量的甲烷和乙烷完全燃烧,消耗的氧气的质量之比为___________ 。
(1)相对分子质量为72的烷烃的分子式为
(2)异丁烷与异戊烷的关系为___________(填字母)。
| A.同素异形体 | B.同一种物质 | C.同分异构体 | D.同系物 |
(4)标准状况下,等物质的量的甲烷和乙烷完全燃烧,消耗的氧气的物质的量之比为
(5)标准状况下,等质量的甲烷和乙烷完全燃烧,消耗的氧气的质量之比为
您最近一年使用:0次
10 . 含氮元素的化合物的转化关系如图所示,按要求书写化学方程式。

(1)反应①实验室制氨气:___________ 。
(2)反应②氨的催化氧化:___________ 。
(3)反应③的化学方程式为___________ 。
(4)反应④硝酸具有不稳定性:___________ 。
(5)反应⑤铜和稀硝酸反应:___________ 。

(1)反应①实验室制氨气:
(2)反应②氨的催化氧化:
(3)反应③的化学方程式为
(4)反应④硝酸具有不稳定性:
(5)反应⑤铜和稀硝酸反应:
您最近一年使用:0次



