解题方法
1 . 我国科学家制备了高选择性的二氧化碳加氢合成甲醇的催化剂氧化锆,其晶胞如下图所示。
(2)结合图中数据,计算该晶胞的密度ρ=___________ g·cm−3。(设NA为阿伏加德罗常数,用含a、b和NA的代数式表示)

| A.ZrO2 | B.ZrO | C.Zr2O | D.Zr2O3 |
(2)结合图中数据,计算该晶胞的密度ρ=
您最近一年使用:0次
2 . 为测定莫尔盐[(NH4)2SO4·FeSO4·6H2O](相对分子质量为392)的纯度,某同学取m g样品配制成500mL溶液,取20.00mL溶液用0.1000mol·L−1KMnO4酸性溶液进行滴定(MnO +5Fe2++8H+=5Fe3++Mn2++4H2O),实验数据如下表:
+5Fe2++8H+=5Fe3++Mn2++4H2O),实验数据如下表:
(1)计算该莫尔盐样品的纯度___________ 。(写出计算过程)
(2)再设计一个测定m g莫尔盐样品纯度的实验方案。___________
 +5Fe2++8H+=5Fe3++Mn2++4H2O),实验数据如下表:
+5Fe2++8H+=5Fe3++Mn2++4H2O),实验数据如下表:| 实验次数 | 1 | 2 | 3 | 4 |
| KMnO4酸性溶液体积/mL | 19.98 | 20.02 | 21.65 | 20.00 |
(2)再设计一个测定m g莫尔盐样品纯度的实验方案。
| 实验原理(用离子方程式表示) | 测定的物理量 |
您最近一年使用:0次
名校
3 . 现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44 L。回答下列问题,并写出计算过程:
(1)该混合气体中CO与CO2的分子数之比___________ 。
(2)混合气体中氧原子的物质的量为___________ 。
(3)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。
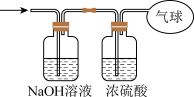
①气球中收集到的气体的摩尔质量为___________ 。
②该气球的体积为___________ 。
(1)该混合气体中CO与CO2的分子数之比
(2)混合气体中氧原子的物质的量为
(3)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。

①气球中收集到的气体的摩尔质量为
②该气球的体积为
您最近一年使用:0次
名校
解题方法
4 . 在49g硫酸中含有______ 个硫酸分子,中和这些硫酸需要氢氧化钠______ mol。
您最近一年使用:0次
5 . 回答下列问题
(1)在标准状况下2.24LCO与CO2混合气的总质量为3.7g,则混合气体中CO与CO2的分子数之比为_______
(2)甲烷(CH4)与氧气的质量比为1:4时极易爆炸,此时甲烷与氧气的体积之比为_______ 。
(3)某人的血糖化验单显示血液中葡萄糖(C6H12O6,M=180g/mol)为 ,此人1mL血液中含葡萄糖
,此人1mL血液中含葡萄糖_______ mg。
(1)在标准状况下2.24LCO与CO2混合气的总质量为3.7g,则混合气体中CO与CO2的分子数之比为
(2)甲烷(CH4)与氧气的质量比为1:4时极易爆炸,此时甲烷与氧气的体积之比为
(3)某人的血糖化验单显示血液中葡萄糖(C6H12O6,M=180g/mol)为
 ,此人1mL血液中含葡萄糖
,此人1mL血液中含葡萄糖
您最近一年使用:0次
名校
6 . 计算25 ℃时下列溶液的pH:
(1)1 mL pH=2的 溶液加水稀释至100 mL,pH=
溶液加水稀释至100 mL,pH=_______ ;
(2)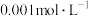 的盐酸,pH=
的盐酸,pH=_______ ;
(3) 的NaOH溶液,pH=
的NaOH溶液,pH=_______ ;
(1)1 mL pH=2的
 溶液加水稀释至100 mL,pH=
溶液加水稀释至100 mL,pH=(2)
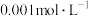 的盐酸,pH=
的盐酸,pH=(3)
 的NaOH溶液,pH=
的NaOH溶液,pH=
您最近一年使用:0次
2022-10-06更新
|
372次组卷
|
2卷引用:上海市市西中学2022-2023学年高二上学期期末考试化学试题
7 . CO和CO2的混合气体18 g,完全燃烧后测得CO2体积为11.2 L(标准状况)。试回答:
(1)混合气体中CO的质量是_______ g。
(2)混合气体中CO2在标准状况下的体积是多少_______ L。
(3)等质量CO和CO2分子个数比是_______ ;原子个数比是_______ ;等温等压下体积比是_______ 。
(1)混合气体中CO的质量是
(2)混合气体中CO2在标准状况下的体积是多少
(3)等质量CO和CO2分子个数比是
您最近一年使用:0次
名校
8 . 一个SO2分子的质量为a g,一个SO3分子的质量为b g,若以氧原子质量的1/8为标准,则SO2的相对分子质量为_______ ,硫的相对原子质量为_______ 。 (用a、b表示)
您最近一年使用:0次
12-13高二下·上海静安·期中
9 . 将2.24L(标准状况)的氯气通入30.00mL密度为1.33g/cm3的10.000 mol/L氢氧化钠热溶液中,生成NaCl 、NaClO 、NaClO3和H2O,其中NaCl为 0.16 mol。
(1)标准状况下, 2.24L氯气的物质的量为________ mol。
(2)氢氧化钠溶液的质量分数为______ %(保留两位小数)。
(3)反应所得溶液中NaClO 和NaClO3的物质的量共为________ mol。
(4)含氯消毒剂杀菌后氯元素均以-1价态存在。试通过计算回答,上述反应所得溶液的杀菌能力相当于多少mL0.1000mol/L次氯酸钙溶液的的杀菌能力______ ?
(1)标准状况下, 2.24L氯气的物质的量为
(2)氢氧化钠溶液的质量分数为
(3)反应所得溶液中NaClO 和NaClO3的物质的量共为
(4)含氯消毒剂杀菌后氯元素均以-1价态存在。试通过计算回答,上述反应所得溶液的杀菌能力相当于多少mL0.1000mol/L次氯酸钙溶液的的杀菌能力
您最近一年使用:0次
10 . I.中国科学家制得一种蓝色钨的氧化物(WOa ),其中钨的质量分数为 0.7985。
(1)a=______ (保留2位小数)。
(2)WOa中存在五价和六价两种价态的钨。则蓝色钨的氧化物中这两种价态的钨原子数之比为________ 。
II.将铁锰的钨酸盐[(Fe,Mn)WO4]碱熔,发生如下反应(设空气中N2、O2的体积分数分别为0.8和0.2):
4FeWO4+4 Na2CO3+ O2 4 Na2WO4+ 2Fe2O3+ 4CO2 ①
4 Na2WO4+ 2Fe2O3+ 4CO2 ①
2MnWO4+2Na2CO3+ O2 2 Na2WO4+ 2MnO2+ 2CO2 ②
2 Na2WO4+ 2MnO2+ 2CO2 ②
(1)根据反应①,若反应前空气为100L,反应后气体为160L(气体体积在同温同压下测定),则反应后所得气体中CO2的体积分数为_________ 。
(2)某工厂投料550 mol Na2CO3制备Na2WO4,每反应1mol O2时,气体就增加1.5mol,则生成物中Fe2O3与MnO2的物质的量之比为_________ ;若反应后气体增加300 mol,制得Na2WO4_____ mol。
III.由Na2WO4制备W的第一步反应为:Na2WO4+2HCl→H2WO4↓+2NaCl。往1L密度为1.190g /cm3的37%的浓盐酸加入6.030 mol Na2WO4,恰好完全反应。将产生的沉淀过滤后,溶液中溶质只有NaCl,求该溶液中NaCl的质量分数(25℃时NaCl的溶解度为36.0 g/100 g水)______________
(1)a=
(2)WOa中存在五价和六价两种价态的钨。则蓝色钨的氧化物中这两种价态的钨原子数之比为
II.将铁锰的钨酸盐[(Fe,Mn)WO4]碱熔,发生如下反应(设空气中N2、O2的体积分数分别为0.8和0.2):
4FeWO4+4 Na2CO3+ O2
 4 Na2WO4+ 2Fe2O3+ 4CO2 ①
4 Na2WO4+ 2Fe2O3+ 4CO2 ①2MnWO4+2Na2CO3+ O2
 2 Na2WO4+ 2MnO2+ 2CO2 ②
2 Na2WO4+ 2MnO2+ 2CO2 ②(1)根据反应①,若反应前空气为100L,反应后气体为160L(气体体积在同温同压下测定),则反应后所得气体中CO2的体积分数为
(2)某工厂投料550 mol Na2CO3制备Na2WO4,每反应1mol O2时,气体就增加1.5mol,则生成物中Fe2O3与MnO2的物质的量之比为
III.由Na2WO4制备W的第一步反应为:Na2WO4+2HCl→H2WO4↓+2NaCl。往1L密度为1.190g /cm3的37%的浓盐酸加入6.030 mol Na2WO4,恰好完全反应。将产生的沉淀过滤后,溶液中溶质只有NaCl,求该溶液中NaCl的质量分数(25℃时NaCl的溶解度为36.0 g/100 g水)
您最近一年使用:0次



