名校
1 .  、
、 、
、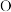 、
、 、
、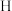 、
、 都是中学化学中常见的元素。按要求完成下列填空。
都是中学化学中常见的元素。按要求完成下列填空。
(1) 分子中含
分子中含_______  氧原子、
氧原子、_______ 个氢原子。
(2)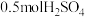 的质量为
的质量为_______ ;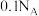 个
个 所含
所含 的物质的量为
的物质的量为_______ 。等物质的量的 和
和 两种气体,所含原子数之比为
两种气体,所含原子数之比为_______ ,等质量的 和
和 物质的量之比为
物质的量之比为_______ 。
(3)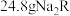 含
含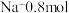 ,则
,则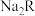 物质的量为
物质的量为_______ ,摩尔质量为_______ 。
(4)现有 某气体,该气体分子为双原子分子。它的摩尔质量为
某气体,该气体分子为双原子分子。它的摩尔质量为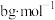 若阿伏加德罗常数用
若阿伏加德罗常数用 表示,则:
表示,则:
①该气体的物质的量为_______  ;
;
②该气体所含原子总数为_______ 个。
 、
、 、
、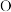 、
、 、
、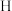 、
、 都是中学化学中常见的元素。按要求完成下列填空。
都是中学化学中常见的元素。按要求完成下列填空。(1)
 分子中含
分子中含 氧原子、
氧原子、(2)
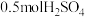 的质量为
的质量为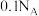 个
个 所含
所含 的物质的量为
的物质的量为 和
和 两种气体,所含原子数之比为
两种气体,所含原子数之比为 和
和 物质的量之比为
物质的量之比为(3)
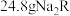 含
含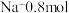 ,则
,则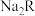 物质的量为
物质的量为(4)现有
 某气体,该气体分子为双原子分子。它的摩尔质量为
某气体,该气体分子为双原子分子。它的摩尔质量为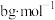 若阿伏加德罗常数用
若阿伏加德罗常数用 表示,则:
表示,则:①该气体的物质的量为
 ;
;②该气体所含原子总数为
您最近一年使用:0次
2 . 电解饱和食盐水是“氯碱工业”的重要反应。当两极共产生气体2.5mol时(假设气体全部逸出),食盐完全电解。已知20℃时,食盐的溶解度为36克/100克水。试求:
(1)电解时消耗的氯化钠的物质的量_________ ;
(2)电解时所取饱和食盐水的质量_________ ;
(3)电解后所得NaOH溶液的质量分数_________ 。
(1)电解时消耗的氯化钠的物质的量
(2)电解时所取饱和食盐水的质量
(3)电解后所得NaOH溶液的质量分数
您最近一年使用:0次
名校
解题方法
3 . 容积为1升的干燥容器中充入氯化氢气体后,测得容器内气体对氢气的相对密度为17。容器内气体的平均相对分子质量是______ ,用此气体进行喷泉实验,当喷泉停止后,进入容器中的液体的体积是______ L。
您最近一年使用:0次
名校
4 . 同温同压下,等质量的CO2和CO的物质的量之比为______ ,体积之比为_______ ,原子数之比为______ ,密度之比为_______ 。
您最近一年使用:0次
11-12高三上·上海长宁·期末
解题方法
5 . 在标准状况下进行下列实验:甲、乙、丙各取30.00mL同浓度的盐酸,加入同一镁、铝合金,产生气体,测得有关数据列表如下:
(1)分析上表数据后填空:
①盐酸的物质的量浓度为__________ mol/L,在表中可作为计算依据的是(填实验序号,要求全部写出)_______________
②据(填实验序号)__________ 中的数据,可计算出合金中镁与铝的物质的量之比为__________________
(2)在丙实验之后,向容器中加入一定量1.00mol/L的NaOH溶液,使合金中的铝恰好完全溶解,再滤出不溶固体请计算:
①滤液中溶质的物质的量______________ 。
②加入NaOH溶液的体积______________ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量 | 0.255g | 0.385g | 0.459g |
| 气体体积 | 280mL | 336mL | 336mL |
(1)分析上表数据后填空:
①盐酸的物质的量浓度为
②据(填实验序号)
(2)在丙实验之后,向容器中加入一定量1.00mol/L的NaOH溶液,使合金中的铝恰好完全溶解,再滤出不溶固体请计算:
①滤液中溶质的物质的量
②加入NaOH溶液的体积
您最近一年使用:0次
11-12高三上·上海长宁·期末
6 . 将a mol的 和
和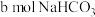 固体混合后,在密闭容器中加热到250℃,让其充分反应,假设
固体混合后,在密闭容器中加热到250℃,让其充分反应,假设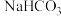 分解产生的
分解产生的 与
与 反应完后,
反应完后, 再与
再与 反应.
反应.
(1)当剩余固体只有 ,排出气体中
,排出气体中 的物质的量为
的物质的量为 ____________ (用含a或b的代数式表示)
(2)当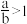 时,剩余固体是
时,剩余固体是________ ,排出气体是________ 。
(3)当剩余固体为 ,NaOH,排出气体为
,NaOH,排出气体为 ,
, 时,
时, 的值为
的值为________ .
(3)当排出的 和
和 为等物质的量时,则
为等物质的量时,则 的值为
的值为________ .
 和
和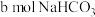 固体混合后,在密闭容器中加热到250℃,让其充分反应,假设
固体混合后,在密闭容器中加热到250℃,让其充分反应,假设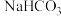 分解产生的
分解产生的 与
与 反应完后,
反应完后, 再与
再与 反应.
反应.(1)当剩余固体只有
 ,排出气体中
,排出气体中 的物质的量为
的物质的量为 (2)当
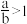 时,剩余固体是
时,剩余固体是(3)当剩余固体为
 ,NaOH,排出气体为
,NaOH,排出气体为 ,
, 时,
时, 的值为
的值为(3)当排出的
 和
和 为等物质的量时,则
为等物质的量时,则 的值为
的值为
您最近一年使用:0次
解题方法
7 . 绿矾(FeSO4•7H2O)在化学合成上用作还原剂及催化剂,工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾。
(1)98% 1.84g/cm3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4g/cm3,50%的硫酸物质的量浓度为______ (保留两位小数),50%的硫酸与30%的硫酸等体积混合,混合酸的浓度为______ (填>、<、=)40%。
(2)实际生产用20%发烟硫酸(100克发烟硫酸含SO320克)配制稀硫酸,若用SO3•nH2O表示20%的发烟硫酸,则n=______ (保留两位小数)。
(3)某厂废水中含1.00×10﹣3mol/L的Cr2O72-,其毒性较大.某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合价为+3,Fe的化合价依次为+3、+2).欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4.理论上需要加入______ g FeSO4•7H2O。
(4)硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O](俗称莫尔盐),较绿矾稳定,在分析化学中常用来配制Fe2+的标准溶液,用此Fe2+的标准溶液可以测定剩余稀硝酸的量.现取8.64克Cu2S和CuS的混合物用200mL2mol/L稀硝酸溶液处理,发生反应如下:
10NO3﹣+3Cu2S+16H+→6Cu2++10NO↑+3SO42﹣+8H2O
8NO3﹣+3CuS+8H+→3Cu2++3 SO42﹣+8NO↑+4H2O
剩余的稀硝酸恰好与48mL 2mol/L (NH4)2Fe(SO4)2溶液完全反应.
已知:NO3﹣+3Fe2++4H+→NO↑+3Fe3++2H2O
试计算混合物中CuS的质量分数(保留两位小数)。______________
(1)98% 1.84g/cm3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4g/cm3,50%的硫酸物质的量浓度为
(2)实际生产用20%发烟硫酸(100克发烟硫酸含SO320克)配制稀硫酸,若用SO3•nH2O表示20%的发烟硫酸,则n=
(3)某厂废水中含1.00×10﹣3mol/L的Cr2O72-,其毒性较大.某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合价为+3,Fe的化合价依次为+3、+2).欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4.理论上需要加入
(4)硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O](俗称莫尔盐),较绿矾稳定,在分析化学中常用来配制Fe2+的标准溶液,用此Fe2+的标准溶液可以测定剩余稀硝酸的量.现取8.64克Cu2S和CuS的混合物用200mL2mol/L稀硝酸溶液处理,发生反应如下:
10NO3﹣+3Cu2S+16H+→6Cu2++10NO↑+3SO42﹣+8H2O
8NO3﹣+3CuS+8H+→3Cu2++3 SO42﹣+8NO↑+4H2O
剩余的稀硝酸恰好与48mL 2mol/L (NH4)2Fe(SO4)2溶液完全反应.
已知:NO3﹣+3Fe2++4H+→NO↑+3Fe3++2H2O
试计算混合物中CuS的质量分数(保留两位小数)。
您最近一年使用:0次
8 . 硫化钠是用于皮革鞣制的重要化学试剂,可用无水芒硝(Na2SO4)与炭粉在高温下反应而制得,反应方程式如下:Na2SO4+4C →Na2S+ 4CO,Na2SO4+4CO→Na2S+4CO2
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S_____ g,最多生成标况下的CO_____ L。
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是____ mol≤n≤___ mol,若生成等物质的量CO和CO2,则消耗的碳的物质的量为____ mol。
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。_____
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。
您最近一年使用:0次
9 . 绿矾(FeSO4·7H2O)在化学合成上用作还原剂及催化剂。工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾。
(1)98% 1.84g/cm3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4g/cm3,50%的硫酸物质的量浓度为________ (保留两位小数),50%的硫酸与30%的硫酸等体积混合,混合酸的浓度为_______ (填>、<、=)40%。
(2)将111.2g绿矾(FeSO4∙7H2O,式量为278)在高温下加热,充分反应后生成Fe2O3固体和SO2、SO3、水的混合气体,则生成Fe2O3的质量为_______ g;SO2为_______ mol。实验室可用以下方法制备摩尔盐晶体[(NH4)2SO4·FeSO4·6H2O,式量为392]。
(3)将4.88g铁屑(含Fe2O3)与25mL 3mol/L H2SO4充分反应后,得到FeSO4和H2SO4的混合溶液,稀释溶液至100mL,测得其pH=1。铁屑中Fe2O3的质量分数是________ (保留两位小数)。
(4)向上述100mL溶液中加入与该溶液中FeSO4等物质的量的(NH4)2SO4晶体,待晶体完全溶解后蒸发掉部分水,冷却至t℃,析出摩尔盐晶体12.360g,剩余溶液的质量为82.560g。t℃时,计算(NH4)2SO4·FeSO4·6H2O的溶解度。_______ (保留两位小数)。
(1)98% 1.84g/cm3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4g/cm3,50%的硫酸物质的量浓度为
(2)将111.2g绿矾(FeSO4∙7H2O,式量为278)在高温下加热,充分反应后生成Fe2O3固体和SO2、SO3、水的混合气体,则生成Fe2O3的质量为
(3)将4.88g铁屑(含Fe2O3)与25mL 3mol/L H2SO4充分反应后,得到FeSO4和H2SO4的混合溶液,稀释溶液至100mL,测得其pH=1。铁屑中Fe2O3的质量分数是
(4)向上述100mL溶液中加入与该溶液中FeSO4等物质的量的(NH4)2SO4晶体,待晶体完全溶解后蒸发掉部分水,冷却至t℃,析出摩尔盐晶体12.360g,剩余溶液的质量为82.560g。t℃时,计算(NH4)2SO4·FeSO4·6H2O的溶解度。
您最近一年使用:0次
2019-10-26更新
|
482次组卷
|
5卷引用:上海市长宁、嘉定区2015届高三第二次质量调研(二模)化学试题
上海市长宁、嘉定区2015届高三第二次质量调研(二模)化学试题上海市2016届高考化学模拟试卷(压轴卷)(已下线)第02讲 物质的量浓度(练)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第二章 物质的量化学实验基本技能 第6练 物质的量(已下线)第2讲 物质的浓度及溶液配制
10 . (1)常温下,2L pH=12的Ba(OH)2溶液的物质的量浓度为________ ,从中取出10mL加水稀释到100mL,pH=______ 。
(2)已知500mLAl2(SO4)3溶液中含有Al3+为0.5mol,则Al2(SO4)3溶液的物质的量浓度为____ mol/L,取上述溶液50mL加水到150mL,此溶液中SO42-的物质的量浓度为_____ mol/L。
(2)已知500mLAl2(SO4)3溶液中含有Al3+为0.5mol,则Al2(SO4)3溶液的物质的量浓度为
您最近一年使用:0次



