名校
1 . 已知酸性KMnO4溶液可与FeSO4反应生成Fe3+和Mn2+。现将硫酸酸化的KMnO4溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是
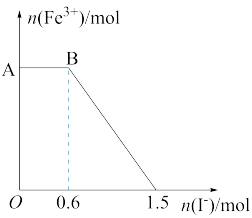

| A.图中AB段的氧化剂为KMnO4 |
| B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C.KMnO4与FeSO4反应的物质的量之比为1∶6 |
| D.开始加入的KMnO4为0.3 mol |
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式正确的是
A.1 mol·L-1的NaAlO2溶液和2.5 mol·L-1的HCl溶液等体积互相均匀混合:2 +5H+=Al3++Al(OH)3↓+H2O +5H+=Al3++Al(OH)3↓+H2O |
B.Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++ +OH-=MgCO3↓+H2O +OH-=MgCO3↓+H2O |
| C.向次氯酸钙溶液中通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| D.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
您最近一年使用:0次
3 . 下列实验中,所采取的分离方法与对应原理都正确的是
| 选项 | 目的 | 分离方法 | 原理 |
| A | 分离氢氧化铁胶体与FeCl3溶液 | 过滤 | 胶体粒子不能通过滤纸 |
| B | 除去KNO3固体中混有的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
| C | 用MgCl2溶液制备无水MgCl2固体 | 蒸发 | MgCl2受热不分解 |
| D | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . NA代表阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,124 g P4中所含P—P键数目为4NA |
| B.100 mL 1 mol·L-1FeCl3溶液中所含Fe3+的数目为0.1NA |
| C.标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA |
| D.用电解粗铜的方法精炼铜,当电路中通过的电子数为NA时,阳极应有32 g Cu转化为Cu2+ |
您最近一年使用:0次
名校
5 . NaH是有机合成中用途很广泛的物质。已知NaH遇水蒸气剧烈反应,某小组设计如图实验装置制备NaH,下列说法错误的是


| A.安全漏斗的作用是“液封” |
| B.装置A中的试剂是稀硫酸和粗锌 |
| C.装置B中的试剂是浓硫酸 |
| D.实验开始后先点燃C处酒精灯,再启动A中反应 |
您最近一年使用:0次
2022-12-10更新
|
229次组卷
|
3卷引用:河南省许昌市高级中学2022-2023学年高三上学期第二次模拟考试化学试题
名校
解题方法
6 . 下列实验操作能达到实验目的的是
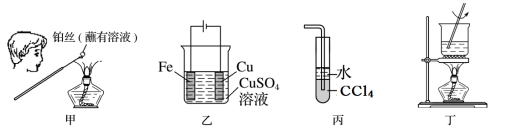

| A.用装置甲检验溶液中是否有K+ | B.用装置乙在铁上镀铜 |
| C.用装置丙吸收氨气,并防止倒吸 | D.用装置丁将FeCl3溶液蒸干制备FeCl3 |
您最近一年使用:0次
解题方法
7 . 已知:①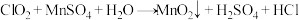
②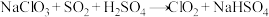
③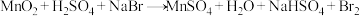
下列说法正确的是
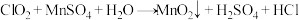
②
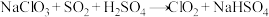
③
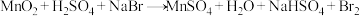
下列说法正确的是
A.氧化性: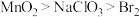 |
| B.反应①②中含氯的物质均被还原 |
C. 溶液与 溶液与 溶液不能发生反应 溶液不能发生反应 |
D.反应②③中转移等物质的量的电子时,消耗 的物质的量相等 的物质的量相等 |
您最近一年使用:0次
8 . FTO导电玻璃为掺杂氟的SnO2透明导电玻璃,广泛用于液晶显示屏、薄膜太阳能电池基底等方面,SnCl4可用于制作FTO导电玻璃。实验室可用熔融的锡与Cl2反应制备SnCl4,此反应放热,生成的SnCl4易水解生成SnO2·xH2O。回答下列问题:

有关物理性质如下表:
(1)II装置中发生反应的离子方程式为_______ 。
(2)将上述装置用玻璃管连接,组装成一套制备SnCl4的实验装置(每个装置最多使用一次),正确的顺序是(填各接口字母序号):B_______ N,A_______ 。
(3)检查装置气密性并装好药品后,应先打开II中的分液漏斗活塞,待出现______ 现象后,再点燃I处的酒精灯。
(4)VI 装置的作用是_______ 。若没有VI装置,可能发生的化学反应方程式为_______ 。
(5)实验制得30g溶有氯气的SnCl4,其中氯气质量分数为13.0%,则需向I中通入氯气的物质的量为_______ mol(保留2位小数)。提纯该SnCl4的方法是_______ 。
a.用NaOH溶液洗涤再蒸馏 b.升华 c.重结晶 d.蒸馏 e.过滤

有关物理性质如下表:
| 物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
| Sn | 银白色固体 | 231.9 | 2 260 |
| SnCl4 | 无色液体 | -33 | 114 |
| SnCl2 | 无色晶体 | 246 | 652 |
(2)将上述装置用玻璃管连接,组装成一套制备SnCl4的实验装置(每个装置最多使用一次),正确的顺序是(填各接口字母序号):B
(3)检查装置气密性并装好药品后,应先打开II中的分液漏斗活塞,待出现
(4)VI 装置的作用是
(5)实验制得30g溶有氯气的SnCl4,其中氯气质量分数为13.0%,则需向I中通入氯气的物质的量为
a.用NaOH溶液洗涤再蒸馏 b.升华 c.重结晶 d.蒸馏 e.过滤
您最近一年使用:0次
名校
9 . 草酸亚铁晶体(FeC2O4·2H2O)可作为制备电池正极材料磷酸铁锂的原料。以FeSO4溶液制备电池级草酸亚铁晶体的实验流程如下:

(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是_______ 。
(2)“转化”在如图所示的装置中进行。导管A的作用是_______ 。

(3)检验“洗涤”完全的实验操作是_______ 。
(4)测定草酸亚铁样品纯度的方法如下:准确称取0.250 0 g样品,加入适量水、浓H2SO4、磷酸,用0.045 00 mol·L-1 KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00 mL。计算样品中FeC2O4·2H2O的纯度为_______ (保留三位有效数字)。

(1)“沉淀”步骤得到的混合体系不宜在空气中久置,其原因是
(2)“转化”在如图所示的装置中进行。导管A的作用是

(3)检验“洗涤”完全的实验操作是
(4)测定草酸亚铁样品纯度的方法如下:准确称取0.250 0 g样品,加入适量水、浓H2SO4、磷酸,用0.045 00 mol·L-1 KMnO4标准溶液滴定至终点(草酸亚铁转化为Fe3+和CO2),消耗KMnO4标准溶液18.00 mL。计算样品中FeC2O4·2H2O的纯度为
您最近一年使用:0次
名校
10 . 氧化铜和氧化亚铁的混合物a g,加入2 mol·L-1的硫酸溶液50 mL,恰好完全溶解,若将a g的该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为
| A.1.6a g | B.(a-1.6) g |
| C.(a-3.2) g | D.无法计算 |
您最近一年使用:0次



