解题方法
1 . 下列实验能达到目的的是
| 选项 | 实验目的 | 实验方法或操作 |
| A | 制备NO气体 | 将铜丝插入浓硝酸中 |
| B | 探究浓度对化学反应速率的影响 | 取等体积不同浓度的NaClO溶液,分别加入等体积等浓度的 溶液,对比现象 溶液,对比现象 |
| C | 检验某盐溶液中是否含有 | 向溶液中加入NaOH溶液并加热,观察产生的气体能否使湿润的红色石蕊试纸变蓝 |
| D | 检验淀粉是否发生水解 | 向淀粉水解液中加入碘水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列装置和操作能达到实验目的的是
| A | B | C | D |
 |  | 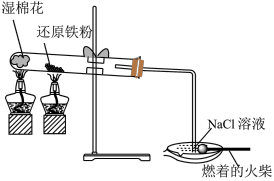 |  |
| 测定醋酸的浓度 | 观察甲烷与氯气反应的现象 | 验证铁与水蒸气反应产生 | 向铁电极区附近溶液中滴入2滴铁氰化钾溶液,验证铁电极受到了保护 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 较活泼金属与硝酸反应,产物复杂。如一定浓度的硝酸与镁反应,可同时得到 、
、 、
、 三种气体。某同学欲用下列仪器组装装置来直接验证有
三种气体。某同学欲用下列仪器组装装置来直接验证有 、
、 生成并制取氮化镁。(假设实验中每步转化均是完全的)
生成并制取氮化镁。(假设实验中每步转化均是完全的)
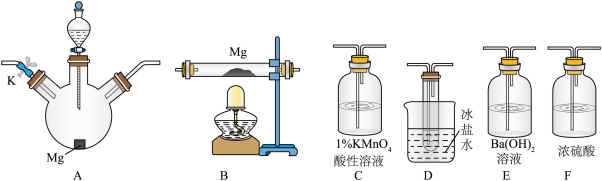
已知:① 沸点是21.1℃、熔点是
沸点是21.1℃、熔点是 ℃;
℃; 的沸点是
的沸点是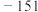 ℃、熔点是
℃、熔点是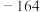 ℃;
℃;
②氮化镁遇水会发生水解。
回答下列问题:
(1)为达到上述实验目的,所选用的仪器的正确连接方式是_________ (填序号)
a.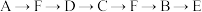 b.
b.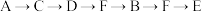
c.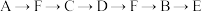 d.
d.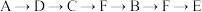
(2)实验中两次使用装置 ,第二次使用装置
,第二次使用装置 的作用是
的作用是_________ 。
(3)实验前需先打开开关 ,向装置内通
,向装置内通 气体,其目的是
气体,其目的是_________ ,当_________ 时停止通入 。
。
(4)实验过程中,发现在 中产生预期现象的同时,
中产生预期现象的同时, 中溶液颜色慢慢褪去,试写出
中溶液颜色慢慢褪去,试写出 中反应的离子方程式
中反应的离子方程式_________ 。
 、
、 、
、 三种气体。某同学欲用下列仪器组装装置来直接验证有
三种气体。某同学欲用下列仪器组装装置来直接验证有 、
、 生成并制取氮化镁。(假设实验中每步转化均是完全的)
生成并制取氮化镁。(假设实验中每步转化均是完全的)
已知:①
 沸点是21.1℃、熔点是
沸点是21.1℃、熔点是 ℃;
℃; 的沸点是
的沸点是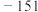 ℃、熔点是
℃、熔点是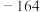 ℃;
℃;②氮化镁遇水会发生水解。
回答下列问题:
(1)为达到上述实验目的,所选用的仪器的正确连接方式是
a.
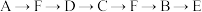 b.
b.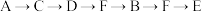
c.
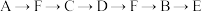 d.
d.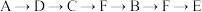
(2)实验中两次使用装置
 ,第二次使用装置
,第二次使用装置 的作用是
的作用是(3)实验前需先打开开关
 ,向装置内通
,向装置内通 气体,其目的是
气体,其目的是 。
。(4)实验过程中,发现在
 中产生预期现象的同时,
中产生预期现象的同时, 中溶液颜色慢慢褪去,试写出
中溶液颜色慢慢褪去,试写出 中反应的离子方程式
中反应的离子方程式
您最近一年使用:0次
4 . 下列实验设计能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 探究浓度对化学反应速率的影响 | 常温常压下,向一试管中加入10%的 溶液,另一试管中加入 溶液,另一试管中加入 固体和5%的 固体和5%的 溶液,观察现象 溶液,观察现象 |
| B | 制备并得到纯净的溴苯 | 向含溴的苯溶液中加入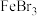 溶液,充分反应后,过滤洗涤 溶液,充分反应后,过滤洗涤 |
| C | 证明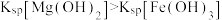 | 向  NaOH溶液中滴加2滴同浓度的 NaOH溶液中滴加2滴同浓度的 溶液后,再滴加2滴同浓度的 溶液后,再滴加2滴同浓度的 溶液,观察现象 溶液,观察现象 |
| D | 验证某溶液中一定含有钾元素 | 用洁净的铁丝蘸取该溶液在酒精灯外焰上灼烧,透过蓝色钴玻璃观察,火焰呈紫色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-16更新
|
135次组卷
|
2卷引用:海南省琼海市2023届高三联考二模化学试题
5 . 利用如图所示装置进行实验,可以达到实验目的的是
 | 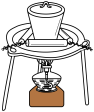 | 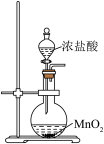 | 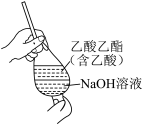 |
| A.铁上镀铜 | B.加热金属钠观察钠燃烧的现象 | C.制取 | D.提纯乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 根据实验目的,下列实验方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 实验方案设计 | 现象和结论 |
| A | 制备Fe(OH)3胶体 | 向5 mL NaOH溶液中滴加2滴FeCl3饱和溶液,煮沸 | 溶液变红褐色;说明有Fe(OH)3胶体生成 |
| B | 验证铁的电化学腐蚀 | 在一 块除去铁锈的铁片上面滴1滴含有酚酞的食盐水,静置2~3 min | 溶液边缘 出现红色;说明铁发生了吸氧腐蚀 |
| C | 探究SO2的还原性 | 将SO2通入适量品红溶液中 | 溶液褪色:说明SO2具有还原性 |
| D | 比较C与Cl的非金属性强弱 | 用pH试纸测定1mol/L的Na2CO3和NaClO溶液的pH | 前者的试纸颜色比后者深; 说明非金属性Cl>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 已知:①氧化亚铜在酸性条件下能发生歧化反应: ;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
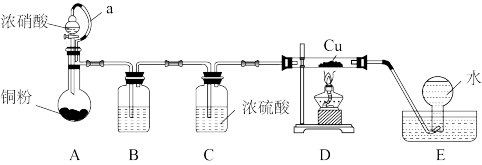
(1)①a管的作用是_______ ,②装置A中发生反应的离子方程式为_______ 。
(2)实验开始时,先打开A中分液漏斗活塞,过一会儿,点燃D处酒精灯,①这样操作的目的是_______ ,当Cu充分反应,实验结束时,②下列操作中应首先进行的是_______ (填序号)。
①停止滴加浓硝酸②熄灭酒精灯③从E装置中取出导气管
(3)为了探究氧化产物是否含有 ,取少量完全反应后的产物,进行如下实验:
,取少量完全反应后的产物,进行如下实验:
(甲)加入足量的稀硝酸,观察是否完全溶解
(乙)加入足量的稀硫酸,观察是否完全溶解
(丙)加入足量的浓硝酸,观察是否完全溶解
(丁)在加热条件下通入乙醇蒸气,观察固体是否变为红色。其中,能达到实验目的的是_______ (填代号)。
(4)查文献发现:铜与浓酸反应一旦发生就变快,是因为开始生成的 溶于水形成
溶于水形成 (弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成
(弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成 后反应变快的原因进行探究。
后反应变快的原因进行探究。
a.Ⅰ中加入的固体为_______ 。b.Ⅱ中“放置一段时间”的目的是_______ 。
实验Ⅰ、Ⅱ说明 氧化Cu的反应速率比
氧化Cu的反应速率比 氧化Cu快。
氧化Cu快。
(5)某同学将铜片放入盛有稀 的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是
的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是_______ 。
(6)若产物为CuO和 的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和
的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和 的物质的量之比为
的物质的量之比为_______ 。
 ;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
(1)①a管的作用是
(2)实验开始时,先打开A中分液漏斗活塞,过一会儿,点燃D处酒精灯,①这样操作的目的是
①停止滴加浓硝酸②熄灭酒精灯③从E装置中取出导气管
(3)为了探究氧化产物是否含有
 ,取少量完全反应后的产物,进行如下实验:
,取少量完全反应后的产物,进行如下实验:(甲)加入足量的稀硝酸,观察是否完全溶解
(乙)加入足量的稀硫酸,观察是否完全溶解
(丙)加入足量的浓硝酸,观察是否完全溶解
(丁)在加热条件下通入乙醇蒸气,观察固体是否变为红色。其中,能达到实验目的的是
(4)查文献发现:铜与浓酸反应一旦发生就变快,是因为开始生成的
 溶于水形成
溶于水形成 (弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成
(弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成 后反应变快的原因进行探究。
后反应变快的原因进行探究。| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 取B中溶液,加入一定量_______固体,再加入铜片 | 立即产生无色气体;液面上方呈红棕色 |
| Ⅱ | 取B中溶液,放置一段时间,溶液变为无色,再加入钢片 | 产生无色气体,较Ⅰ慢;液面上方呈浅红棕色 |
实验Ⅰ、Ⅱ说明
 氧化Cu的反应速率比
氧化Cu的反应速率比 氧化Cu快。
氧化Cu快。(5)某同学将铜片放入盛有稀
 的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是
的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是(6)若产物为CuO和
 的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和
的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
8 . 下列实验操作或现象正确且能达到实验目的的是
| 实验目的 | 实验操作或现象 | |
| A | 证明溶液中含有Fe2+ | 向某溶液中先滴加氯水,再滴加少量KSCN溶液,溶液变成血红色 |
| B | 除去CO2中少量的SO2 | 将混合气体通过饱和Na2CO3溶液 |
| C | 证明AgI的Ksp小于AgCl的Ksp | 向两份相同的银氨溶液中分别滴加2滴等浓度的NaCl和NaI溶液,一份中产生黄色沉淀,另一份无明显现象 |
| D | 清洗用KMnO4制备O2的试管中残留的MnO2 | 用稀盐酸清洗并用酒精灯加热试管 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-12更新
|
301次组卷
|
3卷引用:河北省唐山市第一中学2021-2022学年高三上学期期中考试化学试题
河北省唐山市第一中学2021-2022学年高三上学期期中考试化学试题(已下线)第八单元 水溶液中的离子平衡(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)河南省周口恒大中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
9 .  俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
 俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是| 选项 | 实验目的 | 实验操作或现象 | 相关离子方程式 |
| A | 制备 | 实验室用 通入 通入 和 和 的混合溶液中来制备 的混合溶液中来制备 | 4SO2+2S2-+CO =3S2O =3S2O +CO2 +CO2 |
| B | 检验硫代硫酸钠氧化变质可能混有的 | 取少量样品溶于水,先加入过量稀盐酸,再滴加 溶液,有沉淀生成 溶液,有沉淀生成 | SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C | 探究温度对硫代硫酸钠与硫酸反应速率的影响 | 分别将两种反应溶液先混合,再水浴加热至反应要求温度,测得该温度下的反应速率 | 2S2O +2H+=S↓+SO +2H+=S↓+SO +2H2O +2H2O |
| D | 用过量硫代硫酸钠除去水中溶解的氯气 | 黄绿色褪去 | S2O +4Cl2+5H2O=2SO +4Cl2+5H2O=2SO +8Cl-+10H+ +8Cl-+10H+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-11更新
|
2440次组卷
|
7卷引用:湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题
湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题(已下线)素养卷09 微型原理验证方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题04 离子反应湖南省部分学校2022-2023学年高三下学期开学考试化学试题湖南省衡阳市第八中学2023-2024学年高三上学期开学(暑假检测)化学试题江苏省靖江高级中学、华罗庚中学2023-2024学年高三上学期第一次阶段考试化学试题江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题
10 . 实验目的:为研究铁质材料与热浓硫酸的反应
(1)称取铁钉(碳素钢 ) 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。
①甲同学认为 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为___________ (选填序号)
A. 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液
②乙同学取 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为___________ 。(保留三位有效数字)。
(2)分析上述实验中 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是___________ 。

(3)装置A中试剂的作用是___________ ,反应的离子方程式___________ 。
(4)简述确认气体Y中含有 的实验现象
的实验现象___________ 。
(5)如果气体Y中含有 ,预计实验现象应是
,预计实验现象应是___________ 。
(1)称取铁钉(
 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。①甲同学认为
 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为A.
 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液②乙同学取
 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为(2)分析上述实验中
 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是
(3)装置A中试剂的作用是
(4)简述确认气体Y中含有
 的实验现象
的实验现象(5)如果气体Y中含有
 ,预计实验现象应是
,预计实验现象应是
您最近一年使用:0次
2021-10-10更新
|
285次组卷
|
5卷引用:河北省衡水市武邑武罗学校2020-2021学年高三上学期期中考试化学试题



