1 . 实验室需要0.1 mol /L氢氧化钠溶液100 mL,现有2 mol /L氢氧化钠溶液。
(1)计算所需溶质氢氧化钠的质量是多少?
(2)计算所需2 mol /L氢氧化钠溶液的体积
(1)计算所需溶质氢氧化钠的质量是多少?
(2)计算所需2 mol /L氢氧化钠溶液的体积
您最近一年使用:0次
2011-12-15更新
|
862次组卷
|
3卷引用:陕西省汉中市龙岗学校2019-2020学年高二上学期期末考试化学试题(文)
陕西省汉中市龙岗学校2019-2020学年高二上学期期末考试化学试题(文)(已下线)2011-2012学年河南省焦作市修武一中分校高一上学期期中考试化学试卷青海省西宁市海湖中学2019-2020学年高一上学期第二次阶段考试化学试题
11-12高一上·陕西咸阳·期中
2 . 用20.0g烧碱配制成500mL溶液。
(1)所得溶液溶质的物质的量浓度为_________ mol·L—1。
(2)若从上述溶液中取出10mL用水稀释到250mL,所得溶液中溶质的物质的量浓度为________ mol·L—1
(1)所得溶液溶质的物质的量浓度为
(2)若从上述溶液中取出10mL用水稀释到250mL,所得溶液中溶质的物质的量浓度为
您最近一年使用:0次
10-11高三·陕西西安·开学考试
3 . 亚氯酸钠(NaClO2)是一种重要的含氯消毒剂。以下是过氧化氢法生产亚氯酸钠的工艺流程图
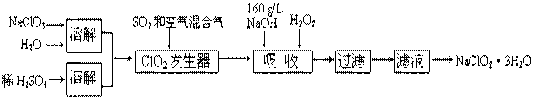
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②ClO2的沸点为283 K,纯ClO2易分解爆炸,常用稀有气体或空气稀释防止爆炸性分解
③HClO2在25 ℃时的电离常数与硫酸的第二步电离常数相当,可视为强酸。
(1)160g/L NaOH溶液的物质的量浓度为____________________ 。若要计算该溶液的质量分数,还需要的一个数据是__________________ 。
(2)ClO2发生器中所发生反应的离子方程式为__________________________
(3)吸收塔中为防止产生NaClO2被继续还原成NaCl,所用还原剂的还原性应适中。除H2O2处,还可以选择的还原剂是( ) (填序号)
A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
(4)写出吸收塔中发生反应的化学方程式____________________________
(5)从滤液中得到NaClO2·3H2O晶体还必须进行的操作是_____________ (填操作步骤)

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②ClO2的沸点为283 K,纯ClO2易分解爆炸,常用稀有气体或空气稀释防止爆炸性分解
③HClO2在25 ℃时的电离常数与硫酸的第二步电离常数相当,可视为强酸。
(1)160g/L NaOH溶液的物质的量浓度为
(2)ClO2发生器中所发生反应的离子方程式为
(3)吸收塔中为防止产生NaClO2被继续还原成NaCl,所用还原剂的还原性应适中。除H2O2处,还可以选择的还原剂是
A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
(4)写出吸收塔中发生反应的化学方程式
(5)从滤液中得到NaClO2·3H2O晶体还必须进行的操作是
您最近一年使用:0次



