真题
名校
1 . 聚合硫酸铁[Fe(OH)SO4]n能用作净水剂(絮凝剂),可由绿矾(FeSO4·7H2O)和KClO3在水溶液中反应得到。下列说法不正确 的是
| A.KClO3作氧化剂,每生成1 mol [Fe(OH)SO4]n消耗6/n mol KClO3 |
| B.生成聚合硫酸铁后,水溶液的pH增大 |
| C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水 |
| D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强 |
您最近一年使用:0次
2019-04-12更新
|
5923次组卷
|
36卷引用:2019年4月浙江省普通高校招生选考科目考试化学试题
2019年4月浙江省普通高校招生选考科目考试化学试题福建省华安一中2018-2019学年高二下学期期末考试化学试题湖南省长沙市第一中学2020届高三第一次月考化学试题江西省宜春市奉新县第一中学2020届高三上学期第二次月考化学试题黑龙江省牡丹江市第一高级中学2020届高三10月月考化学试题河北省邯郸市2019-2020学年高三上学期期中考试化学试题2020届高考化学小题狂练(全国通用版)专练5 氧化还原反应辽宁省抚顺市第一中学2020届高三上学期期中考试化学试题江西省吉安市五校2019-2020学年高二上学期第二次联考化学试题2020届高三化学化学二轮复习——高考常考题:氧化还原反应的实际应用【精编选择25题】专题1.3 氧化还原反应(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)广东省佛山市第一中学2020-2021学年高二上学期期中考试化学(选考)试题安徽省池州市第一中学2020-2021学年高二12月月考化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练上海交通大学附属中学2021届高三下学期3月月考化学试题(已下线)课时17 铁及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)3.3.1 盐类的水解-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题05.元素及其化合物-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)湖南省长沙市雅礼中学2022-2023学年高三上学期第五次月考化学试题第三章 金属及其化合物 第13讲 铁及其重要化合物湖南省株洲市第四中学2023届高三第六次月考化学试题(已下线)题型27 铁及其化合物的性质、用途及相关计算重庆市万州第二高级中学2022-2023学年高三下学期5月月考化学试题新疆喀什地区伽师县2022-2023学年高三上学期11月期中考试化学试题(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)北京市第八十中学2024届高三上学期10月月考化学试题化学江苏省扬州市宝应区2023-2024学年曹甸高级中学高三上学期9月化学试卷
2 . 四氧化三锰是一种重要的电子和新能源基础原材料,可以用于生产软磁锰锌铁氧体、锂电正极材料锰酸锂和负温度系数热敏电阻等。以软锰矿(主要成分为 还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分
还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分 )为原料制备大颗粒的电池
)为原料制备大颗粒的电池 。
。
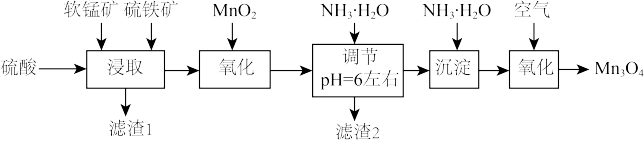
说明:
Ⅰ.“浸取”:研究发现,酸浸时 和
和 颗粒反应的原理如图1所示(部分产物未标出)。
颗粒反应的原理如图1所示(部分产物未标出)。
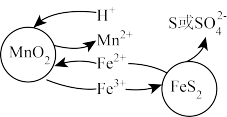
图1
Ⅱ.通空气“氧化”:将“沉淀”步骤所得含少量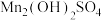 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得 。
。
Ⅲ.氢氧化物形式完全沉淀时溶液的pH见表:
(1)滤渣1中主要成分的化学式为_______ 。
(2)随硫铁矿的增加,锰的浸出率降低,可能的原因是_______ 。
(3)写出“浸取”时 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
(4)加入 “氧化”的目的是
“氧化”的目的是_______ 。
(5)检验“沉淀”已洗净的操作是_______ 。
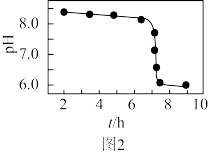
(6)“沉淀”加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是_______ 。
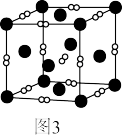
(7)一个立方体结构的 晶胞如图3所示,距离
晶胞如图3所示,距离 最近的
最近的 有
有_______ 个,已知阿伏加德罗数值为 ,则
,则 的晶体密度为
的晶体密度为 ,则晶胞的边长为
,则晶胞的边长为_______ nm(用含ρ、 的代数式表示)。
的代数式表示)。
 还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分
还含少量Fe、Si、Al等的氧化物)和硫铁矿(主要成分 )为原料制备大颗粒的电池
)为原料制备大颗粒的电池 。
。
说明:
Ⅰ.“浸取”:研究发现,酸浸时
 和
和 颗粒反应的原理如图1所示(部分产物未标出)。
颗粒反应的原理如图1所示(部分产物未标出)。
图1
Ⅱ.通空气“氧化”:将“沉淀”步骤所得含少量
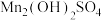 的
的 固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得
固体滤出,洗净,加水打成浆,浆液边加热边持续通入空气,制得 。
。Ⅲ.氢氧化物形式完全沉淀时溶液的pH见表:
| 沉淀物 |  |  |  |  |
| 开始沉淀的pH | 3.4 | 2.2 | 6.3 | 8.1 |
| 完全沉淀的pH | 5.2 | 3.2 | 9.7 | 10.4 |
(2)随硫铁矿的增加,锰的浸出率降低,可能的原因是
(3)写出“浸取”时
 与
与 反应的离子方程式为
反应的离子方程式为(4)加入
 “氧化”的目的是
“氧化”的目的是(5)检验“沉淀”已洗净的操作是
(6)“沉淀”加热通空气过程中溶液pH随时间变化如图2所示,其中pH先基本不变后迅速下降的原因是

(7)一个立方体结构的
 晶胞如图3所示,距离
晶胞如图3所示,距离 最近的
最近的 有
有 ,则
,则 的晶体密度为
的晶体密度为 ,则晶胞的边长为
,则晶胞的边长为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
3 . “84消毒液”广泛应用于杀菌消毒,其有效成分是 。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
资料:i. 的电离常数为
的电离常数为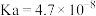 ;
; 的电离常数为
的电离常数为 、
、
ii.碘的化合物主要以 和
和 的形式存在,
的形式存在, 。
。
iii.碘单质能与 反应:
反应: (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。
I.制备消毒液(夹持装置略)

(1)制备 的离子反应方程式
的离子反应方程式_______ 。
(2)结合资料i,写出D中反应的化学方程式_______ 。
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
(3)针对烧杯3“滴加淀粉溶液不变蓝”的原因,提出两种假设:
假设1:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设1成立,实验a的操作及现象是_______ 。
假设2:过量的 将反应生成的
将反应生成的 氧化为
氧化为 。
。
设计实验b证实了假设2成立。 氧化
氧化 生成
生成 的离子方程式是
的离子方程式是_______ 。
(4)某小组检验烧杯3所得溶液中含 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的 溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由_______ 。
(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据_______ 。
(6)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是_______ 。
 。实验小组制备消毒液,并利用其性质探究制备碘水的方法。
。实验小组制备消毒液,并利用其性质探究制备碘水的方法。资料:i.
 的电离常数为
的电离常数为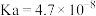 ;
; 的电离常数为
的电离常数为 、
、
ii.碘的化合物主要以
 和
和 的形式存在,
的形式存在, 。
。iii.碘单质能与
 反应:
反应: (
( 低浓度时显黄色,高浓度时为棕色)。
低浓度时显黄色,高浓度时为棕色)。I.制备消毒液(夹持装置略)

(1)制备
 的离子反应方程式
的离子反应方程式(2)结合资料i,写出D中反应的化学方程式
II.利用消毒液的性质探究碘水的制备方法
将某品牌“84消毒液”稀释10倍,各取100mL于三个烧杯中,设计如下实验方案制备碘水:
| 方案 | 操作 | 现象 | 反应后加淀粉溶液 |
| 1 | 烧杯1溶液中加入9g 固体 固体 | 溶液为橙黄色 | …… |
| 2 | 烧杯2溶液中加入9g 固体,再加入1 固体,再加入1 盐酸10mL 盐酸10mL | 溶液颜色快速加深,呈紫红色 | 变蓝 |
| 3 | 烧杯3溶液中加入少量 固体(小于0.5g) 固体(小于0.5g) | 振荡后溶液保持无色 | 不变蓝 |
假设1:生成的I2在碱性溶液中不能存在。
设计实验a证实了假设1成立,实验a的操作及现象是
假设2:过量的
 将反应生成的
将反应生成的 氧化为
氧化为 。
。设计实验b证实了假设2成立。
 氧化
氧化 生成
生成 的离子方程式是
的离子方程式是(4)某小组检验烧杯3所得溶液中含
 :取烧杯3所得无色溶液少许,加入稀硫酸酸化的
:取烧杯3所得无色溶液少许,加入稀硫酸酸化的 溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在
溶液,反应后再滴加淀粉溶液,发现溶液变蓝。该实验方案能否证明烧杯3所得溶液中存在 ,说明理由
,说明理由(5)预测烧杯1反应后加淀粉溶液的实验现象,结合方程式说明预测依据
(6)对比不同方案的实验现象,得出制取碘水的最佳方法要关注的因素是
您最近一年使用:0次
2022-12-30更新
|
1184次组卷
|
4卷引用:河北省邯郸市第一中学2022-2023学年高三上学期一轮复习(四)化学试题
4 . Fe3O4是一种重要的化工产品,以黄铁矿烧渣(主要含Fe2O3、Fe3O4、CaO等物质)为原料制备Fe3O4的过程如下。
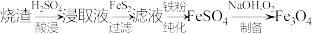
(1)酸浸、过滤
① 酸浸过程Fe3O4发生反应的离子方程式是________ 。
② 充分酸浸后浸取液中仍有Ca2+ 残留,加入FeS2可进一步提高钙的脱除率,结合方程式解释原因________ 。
(2)纯化
① Fe粉的作用是________ 。
② 检验纯化是否完全还原,应向滤液中加入________ 。
a.KMnO4溶液 b.K3[Fe(CN)6]溶液 c.KSCN溶液
(3)制备
将NaOH溶液与FeSO4溶液(稍过量)按一定比例混合,产生白色沉淀,继而转变为墨绿色,最后变为黑色。溶液混合的同时通入空气并记录pH的变化,如图所示。
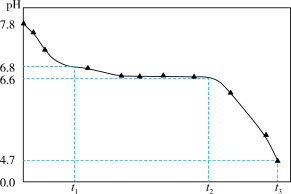
已知:
ⅰ.pH≈7.8时,浊液中主要存在Fe(OH)+、 Fe(OH)2和少量Fe2+
ⅱ.墨绿色物质主要成分为Fe5O2(OH)5SO4
制备过程可能发生了如下历程:
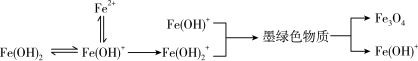
① 0~t1时段,pH明显降低。结合离子方程式解释原因:________ 。
② t1~t2时段,墨绿色物质的生成与转化(生成Fe3O4)同时进行。
a.生成墨绿色物质的方程式是:________ 。
b.墨绿色物质转化为Fe3O4的方程式是:________ 。
③ t2~t3时段,pH继续降低的原因是:________ 。
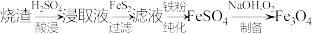
(1)酸浸、过滤
① 酸浸过程Fe3O4发生反应的离子方程式是
② 充分酸浸后浸取液中仍有Ca2+ 残留,加入FeS2可进一步提高钙的脱除率,结合方程式解释原因
(2)纯化
① Fe粉的作用是
② 检验纯化是否完全还原,应向滤液中加入
a.KMnO4溶液 b.K3[Fe(CN)6]溶液 c.KSCN溶液
(3)制备
将NaOH溶液与FeSO4溶液(稍过量)按一定比例混合,产生白色沉淀,继而转变为墨绿色,最后变为黑色。溶液混合的同时通入空气并记录pH的变化,如图所示。

已知:
ⅰ.pH≈7.8时,浊液中主要存在Fe(OH)+、 Fe(OH)2和少量Fe2+
ⅱ.墨绿色物质主要成分为Fe5O2(OH)5SO4
制备过程可能发生了如下历程:
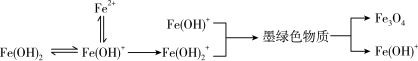
① 0~t1时段,pH明显降低。结合离子方程式解释原因:
② t1~t2时段,墨绿色物质的生成与转化(生成Fe3O4)同时进行。
a.生成墨绿色物质的方程式是:
b.墨绿色物质转化为Fe3O4的方程式是:
③ t2~t3时段,pH继续降低的原因是:
您最近一年使用:0次
解题方法
5 . 碲(Te)广泛应用于冶金、航空航天、电子等领域。从精炼钢的阳极泥中(主要成分为Cu2Te,还含有金、银、铂等)回收碲的工艺流程如下:
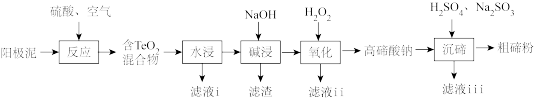
已知:TeO2有强还原性,且TeO2、Cu2TeO4难溶于水;高碲酸钠的化学式:Na2TeO4
回答下列问题:
(1)为提高“反应”效率,可采取的措施为_______ (任答一条)。
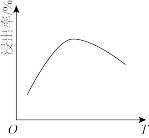
(2)滤液i的主要成分是_______ (写化学式)。滤液i中溶质的浸出率与温度关系如图所示,解释铜的浸出率随温度变化的可能原因_______ 。
(3)“氧化”过程中发生反应的离子方程式为_______ 。滤液ii可循环使用,应将其导入到_______ (写操作单元名称)操作中。
(4)“沉碲”过程中发生反应的离子方程式为_______ 。
(5)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为_______ 。

已知:TeO2有强还原性,且TeO2、Cu2TeO4难溶于水;高碲酸钠的化学式:Na2TeO4
回答下列问题:
(1)为提高“反应”效率,可采取的措施为
(2)滤液i的主要成分是

(3)“氧化”过程中发生反应的离子方程式为
(4)“沉碲”过程中发生反应的离子方程式为
(5)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为
您最近一年使用:0次
名校
6 . 某小组同学制备碘酸盐( )并探究其性质。
)并探究其性质。
资料:① 可与
可与 溶液反应生成
溶液反应生成 和
和 。
。
②碘酸钙 [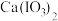 ]为难溶于水、能溶于硝酸的白色固体。
]为难溶于水、能溶于硝酸的白色固体。
③ 的氧化性,
的氧化性, 的还原性与溶液的酸碱性无关:
的还原性与溶液的酸碱性无关: 与氧化性随溶液酸性增强而增强(X为
与氧化性随溶液酸性增强而增强(X为 、
、 或I)。
或I)。
实验装置如图(加热与夹持装置略)
I.打开A中分液漏斗活塞,加热圆底烧瓶;一段时间后,B中溶液由无色变为棕黄色。
II.将B中棕黄色溶液倒入烧杯中,再加入 溶液,烧杯中溶液由棕黄色变为无色。
溶液,烧杯中溶液由棕黄色变为无色。
(1)A装置发生的化学方程式为___________ 。
(2)C装置发生的离子方程式为___________ 。
(3)取少量步骤Ⅱ后所得无色溶液,加入过量盐酸和 ,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色。甲同学得出结论:在酸性条件下
,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色。甲同学得出结论:在酸性条件下 可以氧化
可以氧化 为
为 。
。
①乙同学认为上述结论不合理,可能原因如下:
原因一:空气中 在酸性条件下将溶液中的
在酸性条件下将溶液中的 氧化,离子方程式为
氧化,离子方程式为___________ 。
原因二:___________ (填化学式)在酸性条件下将溶液中的 氧化。
氧化。
②为了进一步证明在酸性条件下 可氧化
可氧化 为
为 ,完成如下实验:
,完成如下实验:
ⅰ.另取与(3)等量的步骤Ⅱ后所得无色溶液,加入稍过量 固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y。
固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y。
ⅱ.向无色溶液X,加入与(3)等量的盐酸和 ,振荡后静置,溶液分层,上、下层均几乎无色。
,振荡后静置,溶液分层,上、下层均几乎无色。
ⅲ.取少量洗涤后的沉淀Y加入稀 ,固体溶解,继续加入少量KI溶液,溶液呈黄色。
,固体溶解,继续加入少量KI溶液,溶液呈黄色。
ⅳ.……
a.由实验ⅰ、ⅱ得出结论:___________ 。
b.由实验ⅲ和ⅳ得出结论:在酸性条件下 可以氧化
可以氧化 为
为 。补全实验ⅳ的操作和现象
。补全实验ⅳ的操作和现象___________ 。
(4)根据实验ⅲ得出:氧化性
___________  (填“
(填“ ”或“
”或“ ”),而实验ⅰ表明
”),而实验ⅰ表明 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
(5)查阅资料发现,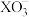 与相应的
与相应的 (
( ,
, )均有类似上述反应。浓度相同时,氧化性
)均有类似上述反应。浓度相同时,氧化性 ,但浓度均为
,但浓度均为 的
的 和
和 开始发生反应时的pH为1,而浓度均为
开始发生反应时的pH为1,而浓度均为 的
的 和
和 开始发生反应的pH为5。试从原子结构的角度解释两个反应开始发生时pH不同的原因
开始发生反应的pH为5。试从原子结构的角度解释两个反应开始发生时pH不同的原因___________ 。
 )并探究其性质。
)并探究其性质。资料:①
 可与
可与 溶液反应生成
溶液反应生成 和
和 。
。②碘酸钙 [
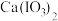 ]为难溶于水、能溶于硝酸的白色固体。
]为难溶于水、能溶于硝酸的白色固体。③
 的氧化性,
的氧化性, 的还原性与溶液的酸碱性无关:
的还原性与溶液的酸碱性无关: 与氧化性随溶液酸性增强而增强(X为
与氧化性随溶液酸性增强而增强(X为 、
、 或I)。
或I)。实验装置如图(加热与夹持装置略)
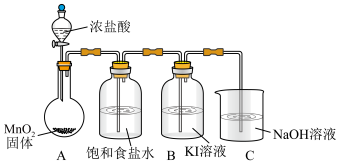
I.打开A中分液漏斗活塞,加热圆底烧瓶;一段时间后,B中溶液由无色变为棕黄色。
II.将B中棕黄色溶液倒入烧杯中,再加入
 溶液,烧杯中溶液由棕黄色变为无色。
溶液,烧杯中溶液由棕黄色变为无色。(1)A装置发生的化学方程式为
(2)C装置发生的离子方程式为
(3)取少量步骤Ⅱ后所得无色溶液,加入过量盐酸和
 ,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色。甲同学得出结论:在酸性条件下
,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色。甲同学得出结论:在酸性条件下 可以氧化
可以氧化 为
为 。
。①乙同学认为上述结论不合理,可能原因如下:
原因一:空气中
 在酸性条件下将溶液中的
在酸性条件下将溶液中的 氧化,离子方程式为
氧化,离子方程式为原因二:
 氧化。
氧化。②为了进一步证明在酸性条件下
 可氧化
可氧化 为
为 ,完成如下实验:
,完成如下实验:ⅰ.另取与(3)等量的步骤Ⅱ后所得无色溶液,加入稍过量
 固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y。
固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y。ⅱ.向无色溶液X,加入与(3)等量的盐酸和
 ,振荡后静置,溶液分层,上、下层均几乎无色。
,振荡后静置,溶液分层,上、下层均几乎无色。ⅲ.取少量洗涤后的沉淀Y加入稀
 ,固体溶解,继续加入少量KI溶液,溶液呈黄色。
,固体溶解,继续加入少量KI溶液,溶液呈黄色。ⅳ.……
a.由实验ⅰ、ⅱ得出结论:
b.由实验ⅲ和ⅳ得出结论:在酸性条件下
 可以氧化
可以氧化 为
为 。补全实验ⅳ的操作和现象
。补全实验ⅳ的操作和现象(4)根据实验ⅲ得出:氧化性

 (填“
(填“ ”或“
”或“ ”),而实验ⅰ表明
”),而实验ⅰ表明 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是(5)查阅资料发现,
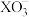 与相应的
与相应的 (
( ,
, )均有类似上述反应。浓度相同时,氧化性
)均有类似上述反应。浓度相同时,氧化性 ,但浓度均为
,但浓度均为 的
的 和
和 开始发生反应时的pH为1,而浓度均为
开始发生反应时的pH为1,而浓度均为 的
的 和
和 开始发生反应的pH为5。试从原子结构的角度解释两个反应开始发生时pH不同的原因
开始发生反应的pH为5。试从原子结构的角度解释两个反应开始发生时pH不同的原因
您最近一年使用:0次
2023-05-01更新
|
853次组卷
|
3卷引用:北京市北京师范大学附属实验中学2022-2023学年高一下学期期中考试化学试题
名校
7 . 绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了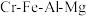 的深度利用和
的深度利用和 内循环。工艺流程如图:
内循环。工艺流程如图:

回答下列问题:
(1)高温连续氧化工序中主要反应的化学方程式为___________ 。
(2)滤渣I的主要成分是___________ (填化学式)。
(3)工序③中发生反应的离子方程式为___________ 。
(4)热解工序产生的混合气体最适宜返回工序___________ (填“①”或“②”或“③”或“④”)参与内循环。
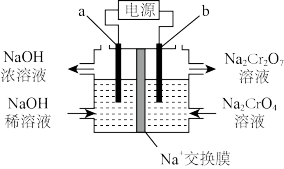
(5)工序③也可以利用电解法制 ,工作原理如下图所示(a,b电极均为石墨):b与电源的
,工作原理如下图所示(a,b电极均为石墨):b与电源的___________ 极相连,制备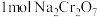 时,理论上左侧溶液总质量增重
时,理论上左侧溶液总质量增重___________ g。
(6)工序④溶液中的铝元素恰好完全转化为沉淀的 为
为___________ 。(通常认为溶液中离子浓度等于 为恰好沉淀完全;已知
为恰好沉淀完全;已知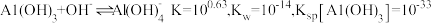 )
)
 的深度利用和
的深度利用和 内循环。工艺流程如图:
内循环。工艺流程如图:
回答下列问题:
(1)高温连续氧化工序中主要反应的化学方程式为
(2)滤渣I的主要成分是
(3)工序③中发生反应的离子方程式为
(4)热解工序产生的混合气体最适宜返回工序
(5)工序③也可以利用电解法制
 ,工作原理如下图所示(a,b电极均为石墨):b与电源的
,工作原理如下图所示(a,b电极均为石墨):b与电源的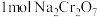 时,理论上左侧溶液总质量增重
时,理论上左侧溶液总质量增重
(6)工序④溶液中的铝元素恰好完全转化为沉淀的
 为
为 为恰好沉淀完全;已知
为恰好沉淀完全;已知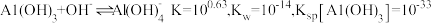 )
)
您最近一年使用:0次
解题方法
8 . 向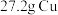 和
和 的混合物中加入某浓度的稀硝酸
的混合物中加入某浓度的稀硝酸 ,固体物质完全反应,得到标准状况下
,固体物质完全反应,得到标准状况下 和
和 的混合气体及
的混合气体及 。在所得溶液中加入
。在所得溶液中加入 的NaOH溶液
的NaOH溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列有关说法正确的是
。下列有关说法正确的是
①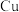 与
与 的物质的量之比为
的物质的量之比为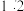
②硝酸的物质的量浓度为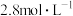
③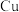 、
、 与硝酸反应后剩余
与硝酸反应后剩余 为
为
④产生的 的体积为
的体积为
⑤原混合物中Cu的质量分数为
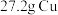 和
和 的混合物中加入某浓度的稀硝酸
的混合物中加入某浓度的稀硝酸 ,固体物质完全反应,得到标准状况下
,固体物质完全反应,得到标准状况下 和
和 的混合气体及
的混合气体及 。在所得溶液中加入
。在所得溶液中加入 的NaOH溶液
的NaOH溶液 ,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为 。下列有关说法正确的是
。下列有关说法正确的是①
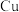 与
与 的物质的量之比为
的物质的量之比为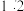
②硝酸的物质的量浓度为
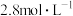
③
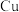 、
、 与硝酸反应后剩余
与硝酸反应后剩余 为
为
④产生的
 的体积为
的体积为
⑤原混合物中Cu的质量分数为

| A.①⑤ | B.②④ | C.①④ | D.②③ |
您最近一年使用:0次
2020-01-26更新
|
3147次组卷
|
2卷引用:2020届高三化学二轮冲刺新题专练——硝酸的性质及应用(强化练)
名校
解题方法
9 . 某钾盐X由四种元素组成,某小组按如下流程进行实验。请回答:
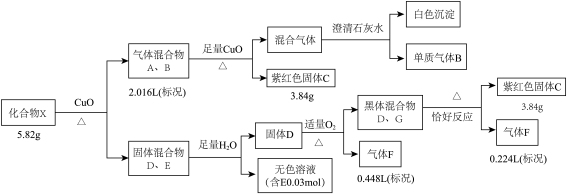
已知:相同条件下,A、B为中学常见气体且密度相同。D、E均为二元化合物,气体F能使品红溶液褪色且通入无色溶液E中,有淡黄色沉淀生成。
(1)气体B的电子式是___________ ,C的化学式是___________ 。
(2)写出固体混合物D、G共热所发生的化学反应方程式___________ 。
(3)无色溶液E中滴加盐酸观察到气泡。收集少量气体通入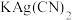 溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)
溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)___________ 。
(4)将G溶于氨水得到一无色溶液,设计实验检验无色溶液中主要离子___________ 。

已知:相同条件下,A、B为中学常见气体且密度相同。D、E均为二元化合物,气体F能使品红溶液褪色且通入无色溶液E中,有淡黄色沉淀生成。
(1)气体B的电子式是
(2)写出固体混合物D、G共热所发生的化学反应方程式
(3)无色溶液E中滴加盐酸观察到气泡。收集少量气体通入
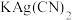 溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)
溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)(4)将G溶于氨水得到一无色溶液,设计实验检验无色溶液中主要离子
您最近一年使用:0次
2023-04-14更新
|
811次组卷
|
3卷引用:浙江省绍兴市2023届高三二模考试化学试题
10 . 下列实验能得出相关结论的是
| 实验操作 | 实验结论 | |
| A | 向NaHA溶液中滴加紫色石蕊溶液,溶液变为蓝色 | Kw>Ka1(H2A)·Ka2(H2A) |
| B | 常温下将铝片投入浓硝酸中,无明显现象 | 铝与浓硝酸不反应 |
| C | 向10mL0.1mol·L-1FeCl3溶液中加入5mL0.1mol·L-1KSCN溶液,溶液显红色,再滴加少量1mol·L-1KSCN溶液,红色加深 | Fe3+和SCN-的反应是可逆反应 |
| D | 向FeCl2溶液中滴加少量的酸性KMnO4溶液,KMnO4溶液褪色 | 氧化性: >Cl2 >Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



