解题方法
1 . 重铬酸钠 主要用于涂料、金属缓蚀剂、有机合成氧化剂等。工业上以铬铁矿(主要成分亚铬酸亚铁
主要用于涂料、金属缓蚀剂、有机合成氧化剂等。工业上以铬铁矿(主要成分亚铬酸亚铁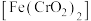 ,含少量Mg、Al、Si等杂质元素)为原料制取重铬酸钠的工艺流程如图:
,含少量Mg、Al、Si等杂质元素)为原料制取重铬酸钠的工艺流程如图:
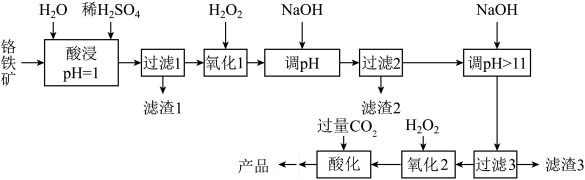
已知:① 在酸性溶液中性质稳定,当
在酸性溶液中性质稳定,当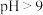 时,以
时,以 形式存在且易被氧化;
形式存在且易被氧化;
②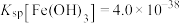 ,
,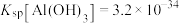 ,
,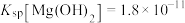 ;
;
③最高价铬酸根在碱性介质中以 存在,在酸性介质中以
存在,在酸性介质中以 存在。
存在。
回答下列问题:
(1)基态Cr原子和Fe原子中未成对电子数之比为_______ 。
(2)滤渣1的主要成分为_______ (写化学式)。
(3)“氧化1”加入足量H2O2的目的是_______ ,为防止反应过于剧烈,可采取的措施是_______ 。
(4)“调pH”至 恰好沉淀完全时滤液中
恰好沉淀完全时滤液中
_______ 。
(5)检验“滤渣3”被水洗净的试剂为_______ 。
(6)“氧化2”反应的离子方程式为_______ 。
(7)“酸化”反应的化学方程式为_______ 。
 主要用于涂料、金属缓蚀剂、有机合成氧化剂等。工业上以铬铁矿(主要成分亚铬酸亚铁
主要用于涂料、金属缓蚀剂、有机合成氧化剂等。工业上以铬铁矿(主要成分亚铬酸亚铁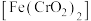 ,含少量Mg、Al、Si等杂质元素)为原料制取重铬酸钠的工艺流程如图:
,含少量Mg、Al、Si等杂质元素)为原料制取重铬酸钠的工艺流程如图:
已知:①
 在酸性溶液中性质稳定,当
在酸性溶液中性质稳定,当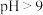 时,以
时,以 形式存在且易被氧化;
形式存在且易被氧化;②
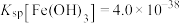 ,
,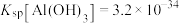 ,
,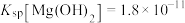 ;
;③最高价铬酸根在碱性介质中以
 存在,在酸性介质中以
存在,在酸性介质中以 存在。
存在。回答下列问题:
(1)基态Cr原子和Fe原子中未成对电子数之比为
(2)滤渣1的主要成分为
(3)“氧化1”加入足量H2O2的目的是
(4)“调pH”至
 恰好沉淀完全时滤液中
恰好沉淀完全时滤液中
(5)检验“滤渣3”被水洗净的试剂为
(6)“氧化2”反应的离子方程式为
(7)“酸化”反应的化学方程式为
您最近一年使用:0次
2 . 过碳酸钠(2 ·
·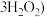 ,被称为固体双氧水,可在水中释放出活性氧而使其具有漂白和杀菌性能,是一种新型氧系漂白剂。过碳酸钠在异丙醇中的溶解度较低,实验室用
,被称为固体双氧水,可在水中释放出活性氧而使其具有漂白和杀菌性能,是一种新型氧系漂白剂。过碳酸钠在异丙醇中的溶解度较低,实验室用 和稳定剂的混合溶液与
和稳定剂的混合溶液与 化合制备,反应原理为:
化合制备,反应原理为: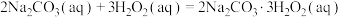
 ,装置如图所示。回答下列问题:
,装置如图所示。回答下列问题:
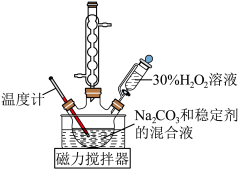
(1)盛装 溶液的仪器名称为
溶液的仪器名称为_______ 。
(2)下列可用作“稳定剂”的是_______(填字母)。
(3)实验时,应打开磁力搅拌器并缓慢加入 溶液的原因是
溶液的原因是____ ;反应结束后,停止搅拌,向反应液中加入异丙醇,静置、过滤、洗涤、干燥,获得过碳酸钠固体。加入异丙醇的目的是______ 。
(4)过碳酸钠是由 和
和 通过
通过_______ (填“化学键”、“氢键”或“分子间作用力”)形成的。过碳酸钠不稳定,在高温条件下,易发生分解,其反应方程式为_______ 。
(5)过碳酸钠活性氧含量的测定:准确称取试样2.0g于250mL锥形瓶中,加入40mL浓度为6%的硫酸溶液,水浴加热至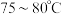 ,然后迅速用0.2000mol·
,然后迅速用0.2000mol· 的
的 溶液滴定,至
溶液滴定,至_______ 即为终点,消耗 溶液30.00mL,该样品中的活性氧含量为
溶液30.00mL,该样品中的活性氧含量为_______ (活性氧含量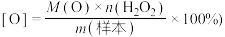 。
。
 ·
·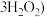 ,被称为固体双氧水,可在水中释放出活性氧而使其具有漂白和杀菌性能,是一种新型氧系漂白剂。过碳酸钠在异丙醇中的溶解度较低,实验室用
,被称为固体双氧水,可在水中释放出活性氧而使其具有漂白和杀菌性能,是一种新型氧系漂白剂。过碳酸钠在异丙醇中的溶解度较低,实验室用 和稳定剂的混合溶液与
和稳定剂的混合溶液与 化合制备,反应原理为:
化合制备,反应原理为: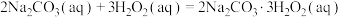
 ,装置如图所示。回答下列问题:
,装置如图所示。回答下列问题:
(1)盛装
 溶液的仪器名称为
溶液的仪器名称为(2)下列可用作“稳定剂”的是_______(填字母)。
A. | B. | C. | D. |
(3)实验时,应打开磁力搅拌器并缓慢加入
 溶液的原因是
溶液的原因是(4)过碳酸钠是由
 和
和 通过
通过(5)过碳酸钠活性氧含量的测定:准确称取试样2.0g于250mL锥形瓶中,加入40mL浓度为6%的硫酸溶液,水浴加热至
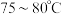 ,然后迅速用0.2000mol·
,然后迅速用0.2000mol· 的
的 溶液滴定,至
溶液滴定,至 溶液30.00mL,该样品中的活性氧含量为
溶液30.00mL,该样品中的活性氧含量为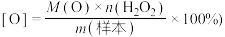 。
。
您最近一年使用:0次
解题方法
3 . Cu2O溶于浓氨水中形成无色的[Cu(NH3)2]+,该无色溶液接触空气会很快变成深蓝色。
(1)[Cu(NH3)2]+中NH3的N原子提供___________,与中心离子形成___________。
| A.空轨道、离子键 | B.孤电子对、离子键 |
| C.空轨道、配位键 | D.孤电子对、配位键 |
| A.大于107° | B.小于107° | C.等于107° | D.等于120° |
完成并配平上述离子方程式。
您最近一年使用:0次
解题方法
4 . “太阳能热化学循环制氢”是将太阳能转化成化学能,通过多个化学过程产生H2.如常见的铁氧化物循环制氢过程如图所示。

(1)写出反应Ⅰ的化学方程式:
(2)若该反应生成标准状况下5.6 L氢气,转移电子数目为:
您最近一年使用:0次
解题方法
5 . 氮及其化合物在生产、生活中广泛应用。
Ⅰ.氮元素化合价-物质类别关系图如图所示。

(1)图中A可以是__________ (写化学式)。写出一个能够生成B的化学方程式__________ 。
(2)实验室中,检验溶液中是否含有 的操作方法是
的操作方法是__________ 。
(3)水体中硝酸盐含量过高对环境不利,通过电催化法可以将水体中的硝酸盐进行合理转化。写出在中性介质中硝酸盐转化为氮气的阴极电极反应式__________ 。
Ⅱ.下图为实验室模拟尿素法制备水合肼( )的流程图:
)的流程图:
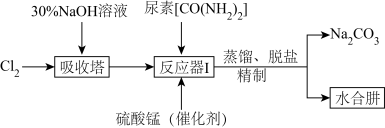
已知:① 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 。
。
②一定条件下,碱性NaClO溶液与尿素溶液反应生成 。
。
回答下列问题:
(4)“吸收塔”内发生反应的离子方程式为__________ 。
(5)写出“反应器Ⅰ”中生成水合肼反应的化学方程式为__________ 。
(6)“反应器Ⅰ”要控制NaClO溶液的用量,其主要目的是__________ 。
Ⅰ.氮元素化合价-物质类别关系图如图所示。

(1)图中A可以是
(2)实验室中,检验溶液中是否含有
 的操作方法是
的操作方法是(3)水体中硝酸盐含量过高对环境不利,通过电催化法可以将水体中的硝酸盐进行合理转化。写出在中性介质中硝酸盐转化为氮气的阴极电极反应式
Ⅱ.下图为实验室模拟尿素法制备水合肼(
 )的流程图:
)的流程图:
已知:①
 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 。
。②一定条件下,碱性NaClO溶液与尿素溶液反应生成
 。
。回答下列问题:
(4)“吸收塔”内发生反应的离子方程式为
(5)写出“反应器Ⅰ”中生成水合肼反应的化学方程式为
(6)“反应器Ⅰ”要控制NaClO溶液的用量,其主要目的是
您最近一年使用:0次
6 . 综合利用软锰矿(主要含 ,还有少量
,还有少量 、
、 、MgO、CaO、
、MgO、CaO、 )和硫铁矿(主要含
)和硫铁矿(主要含 )回收
)回收 的工艺流程如图所示:
的工艺流程如图所示:
请回答下列问题:
(1)“酸浸”时将矿石粉碎,主要目的是___________ 。
(2)浸渣1中除 和S外,还有
和S外,还有___________ (填化学式)。S是 分别与
分别与 、
、 反应产生的,其中
反应产生的,其中 与
与 反应的离子方程式为
反应的离子方程式为___________
(3)当离子浓度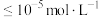 时,可视为沉淀完全,则“除铁铝”时应控制
时,可视为沉淀完全,则“除铁铝”时应控制
___________ (保留两位有效数字)。
(4)“氟化除杂”时除钙的离子反应的平衡常数
___________ (保留两位有效数字)。“转化”时发生反应的离子方程式为___________ 。
(5)氟化钙的晶胞结构如图所示: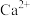 周围最近且距离相等的
周围最近且距离相等的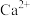 个数为
个数为___________ ,若晶体密度为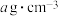 ,用
,用 表示阿伏加德罗常数的值,则晶体中
表示阿伏加德罗常数的值,则晶体中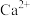 与
与 间的最近距离为
间的最近距离为___________ cm(用含 、
、 的代数式表示)。
的代数式表示)。
 ,还有少量
,还有少量 、
、 、MgO、CaO、
、MgO、CaO、 )和硫铁矿(主要含
)和硫铁矿(主要含 )回收
)回收 的工艺流程如图所示:
的工艺流程如图所示:
| 物质 |  | 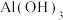 |  |  |  |  |  |
 |  | 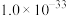 |  | 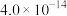 | 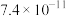 | 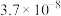 | 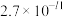 |
(1)“酸浸”时将矿石粉碎,主要目的是
(2)浸渣1中除
 和S外,还有
和S外,还有 分别与
分别与 、
、 反应产生的,其中
反应产生的,其中 与
与 反应的离子方程式为
反应的离子方程式为(3)当离子浓度
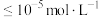 时,可视为沉淀完全,则“除铁铝”时应控制
时,可视为沉淀完全,则“除铁铝”时应控制
(4)“氟化除杂”时除钙的离子反应的平衡常数

(5)氟化钙的晶胞结构如图所示:
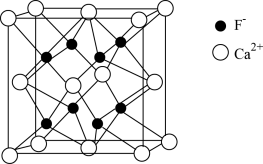
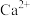 周围最近且距离相等的
周围最近且距离相等的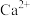 个数为
个数为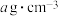 ,用
,用 表示阿伏加德罗常数的值,则晶体中
表示阿伏加德罗常数的值,则晶体中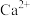 与
与 间的最近距离为
间的最近距离为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-03-26更新
|
387次组卷
|
3卷引用:2024届河南省焦作市普通高中高三上学期第一次模拟考试理科综合试题-高中化学
2024届河南省焦作市普通高中高三上学期第一次模拟考试理科综合试题-高中化学(已下线)压轴题11?无机化工流程综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)2024届河南省禹州市高级中学高三下学期综合考试(1)理综试题-高中化学
解题方法
7 . 某化学兴趣小组采用次氯酸钙与稀盐酸反应制取氯气,并探究了氯气的性质。实验装置如图所示,下列说法正确的是
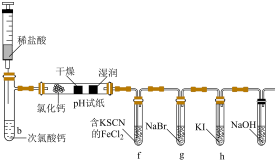
A.b试管中的离子方程式为: |
B.湿润的 试纸先变红后褪色,说明 试纸先变红后褪色,说明 有酸性,同时又有漂白性 有酸性,同时又有漂白性 |
C.f处变红,是因为 被氧化为 被氧化为 , , 遇 遇 溶液变红 溶液变红 |
D.g处变为橙色,h处变为黄色,说明氧化性: |
您最近一年使用:0次
2024-03-26更新
|
409次组卷
|
2卷引用:2024届广东省大亚湾区普通高中毕业年级高三1月份联合模拟考试(一)化学试卷
名校
解题方法
8 . 按要求完成下面小题。
(1)有以下转化关系:
反应①:___________
 在上述有序号的反应中,除了①⑥外,需用氧化剂的是
在上述有序号的反应中,除了①⑥外,需用氧化剂的是___________ (填序号)。
(2) 。该反应中,生成物M是
。该反应中,生成物M是___________ (填化学式)。
(3)针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅作氧化剂的反应是___________ (填序号,下同)。
(4)取少量NaH放入水中,剧烈反应放出一种无色、无味的气体,并形成一种碱性溶液。NaH与水反应的化学方程式为___________ 。
(5) 与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:
与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:___________ 。
(6)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药是将硫磺、木炭、硝酸钾按照一定比例混合,在发生爆炸时,没有产生污染性物质。请书写出该反应方程式并配平___________ 。
(1)有以下转化关系:

反应①:
 在上述有序号的反应中,除了①⑥外,需用氧化剂的是
在上述有序号的反应中,除了①⑥外,需用氧化剂的是(2)
 。该反应中,生成物M是
。该反应中,生成物M是(3)针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅作氧化剂的反应是
(4)取少量NaH放入水中,剧烈反应放出一种无色、无味的气体,并形成一种碱性溶液。NaH与水反应的化学方程式为
(5)
 与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:
与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:(6)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药是将硫磺、木炭、硝酸钾按照一定比例混合,在发生爆炸时,没有产生污染性物质。请书写出该反应方程式并配平
您最近一年使用:0次
2024-03-25更新
|
91次组卷
|
2卷引用:云南省丽江润泽高级中学2023-2024学年高一上学期11月月考化学试题
解题方法
9 . 某同学利用钠与硫酸铜溶液进行实验,并对其现象进行分析,研究其产物组成。
(1)硫酸铜溶液的配制:准确称取五水硫酸铜(CuSO4·5H2O)晶体2.5000g,溶解后转移至100mL容量瓶中。
①上述实验过程中,用不到的实验仪器有____ (填标号)。

②该CuSO4溶液的浓度为__________ mo/L。
③通过理论计算,当上述硫酸铜与钠完全反应,溶液质量变化为___ g。
(2)将配好的CuSO4溶液,分3组进行实验,实验结果如下图所示:
查阅资料得知:极细的铜粉,外观呈现黑色
①a组中的蓝色沉淀成分主要是_________ 。
②将c组中黑色沉淀进行抽滤,干燥,对其成分进行初步的猜想
猜想ⅰ:金属钠将铜置换出来,以极细的铜粉存在;
猜想ⅱ:金属钠与水反应剧烈放热,______________ 。
设计一个简单的实验,证明猜想ⅰ是错误的______________ 。
(3)为进一步验证黑色固体的成分,该同学求助实验室检测,得到黑色固体中含铜化合物主要有硫酸氧化铜[Cu2O(SO4)]、碱式硫酸铜[Cu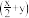 (OH)x(SO4)y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式
(OH)x(SO4)y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式____________ 。
(4)根据实验结果,可以得到的结论为____________ (写一条)。
(1)硫酸铜溶液的配制:准确称取五水硫酸铜(CuSO4·5H2O)晶体2.5000g,溶解后转移至100mL容量瓶中。
①上述实验过程中,用不到的实验仪器有

②该CuSO4溶液的浓度为
③通过理论计算,当上述硫酸铜与钠完全反应,溶液质量变化为
(2)将配好的CuSO4溶液,分3组进行实验,实验结果如下图所示:
| 序号 | CuSO4溶液体积/mL | 金属钠质量/g | 实验现象 |
| a | 15 | 0.01g | 迅速产生大量蓝色沉淀 |
| b | 15 | 0.1g | 蓝色沉淀和黑色沉淀共存 |
| c | 15 | 1.0g | 出现大量黑色沉淀 |
①a组中的蓝色沉淀成分主要是
②将c组中黑色沉淀进行抽滤,干燥,对其成分进行初步的猜想
猜想ⅰ:金属钠将铜置换出来,以极细的铜粉存在;
猜想ⅱ:金属钠与水反应剧烈放热,
设计一个简单的实验,证明猜想ⅰ是错误的
(3)为进一步验证黑色固体的成分,该同学求助实验室检测,得到黑色固体中含铜化合物主要有硫酸氧化铜[Cu2O(SO4)]、碱式硫酸铜[Cu
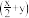 (OH)x(SO4)y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式
(OH)x(SO4)y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式(4)根据实验结果,可以得到的结论为
您最近一年使用:0次
解题方法
10 . 亚硝酸钙 广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的NO与过氧化钙反应制取
广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的NO与过氧化钙反应制取 。
。
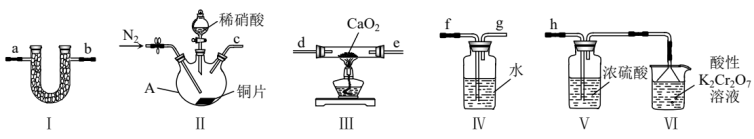
(1)仪器A的名称是___________ ,装置I中试剂名称是___________ 。
(2)装置的连接顺序是___________ (填字母)。
c→_______→_______→_______→______→_______→_______→______
(3)滴入稀硝酸前需要通入一段时间N2,待反应结束后还需继续通一会N2,继续通N2的目的是___________ 。
(4)装置Ⅱ中滴入稀硝酸后,A中观察到的现象是___________ 。
(5)装置Ⅴ的作用是___________ 。
(6)装置Ⅵ中氮元素被氧化成+5价,则反应的离子方程式为___________ 。
 广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的NO与过氧化钙反应制取
广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的NO与过氧化钙反应制取 。
。
(1)仪器A的名称是
(2)装置的连接顺序是
c→_______→_______→_______→______→_______→_______→______
(3)滴入稀硝酸前需要通入一段时间N2,待反应结束后还需继续通一会N2,继续通N2的目的是
(4)装置Ⅱ中滴入稀硝酸后,A中观察到的现象是
(5)装置Ⅴ的作用是
(6)装置Ⅵ中氮元素被氧化成+5价,则反应的离子方程式为
您最近一年使用:0次



