解题方法
1 . 亚氯酸钠 和
和 都是重要的化工原料,常用作高效、广谱、安全的杀菌消毒剂。
都是重要的化工原料,常用作高效、广谱、安全的杀菌消毒剂。
(1)用 和硫酸酸化的草酸
和硫酸酸化的草酸 反应可制得
反应可制得 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。
(2)用二氧化氯 可制备用途广泛的亚氯酸钠
可制备用途广泛的亚氯酸钠 ,实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠。
,实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠。 沸点为
沸点为 ,可溶于水,有毒,浓度较高时易发生爆炸。
,可溶于水,有毒,浓度较高时易发生爆炸。
② 饱和溶液高于
饱和溶液高于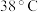 时析出
时析出 ,高于
,高于 时
时 分解为
分解为 和
和 。
。
①实验过程中需持续通入一定量的 ,说明原因
,说明原因___________ ;反应结束后需再通入一定量的 ,说明原因
,说明原因___________ 。
②写出装置 中的化学反应方程式
中的化学反应方程式___________ 。
③通入 中的
中的 与
与 中物质恰好完全反应,若从反应后的溶液中得到
中物质恰好完全反应,若从反应后的溶液中得到 固体,写出实验操作的方法
固体,写出实验操作的方法___________ 。
(3)某水样用 处理后,有少量
处理后,有少量 残留在水中,可用碘量法检测。
残留在水中,可用碘量法检测。
①取 水样,加入过量的
水样,加入过量的 ,用硫酸酸化,再加入淀粉溶液,溶液变为蓝色。写出
,用硫酸酸化,再加入淀粉溶液,溶液变为蓝色。写出 与
与 反应的离子方程式
反应的离子方程式___________ 。
②已知: ,向所得溶液中加入适量
,向所得溶液中加入适量 溶液,将溶液调节为弱酸性,再用
溶液,将溶液调节为弱酸性,再用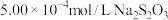 标准溶液进行滴定,恰好反应时消耗
标准溶液进行滴定,恰好反应时消耗 溶液
溶液 。计算水样中
。计算水样中 的浓度
的浓度___________ (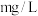 ,不要求计算过程)。
,不要求计算过程)。
 和
和 都是重要的化工原料,常用作高效、广谱、安全的杀菌消毒剂。
都是重要的化工原料,常用作高效、广谱、安全的杀菌消毒剂。(1)用
 和硫酸酸化的草酸
和硫酸酸化的草酸 反应可制得
反应可制得 ,写出该反应的离子方程式
,写出该反应的离子方程式(2)用二氧化氯
 可制备用途广泛的亚氯酸钠
可制备用途广泛的亚氯酸钠 ,实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠。
,实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠。
 沸点为
沸点为 ,可溶于水,有毒,浓度较高时易发生爆炸。
,可溶于水,有毒,浓度较高时易发生爆炸。②
 饱和溶液高于
饱和溶液高于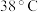 时析出
时析出 ,高于
,高于 时
时 分解为
分解为 和
和 。
。①实验过程中需持续通入一定量的
 ,说明原因
,说明原因 ,说明原因
,说明原因②写出装置
 中的化学反应方程式
中的化学反应方程式③通入
 中的
中的 与
与 中物质恰好完全反应,若从反应后的溶液中得到
中物质恰好完全反应,若从反应后的溶液中得到 固体,写出实验操作的方法
固体,写出实验操作的方法(3)某水样用
 处理后,有少量
处理后,有少量 残留在水中,可用碘量法检测。
残留在水中,可用碘量法检测。①取
 水样,加入过量的
水样,加入过量的 ,用硫酸酸化,再加入淀粉溶液,溶液变为蓝色。写出
,用硫酸酸化,再加入淀粉溶液,溶液变为蓝色。写出 与
与 反应的离子方程式
反应的离子方程式②已知:
 ,向所得溶液中加入适量
,向所得溶液中加入适量 溶液,将溶液调节为弱酸性,再用
溶液,将溶液调节为弱酸性,再用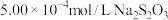 标准溶液进行滴定,恰好反应时消耗
标准溶液进行滴定,恰好反应时消耗 溶液
溶液 。计算水样中
。计算水样中 的浓度
的浓度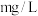 ,不要求计算过程)。
,不要求计算过程)。
您最近一年使用:0次
2 . 氮化镁用途广泛,常用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其他元素的氮化物时作为催化剂。第一次成功合成立方氮化硼时,使用的催化剂就是氮化镁。实验室可用如图装置制取 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。___________ 。
(2)装置C中氧化铜的作用是氧化氨气制取 ,其反应的化学方程式为
,其反应的化学方程式为___________ 。
(3)装置D的作用是___________ 。
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是___________ 。
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为___________ ,固体试剂X可以为___________ (填字母)。
(6)实验室还可用 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为___________ 。___________ 。
 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。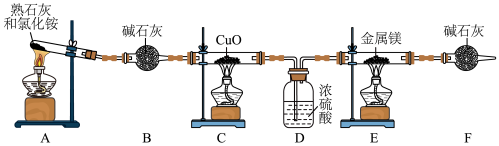
(2)装置C中氧化铜的作用是氧化氨气制取
 ,其反应的化学方程式为
,其反应的化学方程式为(3)装置D的作用是
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为
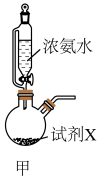
(6)实验室还可用
 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为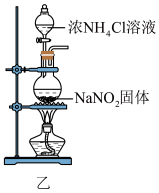
您最近一年使用:0次
名校
3 . 下列物质用途和解释匹配的是
| 选项 | 用途 | 解释 |
| A | 热纯碱溶液常作餐具洗涤剂 | 纯碱是强电解质 |
| B | 石膏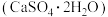 用于制作豆腐的凝固剂 用于制作豆腐的凝固剂 |  微溶于水 微溶于水 |
| C | 丁基羟基茴香醚 作油脂制品的抗氧化剂 作油脂制品的抗氧化剂 | 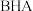 具有较强的还原性 具有较强的还原性 |
| D | 干冰、冰常用作制冷剂 | 断裂化学键吸收热量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 铊(Tl)本身是一种剧毒物质,为毒性最大的金属元素之一,但是铊在工业中的用途非常广泛,主要存在于一些矿物和工业废水中,也可以从含铊的合金中提取.从某铅锌厂的富铊灰(主要成分为 、
、 、
、 、
、 、
、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示:
①在氯化物-硫酸水溶液中,铊元素以 形式存在;
形式存在;
(2)萃取过程的反应原理为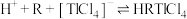 .
.
请回答下列问题:
(1)基态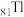 原子核外电子的运动状态有
原子核外电子的运动状态有________ 种.
(2)“浸取I”过程中为提高铊的浸取速率,可采取的措施有________________ (写出两条).
(3)写出“浸取I”中 发生反应的化学方程式:
发生反应的化学方程式:________________ ,“滤渣”的主要成分是________ (填化学式).
(4)请从化学平衡的角度解释“反萃取”过程中加入 溶液的原因:
溶液的原因:________________ .
(5)写出“还原氯化沉淀”中反应的离子方程式:________________ .
(6)通过沉淀法也可以去除工业废水中的 和
和 .
.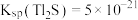 ,某地区规定工业污水中铊的污染物排放限值为
,某地区规定工业污水中铊的污染物排放限值为 ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中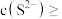
________  (假设污水中铊全部以
(假设污水中铊全部以 形式存在).
形式存在).
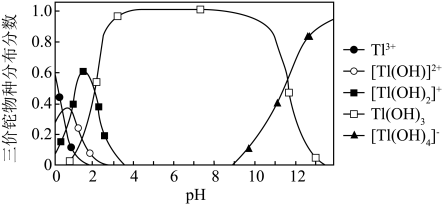
②向含铊废水中加入溴水,使 充分氧化成
充分氧化成 ,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是________________ .
 、
、 、
、 、
、 、
、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示: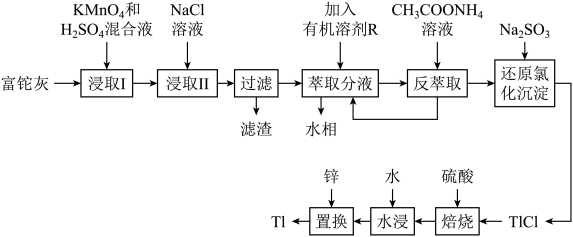
①在氯化物-硫酸水溶液中,铊元素以
 形式存在;
形式存在;(2)萃取过程的反应原理为
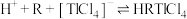 .
.请回答下列问题:
(1)基态
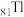 原子核外电子的运动状态有
原子核外电子的运动状态有(2)“浸取I”过程中为提高铊的浸取速率,可采取的措施有
(3)写出“浸取I”中
 发生反应的化学方程式:
发生反应的化学方程式:(4)请从化学平衡的角度解释“反萃取”过程中加入
 溶液的原因:
溶液的原因:(5)写出“还原氯化沉淀”中反应的离子方程式:
(6)通过沉淀法也可以去除工业废水中的
 和
和 .
.
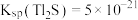 ,某地区规定工业污水中铊的污染物排放限值为
,某地区规定工业污水中铊的污染物排放限值为 ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中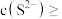
 (假设污水中铊全部以
(假设污水中铊全部以 形式存在).
形式存在).②向含铊废水中加入溴水,使
 充分氧化成
充分氧化成 ,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
您最近一年使用:0次
解题方法
5 . 碱金属和碱土金属元素分别位于元素周期表的ⅠA族和ⅡA族,它们的化合物应用广泛。历史上曾以NaCl为原料生产NaOH作为化学工业开端的标志。 可由侯氏制碱法获得。
可由侯氏制碱法获得。 是强氧化剂,熔融条件下可将
是强氧化剂,熔融条件下可将 氧化为
氧化为 。格氏试剂(如
。格氏试剂(如 )在有机化学中有重要用途,但易与空气中的
)在有机化学中有重要用途,但易与空气中的 等发生反应。盐卤水中含有
等发生反应。盐卤水中含有 ,常用于豆制品加工。
,常用于豆制品加工。 受热分解最终生成MgO。
受热分解最终生成MgO。
碱金属及碱土金属元素及其化合物的转化具有重要应用。下列说法不正确的是
 可由侯氏制碱法获得。
可由侯氏制碱法获得。 是强氧化剂,熔融条件下可将
是强氧化剂,熔融条件下可将 氧化为
氧化为 。格氏试剂(如
。格氏试剂(如 )在有机化学中有重要用途,但易与空气中的
)在有机化学中有重要用途,但易与空气中的 等发生反应。盐卤水中含有
等发生反应。盐卤水中含有 ,常用于豆制品加工。
,常用于豆制品加工。 受热分解最终生成MgO。
受热分解最终生成MgO。碱金属及碱土金属元素及其化合物的转化具有重要应用。下列说法不正确的是
A.侯氏制碱法中的物质转化: |
B.由 制备乙酸的物质转化: 制备乙酸的物质转化: |
C.电解饱和NaCl溶液的阴极反应: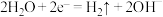 |
D. 与 与 共熔的反应: 共熔的反应: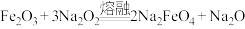 |
您最近一年使用:0次
名校
解题方法
6 . 碳酸锌在工业上用途广泛。利用某种浸锌渣(主要含有 )制备
)制备 的一种流程如下:
的一种流程如下: ;
;
②室温下,部分离子浓度的对数 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体 中主要成分是
中主要成分是______ (填化学式)。
(2)“碱浸”后,浸出液中含有金属元素的离子主要是 和
和______ (填离子符号);欲使浸出液中的含锌微粒完全沉淀,应调节 的范围是
的范围是______ 。
(3)浸渣回收银的过程中有配合物 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为______ 。
(4)“除杂”时滤渣的主要成分是______ (填化学式)。
(5)“沉锌”时发生反应的离子方程式为______ ;此过程不宜用碳酸钠代替碳酸氢铵,原因是______ 。
 )制备
)制备 的一种流程如下:
的一种流程如下: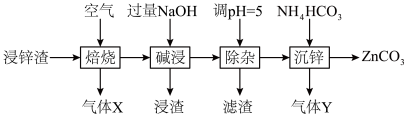
 ;
;②室温下,部分离子浓度的对数
 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):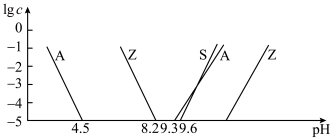
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体
 中主要成分是
中主要成分是(2)“碱浸”后,浸出液中含有金属元素的离子主要是
 和
和 的范围是
的范围是(3)浸渣回收银的过程中有配合物
 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为(4)“除杂”时滤渣的主要成分是
(5)“沉锌”时发生反应的离子方程式为
您最近一年使用:0次
2024-04-21更新
|
230次组卷
|
3卷引用:云南省罗平第一中学2024年高三二模考试化学试题
名校
解题方法
7 .  俗称海波,水处理中常用作还原剂除氯、冶金中常用作络合剂,摄影中常用作定影剂。遇酸、受热都易分解。工业上常用以下两种方法制备:
俗称海波,水处理中常用作还原剂除氯、冶金中常用作络合剂,摄影中常用作定影剂。遇酸、受热都易分解。工业上常用以下两种方法制备:
(1)亚硫酸钠法:
①需用除氧蒸馏水配制亚硫酸钠溶液。研细硫粉,用___________ 润湿后加入 溶液中,水浴加热后再经重结晶精制。
溶液中,水浴加热后再经重结晶精制。
②若未用除氧蒸馏水配制亚硫酸钠溶液,导致产品中存在的杂质为___________ ,证明含有该杂质的方法是___________ 。
(2)硫化钠法:选用以下必要的装置,利用 与
与 、
、 的混合溶液反应制备
的混合溶液反应制备 。
。___________ 。
②丁装置中 与
与 、
、 混合液反应生成
混合液反应生成 的化学方程式:
的化学方程式:___________ 。
③实验过程中,丁中的澄清溶液先变浑浊后变澄清,此时生成大量的 ,一段时间后,丁中再次出现少量浑浊,此时须立刻停止通入
,一段时间后,丁中再次出现少量浑浊,此时须立刻停止通入 ,用离子方程式解释立刻停止通入
,用离子方程式解释立刻停止通入 的原因:
的原因:___________ 。
④简述检验丁装置中导出气体中含有 的方法:
的方法:___________ 。
(3) 的用途:做冶金工业络合剂。
的用途:做冶金工业络合剂。
黄金(Au)浸取工艺:将金矿石浸泡在 、
、 的混合溶液中,并通入
的混合溶液中,并通入 。其中
。其中 作为催化剂参与反应,方程式为:
作为催化剂参与反应,方程式为: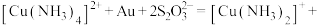
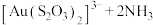 ,则浸金总反应的离子方程式为:
,则浸金总反应的离子方程式为:___________ 。
 俗称海波,水处理中常用作还原剂除氯、冶金中常用作络合剂,摄影中常用作定影剂。遇酸、受热都易分解。工业上常用以下两种方法制备:
俗称海波,水处理中常用作还原剂除氯、冶金中常用作络合剂,摄影中常用作定影剂。遇酸、受热都易分解。工业上常用以下两种方法制备:(1)亚硫酸钠法:
①需用除氧蒸馏水配制亚硫酸钠溶液。研细硫粉,用
 溶液中,水浴加热后再经重结晶精制。
溶液中,水浴加热后再经重结晶精制。②若未用除氧蒸馏水配制亚硫酸钠溶液,导致产品中存在的杂质为
(2)硫化钠法:选用以下必要的装置,利用
 与
与 、
、 的混合溶液反应制备
的混合溶液反应制备 。
。
②丁装置中
 与
与 、
、 混合液反应生成
混合液反应生成 的化学方程式:
的化学方程式:③实验过程中,丁中的澄清溶液先变浑浊后变澄清,此时生成大量的
 ,一段时间后,丁中再次出现少量浑浊,此时须立刻停止通入
,一段时间后,丁中再次出现少量浑浊,此时须立刻停止通入 ,用离子方程式解释立刻停止通入
,用离子方程式解释立刻停止通入 的原因:
的原因:④简述检验丁装置中导出气体中含有
 的方法:
的方法:(3)
 的用途:做冶金工业络合剂。
的用途:做冶金工业络合剂。黄金(Au)浸取工艺:将金矿石浸泡在
 、
、 的混合溶液中,并通入
的混合溶液中,并通入 。其中
。其中 作为催化剂参与反应,方程式为:
作为催化剂参与反应,方程式为: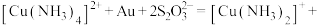
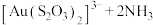 ,则浸金总反应的离子方程式为:
,则浸金总反应的离子方程式为:
您最近一年使用:0次
解题方法
8 . 以菱锰矿(主要成分为MnCO3,还含有铁、镍的碳酸盐以及SiO2杂质)为原料生产次锰酸钠(Na3MnO4)的工艺流程如图:
(1)次锰酸钠中Mn的化合价为___________ ;滤渣1的主要成分为MnO2和___________ (填化学式)。
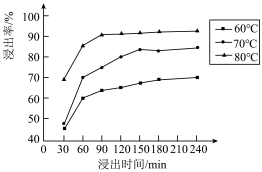
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为___________ 。___________ 。
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=___________ 。
(5)“母液1”中主要溶质的用途___________ 。
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为___________ 。
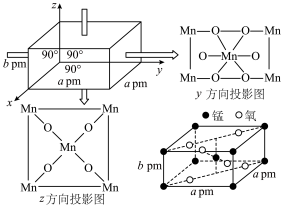
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。___________ ,Mn与Mn之间最近(顶点和体心)距离为___________ pm。(用含a、b的代数式表示)

| 物质 | MnS | NiS |
| Ksp | 2.0×10-13 | 1.0×10-21 |
(1)次锰酸钠中Mn的化合价为
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=
(5)“母液1”中主要溶质的用途
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。
您最近一年使用:0次
9 . 盐酸在中学阶段用途广泛,下列关于盐酸用法错误的是
| A.硫酸根离子的检验 | B.氯化铁溶液的配制 |
| C.高锰酸钾溶液的酸化 | D.氯化镁的结晶 |
您最近一年使用:0次
解题方法
10 .  和
和 都具有广泛的用途。
都具有广泛的用途。
Ⅰ.工业上用软锰矿(主要含 )和硫锰矿(主要含
)和硫锰矿(主要含 )联合制备
)联合制备 的流程如图。
的流程如图。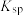
(1)为提高浸出速率,可采取的措施有_________________ (答出两条即可)。
(2)浸出过程中产生的 对
对 与
与 的反应起催化作用,机理如下。
的反应起催化作用,机理如下。
ⅰ.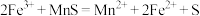 ;
;
ⅱ._________________ (离子方程式)。
(3)流程图中采用①和②共同除去浸出液中金属阳离子杂质,解释不能单独使用①去除这些杂质离子的原因:_____________ 。
(4)滤渣2的主要成分是_________________ 。
Ⅱ.以 溶液为原料,用图1装置(
溶液为原料,用图1装置(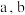 均为惰性电极)同步制备
均为惰性电极)同步制备 和
和 。
。_________________ 。
(6)图1中 电极上
电极上 的电解效率
的电解效率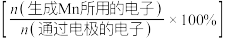 与溶液
与溶液 的关系如图2所示。随
的关系如图2所示。随 的增大,电解效率先增大后减小的原因是
的增大,电解效率先增大后减小的原因是_________________ 。
 和
和 都具有广泛的用途。
都具有广泛的用途。Ⅰ.工业上用软锰矿(主要含
 )和硫锰矿(主要含
)和硫锰矿(主要含 )联合制备
)联合制备 的流程如图。
的流程如图。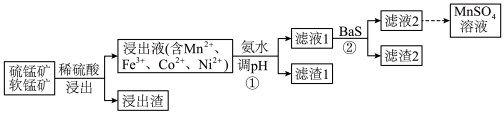
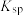
| 硫化物 |  |  |  |  (易溶) (易溶) |
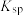 | 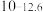 | 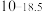 |  | |
| 氢氧化物 |  |  |  |  |
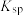 | 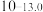 | 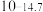 | 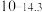 |  |
(1)为提高浸出速率,可采取的措施有
(2)浸出过程中产生的
 对
对 与
与 的反应起催化作用,机理如下。
的反应起催化作用,机理如下。ⅰ.
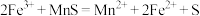 ;
;ⅱ.
(3)流程图中采用①和②共同除去浸出液中金属阳离子杂质,解释不能单独使用①去除这些杂质离子的原因:
(4)滤渣2的主要成分是
Ⅱ.以
 溶液为原料,用图1装置(
溶液为原料,用图1装置( 均为惰性电极)同步制备
均为惰性电极)同步制备 和
和 。
。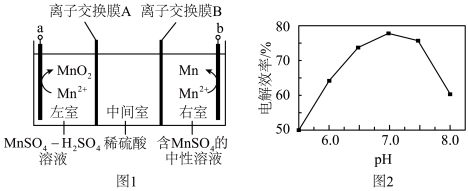
(6)图1中
 电极上
电极上 的电解效率
的电解效率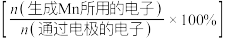 与溶液
与溶液 的关系如图2所示。随
的关系如图2所示。随 的增大,电解效率先增大后减小的原因是
的增大,电解效率先增大后减小的原因是
您最近一年使用:0次



