1 . 已知硫酸酸化的K2Cr2O7溶液能与KI反应:aH2SO4+bK2Cr2O7+cKI=mK2SO4+nI2+pCr2(SO4)3+qH2O,下列说法错误的是
| A.a=7 |
| B.K2Cr2O7也可用盐酸酸化 |
| C.每生成1molCr2(SO4)3,转移6mole- |
| D.由上述反应可知,I-的还原性强于Cr3+的还原性 |
您最近一年使用:0次
2021-10-01更新
|
274次组卷
|
4卷引用:宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题
名校
2 . 硝酸厂的烟气中含有大量的氮氧化物( ),将烟气与
),将烟气与 的混合气体通入
的混合气体通入 与
与 (
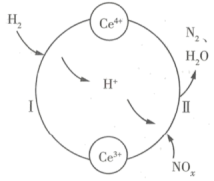
( 为铈元素)的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
为铈元素)的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
 ),将烟气与
),将烟气与 的混合气体通入
的混合气体通入 与
与 (
( 为铈元素)的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
为铈元素)的混合溶液中实现无害化处理,其转化过程如图所示。下列说法正确的是
A.过程Ⅰ发生反应的离子方程式为 |
B. 时,过程Ⅱ中氧化剂与还原剂的物质的量之比为 时,过程Ⅱ中氧化剂与还原剂的物质的量之比为 |
C.处理过程中,混合溶液中 和 和 总数减少 总数减少 |
D.该转化过程的实质为 被 被 还原 还原 |
您最近一年使用:0次
2021-06-05更新
|
765次组卷
|
23卷引用:宁夏石嘴山市第三中学2021届高三上学期第一次月考化学试题
宁夏石嘴山市第三中学2021届高三上学期第一次月考化学试题北京市通州区2020届高三上学期期末摸底考试化学试题北京市2020届高三下学期周末测试化学试题天津市南开区2020届高三年级第二次模拟考试化学试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编(已下线)专题04 氧化还原反应-2020年高考真题和模拟题化学分项汇编(已下线)易错05 氧化还原反应概念及规律-备战2021年高考化学一轮复习易错题广东省广州市2021届高三年级阶段训练化学试题山西省运城市景胜中学2020-2021学年高一10月月考化学试题山东省潍坊市诸城一中2021届高三11月份模拟化学试题甘肃省武威第一中学2021届高三上学期第三次阶段性考试化学试题河南省顶级名校2021届高三年级上学期期中考试化学试题江西师范大学附属中学2020-2021学年高一下学期4月月考化学试题江苏省扬州中学2020-2021高一下学期5月月考化学试题江西省石城中学2020-2021学年高一下学期第二次月考化学试题(苏教版2019)必修第二册专题7 氮与社会可持续发展 C 高考挑战区黑龙江省八校2022届高三上学期期中联合考试化学试题江苏省连云港市赣榆第一中学2021-2022学年高三上学期10月月考化学试题(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-练习内蒙古海拉尔第二中学2021-2022学年高三上学期第三次阶段考化学试题云南省丽江市2021-2022学年高一下学期期末考试化学试题山东省枣庄滕州市2022-2023学年高三上学期期中考试化学试题山东省滕州市第二中学2022-2023学年高三上学期11月定时检测化学试题
名校
解题方法
3 . 含有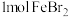 的溶液中,通入
的溶液中,通入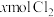 ,反应的离子方程式表示错误的是
,反应的离子方程式表示错误的是
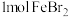 的溶液中,通入
的溶液中,通入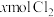 ,反应的离子方程式表示错误的是
,反应的离子方程式表示错误的是A.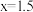 , ,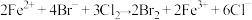 |
B.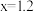 , ,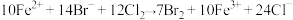 |
C. , ,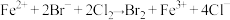 |
D. , ,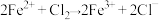 |
您最近一年使用:0次
2021-04-08更新
|
650次组卷
|
4卷引用:宁夏石嘴山市第三中学2021-2022学年高三上学期期中考试化学(理)试题
宁夏石嘴山市第三中学2021-2022学年高三上学期期中考试化学(理)试题上海市金山区2021届高三二模化学试题(已下线)三轮冲刺卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)陕西省西安市铁一中学2023-2024学年高一上学期第二次月考化学试题
解题方法
4 . 用软锰矿(主要成分为MnO2,所含杂质为质量分数约8%Fe3O4和约5%Al2O3)和BaS制备高纯MnCO3,同时制得Ba(OH)2,工艺流程如下:
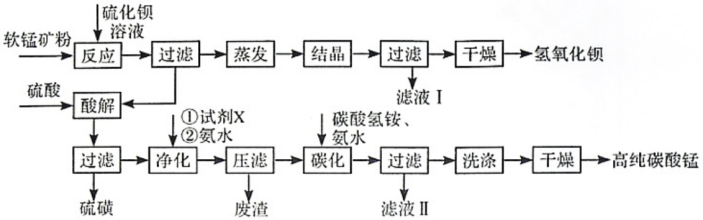
已知:25℃时相关物质的Ksp见下表
回答下列问题:
(1)MnO2与BaS溶液反应转化为MnO的化学方程式为___________ ,能否通过加热的方式加快该反应的速率,___________ (填“能”或“否”)
(2)已知MnO2为两性氧化物,保持BaS投料量不变,随软锰矿粉与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)2的量达到最大值后会减小,减小的原因是___________ 。
(3)在实验室进行过滤操作时,除了使用铁架台和烧杯以外,还需要的玻璃仪器为___________ 。
(4)净化时需先加入的试剂X为___________ (填化学式) 。再使用氨水调溶液的pH,则pH的理论最小值为___________ (当溶液中某离子浓度小于1.0×10-5mol•L-1时,可认为该离子沉淀完全)。
(5)碳化过程中发生反应的离子方程式为___________ 。

已知:25℃时相关物质的Ksp见下表
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 |
(1)MnO2与BaS溶液反应转化为MnO的化学方程式为
(2)已知MnO2为两性氧化物,保持BaS投料量不变,随软锰矿粉与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)2的量达到最大值后会减小,减小的原因是
(3)在实验室进行过滤操作时,除了使用铁架台和烧杯以外,还需要的玻璃仪器为
(4)净化时需先加入的试剂X为
(5)碳化过程中发生反应的离子方程式为
您最近一年使用:0次
2021-03-14更新
|
445次组卷
|
3卷引用:宁夏石嘴山市2021届高三下学期3月高考质量监测(一模) 化学试题
名校
解题方法
5 . HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是_______ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,能用来区分NaNO2和NaCl的是_______ (填序号)。
A.分别溶于水看溶解情况
B.在酸性条件下加入KI淀粉溶液来区别
C.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:_______ 。
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是_______ (填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑,_____ ,若有1molFeSO4反应,则反应中转移____ mol电子。
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,能用来区分NaNO2和NaCl的是
A.分别溶于水看溶解情况
B.在酸性条件下加入KI淀粉溶液来区别
C.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑,
您最近一年使用:0次
6 . 一种新型高效净水剂PAFC(聚合氯化铁铝[AlFe(OH)nC16-n]m),广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC,设计生产流程如图:

(1)浓盐酸配制一定物质的量浓度的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有___ 。
A.容量瓶 B.烧杯 C.烧瓶 D.酒精灯
(2)下列关于PAFC的说法中正确的是____ 。
A.PAFC是一种无机高分子化合物
B.PAFC中Fe显+2价
C.PAFC溶于水能电离出OH-,是一种碱
D.PAFC在强酸性和强碱性溶液中均不能稳定存在
(3)步骤Ⅱ中取样分析的目的是___ 。
A.测定溶液中Fe2+与Fe3+的含量比
B.测定原料是否完全溶解
C.测定溶液中Fe2+的含量,以确定加入NaClO3的量
D.测定溶液中Al3+的含量
(4)写出向溶液中加入NaClO3时,发生反应的离子方程式:___Fe2++___H++___C1O →____Fe3++____Cl-+____H2O
→____Fe3++____Cl-+____H2O___ 。
(5)该化工厂的化验室为测定产品PAFC中A1和Fe的含量,进行下列试剂的选择和基本操作:
①测定时所需的试剂有___ 。
A.NH3·H2O B.NaOH C.CO2 D.NaClO3
②在测定过程中的操作顺序是:过滤、___ 、灼烧、__ 、称量。(写操作名称)。
③测定时,通过灼烧后等操作,直接测定的是___ 和___ 的质量(填化学式)。

(1)浓盐酸配制一定物质的量浓度的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有
A.容量瓶 B.烧杯 C.烧瓶 D.酒精灯
(2)下列关于PAFC的说法中正确的是
A.PAFC是一种无机高分子化合物
B.PAFC中Fe显+2价
C.PAFC溶于水能电离出OH-,是一种碱
D.PAFC在强酸性和强碱性溶液中均不能稳定存在
(3)步骤Ⅱ中取样分析的目的是
A.测定溶液中Fe2+与Fe3+的含量比
B.测定原料是否完全溶解
C.测定溶液中Fe2+的含量,以确定加入NaClO3的量
D.测定溶液中Al3+的含量
(4)写出向溶液中加入NaClO3时,发生反应的离子方程式:___Fe2++___H++___C1O
 →____Fe3++____Cl-+____H2O
→____Fe3++____Cl-+____H2O(5)该化工厂的化验室为测定产品PAFC中A1和Fe的含量,进行下列试剂的选择和基本操作:
①测定时所需的试剂有
A.NH3·H2O B.NaOH C.CO2 D.NaClO3
②在测定过程中的操作顺序是:过滤、
③测定时,通过灼烧后等操作,直接测定的是
您最近一年使用:0次
名校
7 . 作为食品添加剂时,亚硝酸钠 可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
Ⅰ 制备
制备
实验室以木炭、浓硝酸、 为主要原料按照如图所示装置制备亚硝酸钠
为主要原料按照如图所示装置制备亚硝酸钠 加热装置及部分夹持装置已略去
加热装置及部分夹持装置已略去 ,反应原理为:
,反应原理为:
回答下列问题:
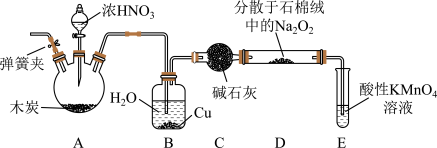
(1)连接好装置之后,下一步实验操作是______ 。
(2) 装置中铜的作用是
装置中铜的作用是______ 。
(3) 装置用于尾气处理,E中反应的离子方程式为
装置用于尾气处理,E中反应的离子方程式为______ 。
(4)实验结束阶段,熄灭酒精灯之后继续通入 直至装置冷却。此时通入
直至装置冷却。此时通入 的目的是
的目的是______ 。
Ⅱ 含量的测定
含量的测定
查阅资料可知:酸性 溶液可将
溶液可将 氧化为
氧化为 ,
, 还原成
还原成 。
。
(5)溶液配制:称取装置D中反应后的固体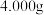 ,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的
,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的______ 中,加蒸馏水至______ 。
滴定:取 溶液于锥形瓶中,用
溶液于锥形瓶中,用 酸性
酸性 溶液进行滴定,实验数据如下表所示:
溶液进行滴定,实验数据如下表所示:
(6)第4组实验数据出现异常,造成这种异常的原因可能是______  双项选择
双项选择 。
。
A.锥形瓶洗净后未干燥 滴定终了仰视读数
滴定终了仰视读数
C.滴定终了俯视读数 酸式滴定管用蒸馏水洗净后未用标准液润洗
酸式滴定管用蒸馏水洗净后未用标准液润洗
(7)根据表中数据,计算所得固体中亚硝酸钠的质量分数______ 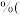 保留2位小数
保留2位小数 。
。
 可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。
可以增加肉类的鲜度,抑制微生物,保持肉制品的结构和营养价值;但是过量振入会导致中毒。某实验小组设计实验制备亚硝酸钠并进行含量测定。Ⅰ
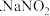 制备
制备实验室以木炭、浓硝酸、
 为主要原料按照如图所示装置制备亚硝酸钠
为主要原料按照如图所示装置制备亚硝酸钠 加热装置及部分夹持装置已略去
加热装置及部分夹持装置已略去 ,反应原理为:
,反应原理为:
回答下列问题:

(1)连接好装置之后,下一步实验操作是
(2)
 装置中铜的作用是
装置中铜的作用是(3)
 装置用于尾气处理,E中反应的离子方程式为
装置用于尾气处理,E中反应的离子方程式为(4)实验结束阶段,熄灭酒精灯之后继续通入
 直至装置冷却。此时通入
直至装置冷却。此时通入 的目的是
的目的是Ⅱ
 含量的测定
含量的测定查阅资料可知:酸性
 溶液可将
溶液可将 氧化为
氧化为 ,
, 还原成
还原成 。
。(5)溶液配制:称取装置D中反应后的固体
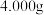 ,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的
,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,全部转移至250mL的滴定:取
 溶液于锥形瓶中,用
溶液于锥形瓶中,用 酸性
酸性 溶液进行滴定,实验数据如下表所示:
溶液进行滴定,实验数据如下表所示:| 滴定次数 | 1 | 2 | 3 | 4 |
 溶液体积 溶液体积 | 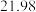 | 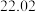 |  | 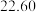 |
 双项选择
双项选择 。
。A.锥形瓶洗净后未干燥
 滴定终了仰视读数
滴定终了仰视读数C.滴定终了俯视读数
 酸式滴定管用蒸馏水洗净后未用标准液润洗
酸式滴定管用蒸馏水洗净后未用标准液润洗(7)根据表中数据,计算所得固体中亚硝酸钠的质量分数
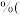 保留2位小数
保留2位小数 。
。
您最近一年使用:0次
2020-11-14更新
|
144次组卷
|
2卷引用:宁夏石嘴山市平罗中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
8 . 已知某一反应体系反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2,则关于该反应体系说法错误的是
| A.该反应的化学方程式为2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O |
| B.该反应中的氧化剂是H2O2,还原产物是O2 |
| C.氧化性:H2CrO4 > O2 |
| D.如反应转移了0.3mol电子,则产生的气体在标准状况下体积为3.36L |
您最近一年使用:0次
2020-11-07更新
|
192次组卷
|
9卷引用:宁夏石嘴山市第三中学2020届高三上学期第一次适应性(开学)考试化学试题
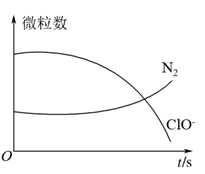
9 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
| A.该反应中Cl-为氧化产物 |
| B.消耗1个还原剂微粒,转移6e- |
C. 被ClO-氧化成N2 被ClO-氧化成N2 |
| D.反应后溶液的酸性减弱 |
您最近一年使用:0次
2020-10-02更新
|
1134次组卷
|
8卷引用:宁夏回族自治区石嘴山市平罗中学2020届高三上学期期中考试化学试题
10 . 过氧化氢H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是______ (填字母)。
(2)H2O2既体现氧化性又体现还原性的反应是_______ (填字母)。
(3)在稀硫酸中,KMnO4和H2O2能构成原电池。其中负极反应为:H2O2-2e-=2H++O2↑,正极反应: +5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:
+5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:___________ 。
(4)在K2Cr2O7+14HCl=2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3mol电子转移时生成Cl2的体积为______ (标准状况),被氧化的HCl的物质的量为___________ 。
(5)除去镁粉中混入的铝粉杂质用____ 溶解、___ 方法分离,化学反应方程式为___ 。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是
(2)H2O2既体现氧化性又体现还原性的反应是
(3)在稀硫酸中,KMnO4和H2O2能构成原电池。其中负极反应为:H2O2-2e-=2H++O2↑,正极反应:
 +5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:
+5e-+8H+=Mn2++4H2O,写出该氧化还原反应的离子方程式:(4)在K2Cr2O7+14HCl=2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3mol电子转移时生成Cl2的体积为
(5)除去镁粉中混入的铝粉杂质用
您最近一年使用:0次



