名校
1 . MnO2在电池、玻璃、有机合成等工业生产中应用广泛。利用粗MnO2(含有杂质MnO和MnCO3)制取纯MnO2的流程如图:
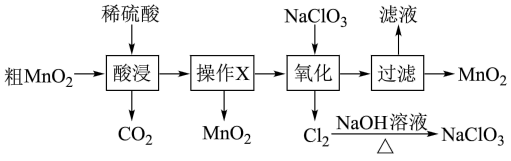
下列说法错误的是

下列说法错误的是
| A.酸浸过程中可以用浓盐酸代替稀硫酸 |
| B.操作X的名称是过滤 |
C.氧化过程发生反应的离子方程式为:5Mn2++2ClO +4H2O=5MnO2↓+Cl2↑+8H+ +4H2O=5MnO2↓+Cl2↑+8H+ |
| D.Cl2与NaOH溶液加热反应得到的NaClO3可以循环使用 |
您最近一年使用:0次
2020-08-24更新
|
1498次组卷
|
9卷引用:宁夏石嘴山市第三中学2021届高三上学期第二次月考化学试题
宁夏石嘴山市第三中学2021届高三上学期第二次月考化学试题广东省惠州市2021届高三上学期第一次调研考试化学试题湖南省长沙市雅礼中学2021届高三上学期第二次月考化学试题(已下线)学科网2020年高三11月大联考考后强化卷(新课标Ⅲ卷)(已下线)学科网2020年高三11月大联考考后强化卷(新课标Ⅱ卷)甘肃省嘉峪关市第一中学2021届高三上学期二模考试化学试题甘肃省民乐县第一中学2021-2022学年高三上学期10月诊断考试化学试题湖北省仙桃中学、天门中学(A班)2021-2022学年高二上学期期中考试化学试题新疆第二师八一中学2022-2023学年高三上学期第一次月考化学试题
名校
解题方法
2 . 黄铁矿(主要成分为FeS2)的有效利用对环境具有重要意义。
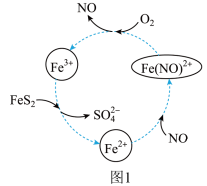
(1)在酸性条件下催化氧化黄铁矿的物质转化关系如图1所示。
①图1转化过程的总反应中,FeS2做__ (填“催化剂”“氧化剂”或“还原剂”,下同)。该转化过程中NO的作用是__ 。
②写出图1中Fe3+与FeS2反应的离子方程式:__ 。
(2)Fe2+被氧化为Fe3+的过程中,控制起始时Fe2+的浓度、溶液体积和通入O2的速率不变,改变其他条件时,Fe2+被氧化的转化率随时间的变化如图2所示。
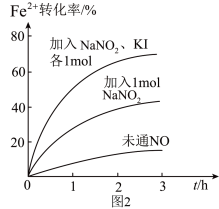
①加入NaNO2发生反应:2H++3NO =NO
=NO +2NO↑+H2O。该反应中若有6molNaNO2完全反应,转移电子的物质的量为
+2NO↑+H2O。该反应中若有6molNaNO2完全反应,转移电子的物质的量为__ mol。
②加入NaNO2、KI发生反应:4H++2NO +2I-=2NO↑+I2+2H2O。解释图2中该条件下能进一步提高单位时间内Fe2+转化率的原因:
+2I-=2NO↑+I2+2H2O。解释图2中该条件下能进一步提高单位时间内Fe2+转化率的原因:__ 。

(1)在酸性条件下催化氧化黄铁矿的物质转化关系如图1所示。
①图1转化过程的总反应中,FeS2做
②写出图1中Fe3+与FeS2反应的离子方程式:
(2)Fe2+被氧化为Fe3+的过程中,控制起始时Fe2+的浓度、溶液体积和通入O2的速率不变,改变其他条件时,Fe2+被氧化的转化率随时间的变化如图2所示。

①加入NaNO2发生反应:2H++3NO
 =NO
=NO +2NO↑+H2O。该反应中若有6molNaNO2完全反应,转移电子的物质的量为
+2NO↑+H2O。该反应中若有6molNaNO2完全反应,转移电子的物质的量为②加入NaNO2、KI发生反应:4H++2NO
 +2I-=2NO↑+I2+2H2O。解释图2中该条件下能进一步提高单位时间内Fe2+转化率的原因:
+2I-=2NO↑+I2+2H2O。解释图2中该条件下能进一步提高单位时间内Fe2+转化率的原因:
您最近一年使用:0次
2020-08-16更新
|
311次组卷
|
6卷引用:宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题
宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题河北省承德市各县第一中学2018届高三上学期期末考试化学试题(已下线)第08讲 氧化还原反应的基本概念和规律(精练)——2021年高考化学一轮复习讲练测(已下线)第03讲 氧化还原反应(练)-2023年高考化学一轮复习讲练测(新教材新高考)辽宁省沈阳市辽中区第二高级中学2021-2022学年高二下学期摸底考试化学试题(已下线)第4讲 氧化还原反应的基本概念与规律
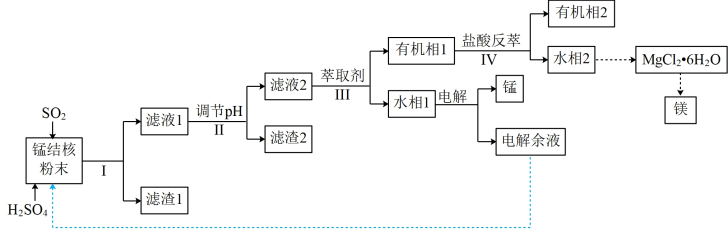
3 . 用海底锰结核(主要成分为MnO2,含少量MgO、Fe2O3、Al2O3、SiO2)为原料,制备金属锰、镁的一种工艺流程路线如下:
已知:①几种难溶物的溶度积(25℃)如下表所示:
②溶液中某离子浓度≤1.0×10-6mol·L-1时,认为该离子沉淀完全。
完成下列问题:
(1)“锰结核粉末”中MnO2与SO2反应的离子方程式为_____ 。
(2)“滤液1”中c(Mn2+)为0.18mol·L-1,则“调节pH”的范围为_______ ,“滤渣2”的成分为______ 。
(3)“Ⅲ”处“萃取剂”萃取的成分是___ ;“Ⅳ”处用“盐酸反萃”的作用是____ 。
(4)MgCl2·6H2O制取无水MgCl2时,需要在干燥的HCl气流中加热分解。HCl的作用为__________ 。
(5)该工艺流程中除电解余液可循环利用外,还能循环利用的试剂为____ 。
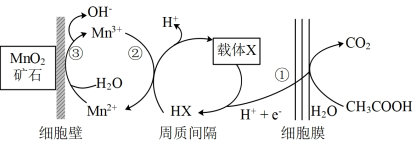
(6)一种海生假单孢菌(采自太平洋深海处),在无氧条件下以醋酸为电子供体还原MnO2生成Mn2+的机理如图所示。写出反应②③的总反应的离子方程式____________ 。

已知:①几种难溶物的溶度积(25℃)如下表所示:
| 化学式 | Mg(OH)2 | Mn(OH)2 | Al(OH)3 | Fe(OH)3 |
| Ksp | 1.8×10-11 | 1.8×10-13 | 1.0×10-33 | 4.0×10-38 |
②溶液中某离子浓度≤1.0×10-6mol·L-1时,认为该离子沉淀完全。
完成下列问题:
(1)“锰结核粉末”中MnO2与SO2反应的离子方程式为
(2)“滤液1”中c(Mn2+)为0.18mol·L-1,则“调节pH”的范围为
(3)“Ⅲ”处“萃取剂”萃取的成分是
(4)MgCl2·6H2O制取无水MgCl2时,需要在干燥的HCl气流中加热分解。HCl的作用为
(5)该工艺流程中除电解余液可循环利用外,还能循环利用的试剂为
(6)一种海生假单孢菌(采自太平洋深海处),在无氧条件下以醋酸为电子供体还原MnO2生成Mn2+的机理如图所示。写出反应②③的总反应的离子方程式

您最近一年使用:0次
2020-07-20更新
|
567次组卷
|
6卷引用:宁夏石嘴山市第三中学2021届高三上学期期末考试理综化学试题
宁夏石嘴山市第三中学2021届高三上学期期末考试理综化学试题河南省郑州市2020届高三第三次质量预测理科综合化学试题(已下线)2021年高考化学押题预测卷(山东卷)(01)(含考试版、答题卡、参考答案、全解全析)陕西省西安中学2021届高三第七次模拟考试化学试题甘肃省武威第六中学 2022~2023学年高三上学期第二次阶段性考试化学试题广东省开平市忠源纪念中学2022届高三考前热身考试化学试题
名校
4 . (1)一个体重50kg的健康人含Fe元素约2g。主要以Fe2+、Fe3+形式存在于人体内。Fe2+易被吸收,给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用Vc可使食物中的Fe3+转化为Fe2+。人体中经常进行Fe2+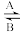 Fe3+的转化,在过程A中,Fe2+做
Fe3+的转化,在过程A中,Fe2+做__ 剂,过程B中Fe3+做___ 剂。
(2)请按要求正确书写:
①“铁与硫酸铜溶液反应”(离子方程式):__ ;
②用CO还原Fe2O3(化学方程式):__ 。
(3)某一反应中有反应物和生成物的粒子共6种:SO32-、I2、H+、SO42-、I-、H2O,已知该反应中I2只发生如下过程:I2→I-,请回答:
①该反应的还原剂是__ (填分子或离子符号)。
②反应过程中,每有1molI2发生反应,转移的电子数为__ 。
③写出该反应的离子方程式(用单线桥法表示出电子的转移方向及数目)__ 。
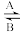 Fe3+的转化,在过程A中,Fe2+做
Fe3+的转化,在过程A中,Fe2+做(2)请按要求正确书写:
①“铁与硫酸铜溶液反应”(离子方程式):
②用CO还原Fe2O3(化学方程式):
(3)某一反应中有反应物和生成物的粒子共6种:SO32-、I2、H+、SO42-、I-、H2O,已知该反应中I2只发生如下过程:I2→I-,请回答:
①该反应的还原剂是
②反应过程中,每有1molI2发生反应,转移的电子数为
③写出该反应的离子方程式(用单线桥法表示出电子的转移方向及数目)
您最近一年使用:0次
名校
解题方法
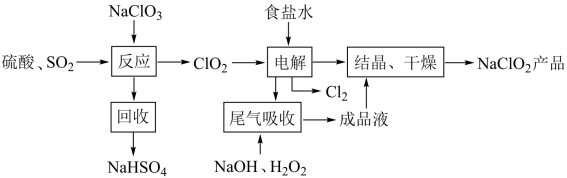
5 . NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下,回答下列问题
(1)NaClO2中Cl的化合价为______________________ .
(2)写出“反应”步骤中生成ClO2的化学方程式._______________________________ 。
(3)“电解”所用食盐水由粗盐水精制而成。粗盐精制时,为除去其中的Mg 2+和Ca 2+,要加入的试剂分别为_____________________ 、______________________ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应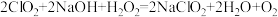 ,氧化剂与氧化产物的质量之比为
,氧化剂与氧化产物的质量之比为_________________ ,在标况下生成44.8LO2则转移电子的物质的量是____ .
(5)双氧水是中学常见的绿色化学试剂,既可以表现氧化性,又可以表现还原性。向双氧水中滴加酸性高锰酸钾溶液,产生气泡,紫红色褪去(已知Mn2+为无色),根据现象写出离子方程式._____________________________ 。

(1)NaClO2中Cl的化合价为
(2)写出“反应”步骤中生成ClO2的化学方程式.
(3)“电解”所用食盐水由粗盐水精制而成。粗盐精制时,为除去其中的Mg 2+和Ca 2+,要加入的试剂分别为
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应
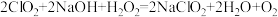 ,氧化剂与氧化产物的质量之比为
,氧化剂与氧化产物的质量之比为(5)双氧水是中学常见的绿色化学试剂,既可以表现氧化性,又可以表现还原性。向双氧水中滴加酸性高锰酸钾溶液,产生气泡,紫红色褪去(已知Mn2+为无色),根据现象写出离子方程式.
您最近一年使用:0次
名校
6 . 请按题目要求完成相应问题:
(1)K2FeO4在溶液中的电离方程式为_____________ 。
(2)除去杂质(括号的物质为杂质)Na2CO3溶液(NaHCO3) 离子方程式为_________________________ 。
(3)可溶性铁盐与足量氨水反应的离子方程式_______________________________________ 。
(4)氧化铁与强酸反应的离子反应方程式:_____________________________________ 。
(5)配平氧化还原反应:□C + □K2Cr2O7 + □H2SO4(稀) △□CO2↑+□K2SO4+□Cr2(SO4)3+□H2O___
(1)K2FeO4在溶液中的电离方程式为
(2)除去杂质(括号的物质为杂质)Na2CO3溶液(NaHCO3) 离子方程式为
(3)可溶性铁盐与足量氨水反应的离子方程式
(4)氧化铁与强酸反应的离子反应方程式:
(5)配平氧化还原反应:□C + □K2Cr2O7 + □H2SO4(稀) △□CO2↑+□K2SO4+□Cr2(SO4)3+□H2O
您最近一年使用:0次
名校
7 . (Ⅰ)如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
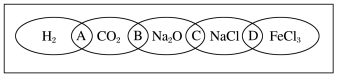
(1)请将分类依据代号填入相应的括号内:
( ) 两种物质都不是电解质
( ) 两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的图中某种物质M的溶液加热至呈红褐色。
①物质M的化学式为________________ 。
②证明有红褐色胶体生成的实验操作是____ 。
(Ⅱ)反应:
A.2F2+2H2O=4HF+O2↑; B.2Na+2H2O=2NaOH+H2↑;
C.CaO+H2O=Ca(OH)2; D.2H2O=2H2↑+O2↑。
其中水只是氧化剂的是______ (填序号),反应B中被氧化的元素名称是________ 。
(Ⅲ)反应:3Cu + 8HNO3 = 3Cu(NO3)2+2NO↑+4H2O, 硝酸在该反应中的作用是______ 还原剂与氧化剂的物质的量之比:__________

(1)请将分类依据代号填入相应的括号内:
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的图中某种物质M的溶液加热至呈红褐色。
①物质M的化学式为
②证明有红褐色胶体生成的实验操作是
(Ⅱ)反应:
A.2F2+2H2O=4HF+O2↑; B.2Na+2H2O=2NaOH+H2↑;
C.CaO+H2O=Ca(OH)2; D.2H2O=2H2↑+O2↑。
其中水只是氧化剂的是
(Ⅲ)反应:3Cu + 8HNO3 = 3Cu(NO3)2+2NO↑+4H2O, 硝酸在该反应中的作用是
您最近一年使用:0次
名校
解题方法
8 . 一种以辉铜矿(主要成分为Cu2S,含少量SiO2)为原料制备硝酸铜的工艺流程如图所示:
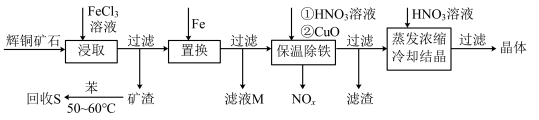
(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:___ 。
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl2是该反应的催化剂,该过程的反应原理可用化学方程式表示为:①Cu2S +2CuCl2=4CuCl+S;②___ 。
(3)“回收S”过程中温度控制在50~60℃之间,不宜过高的原因是___ 。
(4)向滤液M中加入(或通入)___ (填字母),可得到一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(5)“保温除铁”过程中,加入CuO的目的是__ ;“蒸发浓缩、冷却结晶”过程中,要用HNO3溶液调节溶液的pH,其理由_ 。
(6)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见图,转化时转移0.2mol电子,生成Cu2S___ mol。


(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl2是该反应的催化剂,该过程的反应原理可用化学方程式表示为:①Cu2S +2CuCl2=4CuCl+S;②
(3)“回收S”过程中温度控制在50~60℃之间,不宜过高的原因是
(4)向滤液M中加入(或通入)
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(5)“保温除铁”过程中,加入CuO的目的是
(6)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见图,转化时转移0.2mol电子,生成Cu2S

您最近一年使用:0次
2019-12-19更新
|
1285次组卷
|
10卷引用:宁夏石嘴山市第三中学2020届高三第五次模拟考试理综化学试题
宁夏石嘴山市第三中学2020届高三第五次模拟考试理综化学试题广东省六校联盟(深圳实验,广州二中,珠海一中,惠州一中,东莞中学,中山纪中)2020届高三第二次联考理综化学试题2020届高三《新题速递·化学》1月第01期(考点11-13)宁夏六盘山高级中学2020届高三下学期第二次模拟考试理综化学试题江西省南昌市第二中学2020届高三5月模拟理综化学试题江西省南昌市第二中学2021届高三上学期第四次考试理综化学试题江西省新余市第四中学2021届高三化学上学期第四次考试试题2022届陕西省宝鸡市陈仓区高考模拟检测(二)理综化学试题天津市河东区2022-2023学年高三上学期期中检测化学试题(已下线)第三章 金属及其化合物 第15练 金属材料 金属冶炼
名校
9 . (1)配平下列方程式(不需写出配平过程)
________ H2S+_______ HNO3 =________ S↓ +________ NO↑ +_______ H2O
________ S+________ KOH=________ K2S+________ K2SO3 +________ H2O
________ KMnO4+________ HCl(浓)=________ KCl+________ MnCl2+________ Cl2↑+________ H2O
(2)在酸性条件下,向含铬废水中加入FeSO4溶液,可将Cr2O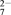 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为________________________ 。
(2)在酸性条件下,向含铬废水中加入FeSO4溶液,可将Cr2O
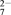 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为
您最近一年使用:0次
名校
10 . 工业上以废铜为原料经一系列化学反应可生产氯化亚铜(CuCl),其工艺流程如下图所示:
试依据如图转化回答下列问题:
(1)工业生产Cl2时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因是_______ 。
(2)还原过程中的产物为Na[CuCl2],试写出该反应的化学方程式:___________ 。
(3)合成结束后所得产品用酒精淋洗的目的是_______________ 。
(4)实验室中在CuCl2热溶液中通入SO2气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式:____ 。
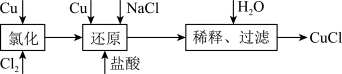
试依据如图转化回答下列问题:
(1)工业生产Cl2时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因是
(2)还原过程中的产物为Na[CuCl2],试写出该反应的化学方程式:
(3)合成结束后所得产品用酒精淋洗的目的是
(4)实验室中在CuCl2热溶液中通入SO2气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式:
您最近一年使用:0次



