1 . 从废旧磷酸铁锂电极材料(LiFePO4、导电石墨、铝箔)中回收锂的工艺流程如图,下列说法错误的是
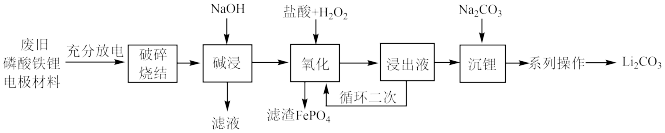
| A.旧电池拆解前进行充分放电是因为放电可使Li+在负极富集 |
| B.“氧化”时,H2O2可用KClO3代替 |
| C.“氧化”时发生的化学反应方程式为:2LiFePO4+H2O2+2HCl=2LiCl+2FePO4+2H2O |
| D.“系列操作”具体包括水浴加热、趁热过滤、洗涤、干燥 |
您最近一年使用:0次
2024-03-21更新
|
384次组卷
|
3卷引用:山东省济宁市2024届高三下学期一模考试化学试题
名校
解题方法
2 . 电池有铅蓄电池、燃料电池(如NO2NH3电池)、锂离子电池、Mg—次氯酸盐电池等,它们可以将化学能转化为电能。NH3、CH4、NaBH4都可用作燃料电池的燃料。CH4的燃烧热为890.3kJ•mol-1。电解则可以将电能转化为化学能,电解饱和NaCl溶液可以得到Cl2,用电解法可制备消毒剂高铁酸钠(Na2FeO4)。下列化学反应表示正确的是
A.铅蓄电池的正极反应:Pb-2e-+SO =PbSO4 =PbSO4 |
B.电解饱和NaCl溶液:2Na++2Cl- 2Na+Cl2↑ 2Na+Cl2↑ |
| C.CH4燃烧:CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3kJ•mol-1 |
D.一定条件下NO2与NH3的反应:6NO2+8NH3 7N2+12H2O 7N2+12H2O |
您最近一年使用:0次
2024-03-21更新
|
88次组卷
|
2卷引用:江苏省常州市联盟校2023-2024学年高二下学期3月阶段调研化学试题
名校
解题方法
3 . 镍及其化合物在工业上有广泛用途,以某地红土镍矿(主要成分NiO、MgO、 、
、 和铁的氧化物)为原料,采用酸溶法制取
和铁的氧化物)为原料,采用酸溶法制取 和
和 ,工业流程如图所示:
,工业流程如图所示:
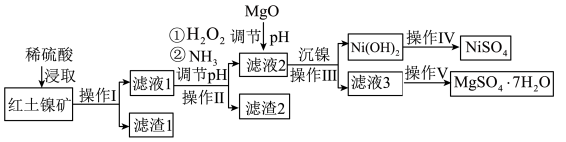
已知:①常温下, 易溶于水,
易溶于水, 和NiOOH不溶于水;
和NiOOH不溶于水;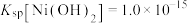 。
。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
回答下列问题:
(1)“滤液1”中加入 的作用是
的作用是___________ (用离子反应方程式表示)。
(2)操作Ⅱ为达到实验目的,由表中的数据判断通入 调节溶液pH的范围是
调节溶液pH的范围是___________ 。
(3)“滤液1”中是否存在 ,可用
,可用___________ 检验。
(4)“沉镍”中pH调为8.5,则滤液中 的浓度为
的浓度为___________  。
。
(5)操作V是___________ 、过滤、洗涤。
(6) 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为___________ 。
 、
、 和铁的氧化物)为原料,采用酸溶法制取
和铁的氧化物)为原料,采用酸溶法制取 和
和 ,工业流程如图所示:
,工业流程如图所示:
已知:①常温下,
 易溶于水,
易溶于水, 和NiOOH不溶于水;
和NiOOH不溶于水;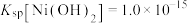 。
。②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
| 沉淀物 |  |  |  |  |  |
| 开始沉淀时的pH | 7.1 | 7.6 | 2.7 | 3.4 | 9.2 |
沉淀完全(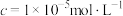 )时的pH )时的pH | 9.0 | 9.6 | 3.2 | 4.7 | 11.1 |
(1)“滤液1”中加入
 的作用是
的作用是(2)操作Ⅱ为达到实验目的,由表中的数据判断通入
 调节溶液pH的范围是
调节溶液pH的范围是(3)“滤液1”中是否存在
 ,可用
,可用(4)“沉镍”中pH调为8.5,则滤液中
 的浓度为
的浓度为 。
。(5)操作V是
(6)
 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
4 . 向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随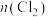 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: 与
与 的水溶液生成
的水溶液生成 和
和 ,
, 为强酸)下列说法中不正确的是
为强酸)下列说法中不正确的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随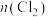 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: 与
与 的水溶液生成
的水溶液生成 和
和 ,
, 为强酸)下列说法中不正确的是
为强酸)下列说法中不正确的是
A.a点溶液中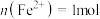 |
B.b点时已通入氯气的总体积为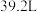 (标况) (标况) |
C.c点的总反应离子方程式为 |
D.d点溶液中阴离子的个数为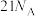 |
您最近一年使用:0次
2024-02-08更新
|
176次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一上学期1月期末化学试题
5 . V2O5-WO3/TiO2催化剂可以催化NH3脱除烟气中的NO,反应为:4NO(g) + 4NH3(g) + O2(g)=4N2(g) + 6H2O(g)  =-1632.4kJ·mol-1,工业上以石煤(主要成分为V2O3,含有少量SiO2、P2O5等杂质)为原料制备V2O5,主要经过“焙烧、水浸、除杂、沉钒、煅烧”等过程。
=-1632.4kJ·mol-1,工业上以石煤(主要成分为V2O3,含有少量SiO2、P2O5等杂质)为原料制备V2O5,主要经过“焙烧、水浸、除杂、沉钒、煅烧”等过程。
已知:NaVO3溶于水,NH4VO3难溶于水。
回答下列问题:
(1)向石煤中加纯碱,在通入空气的条件下焙烧, 转化为
转化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“沉钒”时加入NH4Cl析出NH4VO3,沉钒温度需控制在50℃左右,温度不能过高的原因为___________ ;在水溶液中VO 水解为H3VO4沉淀的离子方程式为
水解为H3VO4沉淀的离子方程式为___________ 。
(3)还原V2O5可制得VO2,下图为VO2的晶胞,该晶胞中钒的配位数为___________ 。

(4)催化剂的应用。将模拟烟气(含NO、NH3、N2、O2)以一定流速通过装有V2O5-WO3/TiO2催化剂的反应管,反应相同时间,测得NO的转化率随温度的变化如图所示,反应温度高于350℃,NO转化率下降的原因可能是___________ 。

(5)为测定回收所得V2O5样品的纯度,进行如下实验:称取2.000g样品,用稀硫酸溶解、定容得100mL (VO2)2SO4溶液,量取20.00mL溶液放入锥形瓶中,加入10.00mL 0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液24.00mL,滴定过程中发生如下反应:
VO +Fe2++2H+ = VO2++Fe3++H2O;MnO
+Fe2++2H+ = VO2++Fe3++H2O;MnO +5Fe2++ 8H+ = Mn2++5Fe3++4H2O。
+5Fe2++ 8H+ = Mn2++5Fe3++4H2O。
则V2O5样品的纯度为___________ 。(写出计算过程)
 =-1632.4kJ·mol-1,工业上以石煤(主要成分为V2O3,含有少量SiO2、P2O5等杂质)为原料制备V2O5,主要经过“焙烧、水浸、除杂、沉钒、煅烧”等过程。
=-1632.4kJ·mol-1,工业上以石煤(主要成分为V2O3,含有少量SiO2、P2O5等杂质)为原料制备V2O5,主要经过“焙烧、水浸、除杂、沉钒、煅烧”等过程。已知:NaVO3溶于水,NH4VO3难溶于水。
回答下列问题:
(1)向石煤中加纯碱,在通入空气的条件下焙烧,
 转化为
转化为 ,该反应的化学方程式为
,该反应的化学方程式为(2)“沉钒”时加入NH4Cl析出NH4VO3,沉钒温度需控制在50℃左右,温度不能过高的原因为
 水解为H3VO4沉淀的离子方程式为
水解为H3VO4沉淀的离子方程式为(3)还原V2O5可制得VO2,下图为VO2的晶胞,该晶胞中钒的配位数为

(4)催化剂的应用。将模拟烟气(含NO、NH3、N2、O2)以一定流速通过装有V2O5-WO3/TiO2催化剂的反应管,反应相同时间,测得NO的转化率随温度的变化如图所示,反应温度高于350℃,NO转化率下降的原因可能是

(5)为测定回收所得V2O5样品的纯度,进行如下实验:称取2.000g样品,用稀硫酸溶解、定容得100mL (VO2)2SO4溶液,量取20.00mL溶液放入锥形瓶中,加入10.00mL 0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液24.00mL,滴定过程中发生如下反应:
VO
 +Fe2++2H+ = VO2++Fe3++H2O;MnO
+Fe2++2H+ = VO2++Fe3++H2O;MnO +5Fe2++ 8H+ = Mn2++5Fe3++4H2O。
+5Fe2++ 8H+ = Mn2++5Fe3++4H2O。则V2O5样品的纯度为
您最近一年使用:0次
6 . 碱式氯化铜[Cu2(OH)2Cl2·3H2O]为绿色或墨绿色的结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中很稳定。
Ⅰ.模拟制备碱式氯化铜。
向CuCl2溶液中通入NH3,同时滴加稀盐酸,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分加持装置已省略)。
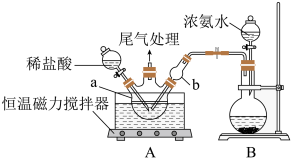
(1)碱式氯化铜中Cu(II)的核外电子排布式为___________ 。
(2)实验室利用装置B制备NH3,圆底烧瓶中盛放的固体药品可能是___________ (填名称)。
(3)反应过程中,需控制盐酸不能过量的原因是___________ 。
(4)反应结束后,将装置A中反应器内的混合物过滤,经提纯得产品无水碱式氯化铜,从滤液中还可以获得的副产品是___________ (填化学式)。
(5)碱式氯化铜[Cu2(OH)2Cl2·3H2O]也可以通过在40℃~50℃,向CuCl悬浊液中持续通空气制得,该反应的化学方程式为___________ 。
Ⅱ.采用沉淀滴定法测定碱式氯化铜中氯含量
(6)请补充完整测定氯的实验过程:取一定量碱式氯化铜固体,溶于稀硝酸,配制成一定体积待测液,准确量取25mL待测液于锥形瓶中,边振荡边向锥形瓶中滴加0.010 mol·L-1AgNO3溶液,直至静置后向上层清液中继续滴加0.010 mol·L-1AgNO3溶液无浑浊产生,记录消耗AgNO3溶液的体积V1,___________ ,重复上述实验2~3次。
已知:①Ag+ + SCN— = AgSCN↓(白色沉淀);②聚乙烯醇可以覆盖在AgCl表面,阻止AgCl转化为AgSCN。[须使用的实验试剂:0.010 mol·L-1NH4SCN标准溶液、Fe(NO3)3溶液、聚乙烯醇]
Ⅰ.模拟制备碱式氯化铜。
向CuCl2溶液中通入NH3,同时滴加稀盐酸,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分加持装置已省略)。

(1)碱式氯化铜中Cu(II)的核外电子排布式为
(2)实验室利用装置B制备NH3,圆底烧瓶中盛放的固体药品可能是
(3)反应过程中,需控制盐酸不能过量的原因是
(4)反应结束后,将装置A中反应器内的混合物过滤,经提纯得产品无水碱式氯化铜,从滤液中还可以获得的副产品是
(5)碱式氯化铜[Cu2(OH)2Cl2·3H2O]也可以通过在40℃~50℃,向CuCl悬浊液中持续通空气制得,该反应的化学方程式为
Ⅱ.采用沉淀滴定法测定碱式氯化铜中氯含量
(6)请补充完整测定氯的实验过程:取一定量碱式氯化铜固体,溶于稀硝酸,配制成一定体积待测液,准确量取25mL待测液于锥形瓶中,边振荡边向锥形瓶中滴加0.010 mol·L-1AgNO3溶液,直至静置后向上层清液中继续滴加0.010 mol·L-1AgNO3溶液无浑浊产生,记录消耗AgNO3溶液的体积V1,
已知:①Ag+ + SCN— = AgSCN↓(白色沉淀);②聚乙烯醇可以覆盖在AgCl表面,阻止AgCl转化为AgSCN。[须使用的实验试剂:0.010 mol·L-1NH4SCN标准溶液、Fe(NO3)3溶液、聚乙烯醇]
您最近一年使用:0次
7 .  在工业上有广泛的用途。以硫铁矿(主要成分为
在工业上有广泛的用途。以硫铁矿(主要成分为 )为原料制备
)为原料制备 的工艺流程如下图:
的工艺流程如下图:_______ (写出一种)。
(2)“操作”在实验室的名称为_______ ,需用到的玻璃仪器是_______ 、玻璃棒和烧杯。
(3)黄铁矿焙烧后得到的主要固体为 ,写出“焙烧”的化学方程式为
,写出“焙烧”的化学方程式为_______ 。
(4)“……”表示的操作为在_______ 气流中蒸发浓缩、_______ 、过滤。
(5)为防治 引起的污染,某工厂设计了新的治污方法,同时可得到化工产品
引起的污染,某工厂设计了新的治污方法,同时可得到化工产品 。该工艺流程如图所示,过程中起催化作用的物质是
。该工艺流程如图所示,过程中起催化作用的物质是_______ ,生成化工产品 的化学方程式为
的化学方程式为_______ 。 生产硫酸。用
生产硫酸。用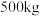 含
含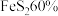 的硫铁矿,生产过程中硫损失
的硫铁矿,生产过程中硫损失 ,则可得
,则可得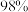 的硫酸
的硫酸_______  。
。
 在工业上有广泛的用途。以硫铁矿(主要成分为
在工业上有广泛的用途。以硫铁矿(主要成分为 )为原料制备
)为原料制备 的工艺流程如下图:
的工艺流程如下图: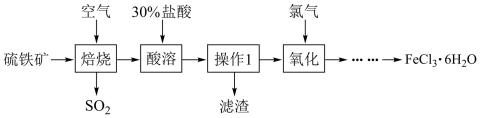
(2)“操作”在实验室的名称为
(3)黄铁矿焙烧后得到的主要固体为
 ,写出“焙烧”的化学方程式为
,写出“焙烧”的化学方程式为(4)“……”表示的操作为在
(5)为防治
 引起的污染,某工厂设计了新的治污方法,同时可得到化工产品
引起的污染,某工厂设计了新的治污方法,同时可得到化工产品 。该工艺流程如图所示,过程中起催化作用的物质是
。该工艺流程如图所示,过程中起催化作用的物质是 的化学方程式为
的化学方程式为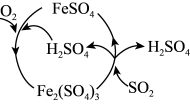
 生产硫酸。用
生产硫酸。用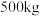 含
含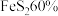 的硫铁矿,生产过程中硫损失
的硫铁矿,生产过程中硫损失 ,则可得
,则可得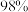 的硫酸
的硫酸 。
。
您最近一年使用:0次
名校
8 . 工业生产中除去电石渣浆(含 )中的
)中的 并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
 )中的
)中的 并制取硫酸盐的一种常用流程如图所示。下列说法正确的是
并制取硫酸盐的一种常用流程如图所示。下列说法正确的是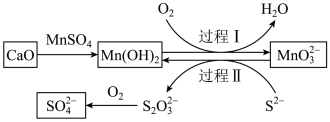
A.碱性条件下,氧化性: |
B.过程Ⅱ中,反应的离子方程式为 |
C.将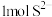 转化为 转化为 理论上需要 理论上需要 的体积为 的体积为 (标准状况) (标准状况) |
| D.该过程中涉及的化学反应均是氧化还原反应 |
您最近一年使用:0次
2024-01-14更新
|
949次组卷
|
3卷引用:云南师范大学附属中学2023-2024学年高一上学期1月教学测评期末化学试题
9 . 近日,中科院上海硅酸盐研究所施剑林团队报道了MnOOH催化谷胱甘肽自氧化产生活性氧。某小组以菱锰矿(主要成分为 ,含少量
,含少量 、FeO、CoO、
、FeO、CoO、 、
、 等)为原料制备高纯度MnOOH,流程如下:
等)为原料制备高纯度MnOOH,流程如下:
②几种金属离子沉淀的pH如表所示:
下列叙述正确的是
 ,含少量
,含少量 、FeO、CoO、
、FeO、CoO、 、
、 等)为原料制备高纯度MnOOH,流程如下:
等)为原料制备高纯度MnOOH,流程如下: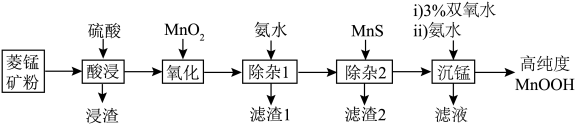
②几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |  |
| 开始沉淀的pH | 2.7 | 7.6 | 4.0 | 7.6 | 8.1 |
| 完全沉淀的pH | 3.7 | 9.6 | 5.2 | 9.2 | 10.1 |
A.滤渣1的成分是 和 和 |
B.“氧化”反应的离子方程式为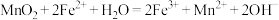 |
C.“除杂2”的原理是 |
D.双氧水氧化 ,滤液一定显酸性 ,滤液一定显酸性 |
您最近一年使用:0次
名校
10 . 大连理工大学课题组通过CuO/ 催化,使NO-CO-
催化,使NO-CO- 反应体系在温和条件下产生
反应体系在温和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
,为NO和CO的烟气处理提供了新的途径,其相关的反应为: (未配平),
(未配平), 是阿伏加德罗常数的值,下列有关说法正确的是
是阿伏加德罗常数的值,下列有关说法正确的是
 催化,使NO-CO-
催化,使NO-CO- 反应体系在温和条件下产生
反应体系在温和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
,为NO和CO的烟气处理提供了新的途径,其相关的反应为: (未配平),
(未配平), 是阿伏加德罗常数的值,下列有关说法正确的是
是阿伏加德罗常数的值,下列有关说法正确的是A.标准状况下,1.12L NO中含有电子数为1.5 |
B.将 个 个 溶于100mL水中,所得溶液的质量分数约为29.9% 溶于100mL水中,所得溶液的质量分数约为29.9% |
C.生成22g  能消除NO的数目为0.2 能消除NO的数目为0.2 |
D.若NO和CO混合气体的平均相对分子质量为29,则含有CO的数目为0.5 |
您最近一年使用:0次
2024-03-13更新
|
302次组卷
|
4卷引用:山东省青岛第二中学2023-2024学年高一上学期第二次月考化学试卷



