1 . 现有下列物质(括号内为对应物质的主要成分):a.熔融NaOH;b.医用酒精;c.蔗糖晶体;d.加碘盐(NaCl和KIO3);e.“84”消毒液(NaClO);f.小苏打(NaHCO3);g.洁厕灵(HCl),回答下列问题:
(1)上述状态下的物质中,属于电解质且能导电的是_______ (填字母,下同);d和f均为厨房中的常用物质,可用于区分两者的物质是________ 。
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:________ 。
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:___________ ;该反应中被氧化的Ⅰ原子与被还原的Ⅰ原子的个数之比为___________ 。
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:_____ ,__NaClO2+__NaHSO4=___ClO2+___NaCl+__Na2SO4+____H2O;若每片泡腾片中NaClO2的质量分数≥17%为合格品,上述所得ClO2溶液的物质的量浓度为0.002mol/L,则所用泡腾片____ (填“属于”或“不属于”)合格品。
(1)上述状态下的物质中,属于电解质且能导电的是
(2)生活中若将“84”消毒液和洁厕灵混合易产生黄绿色有毒气体,写出该反应的离子方程式:
(3)碘酸钾(KIO3)可作为食盐中的补碘剂。一种制备KIO3的方法是将I2与KOH溶液共热,生成KIO3、H2O和另—种化合物,写出该反应的化学方程式:
(4)二氧化氯泡腾片(有效成分为NaClO2和NaHSO4)也是一种用途广泛的消毒用品,将1片(规格为1g/片)二氧化氯泡腾片溶于1L水中,得到ClO2溶液(假设ClO2全部溶于水且反应后溶液体积仍为1L)。补全生成ClO2的化学方程式:
您最近一年使用:0次
2 . 通常利用反应: 定性检验
定性检验 ,关于该反应的下列说法中,
,关于该反应的下列说法中,不正确 的是
 定性检验
定性检验 ,关于该反应的下列说法中,
,关于该反应的下列说法中,A. 被氧化 被氧化 | B.每消耗1mol ,转移2mol ,转移2mol |
C. 和 和 的物质的量之比为5∶2 的物质的量之比为5∶2 | D.在该反应的条件下,氧化性: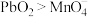 |
您最近一年使用:0次
2023-01-05更新
|
369次组卷
|
4卷引用:黑龙江省双鸭山市第一中学2022-2023学年高一下学期开学考试化学试题
名校
3 . 次磷酸(H3PO2)是一元中强酸,次磷酸钠(NaH2PO2)广泛应用于化学镀镍,次磷酸钠的生产与镀镍过程如图所示。下列有关说法正确的是


A.Ni2+价电子的轨道表示式为 |
| B.“碱溶”时氧化剂与还原剂的物质的量之比为3:1 |
C.PH3、PO 中P的杂化方式相同,键角PO 中P的杂化方式相同,键角PO >PH3 >PH3 |
D.次磷酸铵与足量氢氧化钠共热,发生反应NH +H2PO +H2PO +3OH- +3OH- NH3↑+3H2O+PO NH3↑+3H2O+PO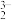 |
您最近一年使用:0次
2022-10-08更新
|
1439次组卷
|
8卷引用:黑龙江省绥化市第一中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
4 . A、B、C、D四种物质之间的转化关系如图所示(部分产物略去),根据所学知识回答下列问题:

(1)若A为NaAlO2溶液,写出A与过量B反应的离子方程式____ 。
(2)若A为Fe,B为稀HNO3,则反应①(还原产物为NO)中氧化剂与还原剂的物质的量之比为____ ,稀硝酸在反应过程中除了起氧化剂的作用外,还有____ 的作用。
(3)若A为Cl2,B为NH3,当NH3过量时,则二者相遇有白烟生成,写出反应①的化学方程式:_____ 。
(4)若A为1L0.1mol·L-1NaOH溶液,B为SO2,当向A中通入0.07molSO2气体时,溶液中的溶质为_____ (填化学式,下同)、____ ,物质的量分别为____ 、___ 。

(1)若A为NaAlO2溶液,写出A与过量B反应的离子方程式
(2)若A为Fe,B为稀HNO3,则反应①(还原产物为NO)中氧化剂与还原剂的物质的量之比为
(3)若A为Cl2,B为NH3,当NH3过量时,则二者相遇有白烟生成,写出反应①的化学方程式:
(4)若A为1L0.1mol·L-1NaOH溶液,B为SO2,当向A中通入0.07molSO2气体时,溶液中的溶质为
您最近一年使用:0次
2022-07-06更新
|
322次组卷
|
2卷引用:黑龙江省牡丹江市第二高级中学2023-2024学年高三上学期第三次阶段性考试化学试题
5 . 一种利用辉铋矿(主要成分是 ,以及少量
,以及少量 、
、 3、
3、 等杂质)为原料制备
等杂质)为原料制备 (难溶于水)的流程如图所示:
(难溶于水)的流程如图所示:

(1)“浸出”时常常需要加热或搅拌,其原因是___________ ;写出“浸出”时 反应的化学方程式:
反应的化学方程式:___________ ( 的化合价不发生变化)。
的化合价不发生变化)。
(2)“氧化”的目的是___________ (用离子方程式表示)。
(3)下列实验仪器与“操作a”相对应的是___________(填字母)。
(4)为提高 的产率,“调pH”时可加入
的产率,“调pH”时可加入___________ (填化学式)。
(5)写出“制备”反应的离子方程式:___________ 。
(6) 氧化性较强,在酸性条件下,可将
氧化性较强,在酸性条件下,可将 氧化为
氧化为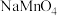 。若生成
。若生成
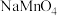 ,则理论上消耗
,则理论上消耗___________ 
 (还原产物为
(还原产物为 )。
)。
 ,以及少量
,以及少量 、
、 3、
3、 等杂质)为原料制备
等杂质)为原料制备 (难溶于水)的流程如图所示:
(难溶于水)的流程如图所示:
(1)“浸出”时常常需要加热或搅拌,其原因是
 反应的化学方程式:
反应的化学方程式: 的化合价不发生变化)。
的化合价不发生变化)。(2)“氧化”的目的是
(3)下列实验仪器与“操作a”相对应的是___________(填字母)。
A. | B. | C. | D. |
 的产率,“调pH”时可加入
的产率,“调pH”时可加入(5)写出“制备”反应的离子方程式:
(6)
 氧化性较强,在酸性条件下,可将
氧化性较强,在酸性条件下,可将 氧化为
氧化为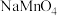 。若生成
。若生成
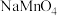 ,则理论上消耗
,则理论上消耗
 (还原产物为
(还原产物为 )。
)。
您最近一年使用:0次



