名校
解题方法
1 . 向KIO3的溶液中,通入H2S发生反应后,生产碘单质、硫酸钾、硫酸和水,在此反应中氧化剂和还原剂的数量比为:
| A.4:5 | B.8:5 | C.5:8 | D.5:4 |
您最近一年使用:0次
2 . 黄铁矿与焦炭充分混合( 与C的质量比为
与C的质量比为 ),在有限量的空气中缓慢燃烧,结果可得到硫磺,过程中可能发生的反应之一为:
),在有限量的空气中缓慢燃烧,结果可得到硫磺,过程中可能发生的反应之一为: 。下列有关说法不正确的是。
。下列有关说法不正确的是。
 与C的质量比为
与C的质量比为 ),在有限量的空气中缓慢燃烧,结果可得到硫磺,过程中可能发生的反应之一为:
),在有限量的空气中缓慢燃烧,结果可得到硫磺,过程中可能发生的反应之一为: 。下列有关说法不正确的是。
。下列有关说法不正确的是。A. 晶体中存在非极性共价键 晶体中存在非极性共价键 |
B.当有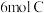 参加反应时,共转移 参加反应时,共转移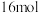 电子 电子 |
C. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
D.当有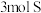 生成时,有 生成时,有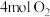 被焦炭还原 被焦炭还原 |
您最近一年使用:0次
2023-12-06更新
|
215次组卷
|
5卷引用:湖北省沙市中学2024届高三下学期模拟预测化学试题
湖北省沙市中学2024届高三下学期模拟预测化学试题浙江省金丽衢十二校2023-2024学年高三上学期联考模拟预测化学试题(已下线)专题01 基本概念(5大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)浙江省四校联考2023-2024学年高二下学期3月月考化学试题(已下线)压轴题02 氧化还原反应的概念及规律(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
3 . 实验室用 等作原料制取少量
等作原料制取少量 的实验流程如下:
的实验流程如下:
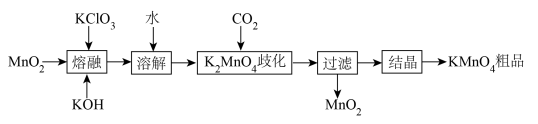
下列说法正确的是
 等作原料制取少量
等作原料制取少量 的实验流程如下:
的实验流程如下:
下列说法正确的是
A.“熔融”时应先将 和 和 混合加热一段时间后再加入 混合加热一段时间后再加入 |
B.“溶解”后的溶液中存在大量的 |
C.“ 歧化”时氧化剂与还原剂的物质的量之比为 歧化”时氧化剂与还原剂的物质的量之比为 |
D.流程中可以循环使用的物质是 |
您最近一年使用:0次
2023-06-29更新
|
1387次组卷
|
5卷引用:湖北省宜昌市长阳土家族自治县第一高级中学2023-2024学年高一上学期11月期中化学试题
湖北省宜昌市长阳土家族自治县第一高级中学2023-2024学年高一上学期11月期中化学试题江苏省南通市2022-2023学年高一下学期期末质量监测化学试题(已下线)专题突破卷13 化学实验基础(二)-2024年高考化学一轮复习考点通关卷(新教材新高考)浙江省金华第一中学2023-2024学年高一上学期11月期中考试化学试题广西钦州市第四中学2023-2024学年高一上学期9月考试化学试卷
名校
4 .  去除酸性废水中
去除酸性废水中 的反应机理如图所示(图中“HS·”为自由基)。下列说法错误的是
的反应机理如图所示(图中“HS·”为自由基)。下列说法错误的是
 去除酸性废水中
去除酸性废水中 的反应机理如图所示(图中“HS·”为自由基)。下列说法错误的是
的反应机理如图所示(图中“HS·”为自由基)。下列说法错误的是
A.X的化学式为 |
| B.HS·反应活性较强,不能稳定存在 |
| C.步骤III反应中氧化剂与还原剂的物质的量比为8∶1 |
D.步骤IV除砷的方程式为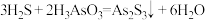 |
您最近一年使用:0次
2023-04-26更新
|
611次组卷
|
4卷引用:湖北省武汉市洪山高级中学2024届高三下学期第 2次模拟考试化学试卷
解题方法
5 . 含有同一种元素的物质A、B、C、D、E存在如图转化关系(某些产物及反应条件已省略)。

Ⅰ.若A在常温下呈固态
请回答下列问题:
(1)物质C、E均能使溴水褪色请写出C的化学式_______ ,写出E与溴水反应的离子方程式_______ 。
(2)通常状况下A的颜色是_______ ;上述转化⑤⑥中一定不是氧化还原反应的是_______ (填序号)。
Ⅱ.若A在常温是气态
(3)请写出A的电子式_______ 。
(4)反应④的实验现象是产生红棕色气体,请写出该反应的化学方程式_______ 。
(5)气体B溶于水,该反应中氧化剂和还原剂物质的量之比是_______ 。
(6)D溶液能与金属单质反应,该反应体现了物质D的_______ 。
a.氧化性 b.还原性 c.酸性

Ⅰ.若A在常温下呈固态
请回答下列问题:
(1)物质C、E均能使溴水褪色请写出C的化学式
(2)通常状况下A的颜色是
Ⅱ.若A在常温是气态
(3)请写出A的电子式
(4)反应④的实验现象是产生红棕色气体,请写出该反应的化学方程式
(5)气体B溶于水,该反应中氧化剂和还原剂物质的量之比是
(6)D溶液能与金属单质反应,该反应体现了物质D的
a.氧化性 b.还原性 c.酸性
您最近一年使用:0次
名校
解题方法
6 . 按要求填空。
(1)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体 ,请写出该过程的离子方程式:
,请写出该过程的离子方程式:_______ 。
(2)某无色溶液中的溶质可能由下列离子组成: 、
、 、
、 、
、 、
、 、
、 、
、 ,某同学为检验其成分,进行了如下实验:
,某同学为检验其成分,进行了如下实验:
①向适量原溶液中加入过量的稀盐酸,有无色气体a和无色溶液b生成;
②向无色溶液b中加入过量的 溶液,有白色沉淀c生成,过滤,得滤液d;
溶液,有白色沉淀c生成,过滤,得滤液d;
③取少量滤液d,加入过量的稀硝酸酸化,再滴加 溶液,有白色沉淀e生成。
溶液,有白色沉淀e生成。
依据以上实验可以推断,原溶液中一定含有大量的_______ (用离子符号表示,下同);可能含有_______ 。
(3) 常用作补铁剂,在酸性(常用稀硫酸酸化)条件下,
常用作补铁剂,在酸性(常用稀硫酸酸化)条件下, 能将
能将 中
中 价的Cr转化为
价的Cr转化为 价的Cr。则反应中氧化剂与还原剂的物质的量之比为
价的Cr。则反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)某一反应体系中反应物和生成物共有六种物质: 、
、 、
、 、NaCl、NaOH、
、NaCl、NaOH、 ,已知该反应中
,已知该反应中 只发生如下过程:
只发生如下过程: ,则该反应的化学方程式为
,则该反应的化学方程式为_______ 。
(5)向 和
和 混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中
混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 的物质的量与所加盐酸体积之间的关系如图所示。
的物质的量与所加盐酸体积之间的关系如图所示。

①盐酸的物质的量浓度为_______  。
。
②当滴入盐酸的体积为12.5mL时,溶液中 为
为_______ 。
(1)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体
 ,请写出该过程的离子方程式:
,请写出该过程的离子方程式:(2)某无色溶液中的溶质可能由下列离子组成:
 、
、 、
、 、
、 、
、 、
、 、
、 ,某同学为检验其成分,进行了如下实验:
,某同学为检验其成分,进行了如下实验:①向适量原溶液中加入过量的稀盐酸,有无色气体a和无色溶液b生成;
②向无色溶液b中加入过量的
 溶液,有白色沉淀c生成,过滤,得滤液d;
溶液,有白色沉淀c生成,过滤,得滤液d;③取少量滤液d,加入过量的稀硝酸酸化,再滴加
 溶液,有白色沉淀e生成。
溶液,有白色沉淀e生成。依据以上实验可以推断,原溶液中一定含有大量的
(3)
 常用作补铁剂,在酸性(常用稀硫酸酸化)条件下,
常用作补铁剂,在酸性(常用稀硫酸酸化)条件下, 能将
能将 中
中 价的Cr转化为
价的Cr转化为 价的Cr。则反应中氧化剂与还原剂的物质的量之比为
价的Cr。则反应中氧化剂与还原剂的物质的量之比为(4)某一反应体系中反应物和生成物共有六种物质:
 、
、 、
、 、NaCl、NaOH、
、NaCl、NaOH、 ,已知该反应中
,已知该反应中 只发生如下过程:
只发生如下过程: ,则该反应的化学方程式为
,则该反应的化学方程式为(5)向
 和
和 混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中
混合溶液中缓慢滴加一定浓度的盐酸,测得溶液中 的物质的量与所加盐酸体积之间的关系如图所示。
的物质的量与所加盐酸体积之间的关系如图所示。
①盐酸的物质的量浓度为
 。
。②当滴入盐酸的体积为12.5mL时,溶液中
 为
为
您最近一年使用:0次
2023-01-31更新
|
419次组卷
|
2卷引用:湖北省武汉市部分重点中学四校联考2022-2023学年高一上学期期末考试化学试卷
解题方法
7 . 铬是一种具有战略意义的金瘺,工业上以铬铁矿[主要成分是 ]为原料冶炼铬的某个流程中发生的反应为
]为原料冶炼铬的某个流程中发生的反应为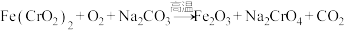 (未配平),已知Cr有+3、+6两种价态。下列关于该反应的说法中正确的是
(未配平),已知Cr有+3、+6两种价态。下列关于该反应的说法中正确的是
 ]为原料冶炼铬的某个流程中发生的反应为
]为原料冶炼铬的某个流程中发生的反应为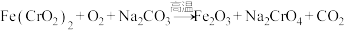 (未配平),已知Cr有+3、+6两种价态。下列关于该反应的说法中正确的是
(未配平),已知Cr有+3、+6两种价态。下列关于该反应的说法中正确的是A. 中Fe为+3价 中Fe为+3价 |
B.每转移7 mol  ,生成8.8 g ,生成8.8 g  |
| C.氧化剂与还原剂的物质的量之比为2∶3 |
D.每消耗1.4 mol  ,被氧化的Cr原子的物质的量为1.6 mol ,被氧化的Cr原子的物质的量为1.6 mol |
您最近一年使用:0次
2022-12-19更新
|
109次组卷
|
2卷引用:湖北省恩施州高中教育联盟2022-2023学年高二上学期期中考试化学试题
解题方法
8 . 近几年,我国汽车工业得到了飞速发展,新能源汽车走在世界前列。回答下列问题:
(1)庚烷是汽车燃料(汽油)的主要成分之一,1mol气态正庚烷(以 表示)完全燃烧生成二氧化碳和水蒸气放出4817kJ热量,该反应的热化学议程式为
表示)完全燃烧生成二氧化碳和水蒸气放出4817kJ热量,该反应的热化学议程式为_______ 。
(2)三种汽车燃料燃烧时的能量变化如下图所示。

根据图示,你认为_______ 作为汽车燃料最好,简述理由_______ (至少回答两点)
(3)在汽车排气管里安装三元催化剂,可有效降低汽车尾气中的CO和NO等污染气体的含量,写出汽车尾气中NO和CO反应的化学方程式:_______ 。
(4)汽车发生剧烈碰撞时,会引发汽车安全气囊中的物质迅速发生反应: ,气囊中产生大量的气体,从而保护驾车人员的安全。
,气囊中产生大量的气体,从而保护驾车人员的安全。
①反应中,每生成16molN2,转移的电子数为_______ 。
②反应中,氧化产物与还原产物的物质的量之比为_______ 。
(5)不使用汽油或柴油作为能源的汽车统称新能源汽车,一种新能源汽车使用的锂电池工作原理如下图,电池反应为: 。
。

①充电时,电解质溶液中的锂离子向电极_______ (填写“M”“N”)方向移动
②若放电时外电路有2NA电子转移,则理论上电极M的质量_______ (填序号)。
A.增重14g B.不变 C.减重14g D.无法确定
(1)庚烷是汽车燃料(汽油)的主要成分之一,1mol气态正庚烷(以
 表示)完全燃烧生成二氧化碳和水蒸气放出4817kJ热量,该反应的热化学议程式为
表示)完全燃烧生成二氧化碳和水蒸气放出4817kJ热量,该反应的热化学议程式为(2)三种汽车燃料燃烧时的能量变化如下图所示。

根据图示,你认为
(3)在汽车排气管里安装三元催化剂,可有效降低汽车尾气中的CO和NO等污染气体的含量,写出汽车尾气中NO和CO反应的化学方程式:
(4)汽车发生剧烈碰撞时,会引发汽车安全气囊中的物质迅速发生反应:
 ,气囊中产生大量的气体,从而保护驾车人员的安全。
,气囊中产生大量的气体,从而保护驾车人员的安全。①反应中,每生成16molN2,转移的电子数为
②反应中,氧化产物与还原产物的物质的量之比为
(5)不使用汽油或柴油作为能源的汽车统称新能源汽车,一种新能源汽车使用的锂电池工作原理如下图,电池反应为:
 。
。
①充电时,电解质溶液中的锂离子向电极
②若放电时外电路有2NA电子转移,则理论上电极M的质量
A.增重14g B.不变 C.减重14g D.无法确定
您最近一年使用:0次
9 . 已知反应:
①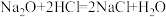
②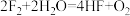
③
④
⑤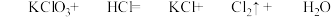
(1)上述反应中,属于置换反应的是_______ (填序号,下同);同一元素之间发生氧化还原的是_______ 。
(2)反应②中氧化剂是_______ (填化学式,下同);反应③中氧化产物是_______ 。
(3)在反应④中,每生成1个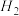 分子时,转移的电子数为
分子时,转移的电子数为_______ 。
(4)配平反应⑤并用双线桥法标出反应⑤中电子转移的方向和数目_______ 。
(5)反应⑤中氧化剂与还原剂的质量之比为_______ (填最简整数比)。
(6)已知有下列两个反应:①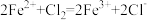 ;②
;② ,
, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(7)下列物质中能使酸性 溶液褪色(转化为
溶液褪色(转化为 而褪色)的是
而褪色)的是_______ (填字母)。
a.臭碱(Na2S) b.小苏打(NaHCO3) c.水玻璃( 溶液)
溶液)
①
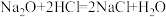
②
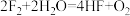
③

④

⑤
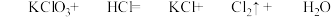
(1)上述反应中,属于置换反应的是
(2)反应②中氧化剂是
(3)在反应④中,每生成1个
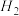 分子时,转移的电子数为
分子时,转移的电子数为(4)配平反应⑤并用双线桥法标出反应⑤中电子转移的方向和数目
(5)反应⑤中氧化剂与还原剂的质量之比为
(6)已知有下列两个反应:①
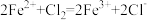 ;②
;② ,
, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(7)下列物质中能使酸性
 溶液褪色(转化为
溶液褪色(转化为 而褪色)的是
而褪色)的是a.臭碱(Na2S) b.小苏打(NaHCO3) c.水玻璃(
 溶液)
溶液)
您最近一年使用:0次
10 . “有效氯”是指每克含氯消毒剂相当于多少克 的氧化能力。
的氧化能力。 (沸点11℃)是国际公认的绿色消毒剂,国外采用硫磺悬浊液与氯酸钠溶液反应制备,其反应原理为
(沸点11℃)是国际公认的绿色消毒剂,国外采用硫磺悬浊液与氯酸钠溶液反应制备,其反应原理为 。下列说法中正确的是
。下列说法中正确的是
 的氧化能力。
的氧化能力。 (沸点11℃)是国际公认的绿色消毒剂,国外采用硫磺悬浊液与氯酸钠溶液反应制备,其反应原理为
(沸点11℃)是国际公认的绿色消毒剂,国外采用硫磺悬浊液与氯酸钠溶液反应制备,其反应原理为 。下列说法中正确的是
。下列说法中正确的是A.上述反应中,氧化剂是 | B.每生成 则有 则有 被氧化 被氧化 |
C. 标准状况下的体积约为 标准状况下的体积约为 | D.相同条件下 的“有效氯”约为 的“有效氯”约为 |
您最近一年使用:0次



