名校
1 . 下列关于氨气的应用及性质说法正确的是
A.氨燃料动力集装箱船中氨气燃烧的化学方程式: |
B.足量的氨气和氯气反应,氧化剂和还原剂的物质的量之比为 |
C.氨气的中心原子采取 杂化,且氮原子提供空轨道与 杂化,且氮原子提供空轨道与 形成配位键 形成配位键 |
D.氨气可用于制备高能分子磷酰三叠氮,结构简式为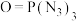 ,其分解产物 ,其分解产物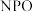 的电子式为 的电子式为 |
您最近一年使用:0次
2024-05-12更新
|
120次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
解题方法
2 . 汽车排放的尾气中一般含有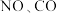 气体,两者均有毒,在催化剂作用下可以反应,生成两种无毒的气体
气体,两者均有毒,在催化剂作用下可以反应,生成两种无毒的气体 和
和 ,反应的化学方程式为
,反应的化学方程式为 (未配平)。回答下列问题:
(未配平)。回答下列问题:
(1)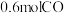 中所含原子数与
中所含原子数与_______  中所含原子数相等。
中所含原子数相等。
(2)该反应中氧化剂为_______ (填化学式),氧化产物与还原产物的质量之比为_______ (填最简整数比)。
(3)配平反应的化学方程式并用双线桥法分析反应中的电子转移:_______ 。
(4)已知:分压 总压
总压 该组分物质的量分数。标准状况
该组分物质的量分数。标准状况 下,由
下,由 和
和 组成的混合气体平均摩尔质量为
组成的混合气体平均摩尔质量为 ,则该混合气体中
,则该混合气体中 和
和 的体积比为
的体积比为_______ ,该体系中 的分压为
的分压为_______ kPa(写表达式,不需计算)。
(5)氧化还原反应可以分解成两个半反应,如 的半反应分别为
的半反应分别为还原反应  和
和氧化反应  。工业上用
。工业上用 溶液吸收
溶液吸收 尾气的离子方程式为
尾气的离子方程式为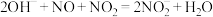 。该反应的氧化反应为
。该反应的氧化反应为_______ 。
(6)呼吸面罩中含有一种淡黄色固体,可以吸收 重新放出
重新放出 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
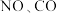 气体,两者均有毒,在催化剂作用下可以反应,生成两种无毒的气体
气体,两者均有毒,在催化剂作用下可以反应,生成两种无毒的气体 和
和 ,反应的化学方程式为
,反应的化学方程式为 (未配平)。回答下列问题:
(未配平)。回答下列问题:(1)
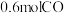 中所含原子数与
中所含原子数与 中所含原子数相等。
中所含原子数相等。(2)该反应中氧化剂为
(3)配平反应的化学方程式并用双线桥法分析反应中的电子转移:
(4)已知:分压
 总压
总压 该组分物质的量分数。标准状况
该组分物质的量分数。标准状况 下,由
下,由 和
和 组成的混合气体平均摩尔质量为
组成的混合气体平均摩尔质量为 ,则该混合气体中
,则该混合气体中 和
和 的体积比为
的体积比为 的分压为
的分压为(5)氧化还原反应可以分解成两个半反应,如
 的半反应分别为
的半反应分别为 和
和 。工业上用
。工业上用 溶液吸收
溶液吸收 尾气的离子方程式为
尾气的离子方程式为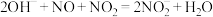 。该反应的氧化反应为
。该反应的氧化反应为(6)呼吸面罩中含有一种淡黄色固体,可以吸收
 重新放出
重新放出 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
3 . 已知 某溶液(该溶液称为
某溶液(该溶液称为 )中仅含有两种溶质
)中仅含有两种溶质 和
和 ,且物质的量浓度依次为
,且物质的量浓度依次为 和
和 ,向该溶液中投入
,向该溶液中投入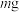 铁粉恰好完全反应,释放出的气体体积为
铁粉恰好完全反应,释放出的气体体积为 。下列叙述正确的是
。下列叙述正确的是
 某溶液(该溶液称为
某溶液(该溶液称为 )中仅含有两种溶质
)中仅含有两种溶质 和
和 ,且物质的量浓度依次为
,且物质的量浓度依次为 和
和 ,向该溶液中投入
,向该溶液中投入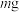 铁粉恰好完全反应,释放出的气体体积为
铁粉恰好完全反应,释放出的气体体积为 。下列叙述正确的是
。下列叙述正确的是A. 中 中 的物质的量为 的物质的量为 |
B.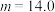 |
C.反应后所得溶液中氧化产物与还原产物的物质的量之比为 |
D.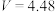 |
您最近一年使用:0次
名校
解题方法
4 . NH3可用作脱硝剂。某科研小组为了探究NO2能否被NH3还原,设计的装置如图所示(夹持、加热装置已略去,K1、K2为止水夹):
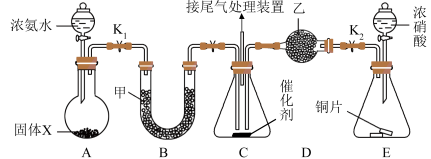
| A.固体X可以是无水CaCl2 |
| B.甲、乙试剂均可以是P2O5 |
| C.实验时宜先通入NO2,再通入NH3有利于减少空气对实验的干扰 |
| D.生成NO2的反应中n(还原剂):n(氧化剂)=1:4 |
您最近一年使用:0次
2023-05-08更新
|
937次组卷
|
7卷引用:皖豫名校联盟2023届高三下学期第三次大联考理科综合化学试题
皖豫名校联盟2023届高三下学期第三次大联考理科综合化学试题(已下线)第5讲 氮及其化合物(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)(已下线)考点16 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)2024届河南省南阳市方城县第一高级中学高一上学期1月期末模拟预测化学试题辽宁省沈阳市第二中学2023-2024学年高一下学期第一次月考化学试题广东省江门市新会第一中学2023-2024学年高三下学期热身考试化学试题
解题方法
5 . “化学—我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。结合给出的几个片段,回答下列问题:
片段1:干燥的空气(①)的成分按体积分数计算是:
 (②)约占78%,
(②)约占78%, (③)约占21%,稀有气体约占0.939%(
(③)约占21%,稀有气体约占0.939%( 、
、 、
、 、
、 、
、 、
、 ),
),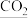 (④)约占0.031%。其他气体和杂质约占0.03%,如
(④)约占0.031%。其他气体和杂质约占0.03%,如 (⑤)、
(⑤)、 、
、 、
、 (⑥)。
(⑥)。
片段2:可以通过分离液态空气法获得 。
。
片段3:实验室制取氮气方法有多种,比如加热亚硝酸铵(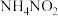 )的浓溶液,将亚硝酸钠
)的浓溶液,将亚硝酸钠 的饱和溶液(⑦)与氯化铵
的饱和溶液(⑦)与氯化铵 的饱和溶液相互作用,或将氨气
的饱和溶液相互作用,或将氨气 (⑧)通过红热的氧化铜
(⑧)通过红热的氧化铜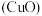 等。
等。
(1)上述划线并标有序号的物质中:属于电解质的是_______ ;属于非电解质的是_______ 。
(2)分离液态空气法是指先将空气加压降温变成液态,然后再加热,_______ (填“ ”或“
”或“ ”)首先从液态空气中蒸发出来。
”)首先从液态空气中蒸发出来。
(3)加热亚硝酸铵 的浓溶液的化学反应方程式为
的浓溶液的化学反应方程式为_______ ,被氧化的氮原子与被还原的氮原子的物质的量之比为_______ 。
(4)若在试管中进行氨气与红热的氧化铜反应实验,可观察到实验现象为_______ ,化学反应方程式为_______ 。
片段1:干燥的空气(①)的成分按体积分数计算是:
 (②)约占78%,
(②)约占78%, (③)约占21%,稀有气体约占0.939%(
(③)约占21%,稀有气体约占0.939%( 、
、 、
、 、
、 、
、 、
、 ),
),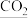 (④)约占0.031%。其他气体和杂质约占0.03%,如
(④)约占0.031%。其他气体和杂质约占0.03%,如 (⑤)、
(⑤)、 、
、 、
、 (⑥)。
(⑥)。片段2:可以通过分离液态空气法获得
 。
。片段3:实验室制取氮气方法有多种,比如加热亚硝酸铵(
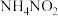 )的浓溶液,将亚硝酸钠
)的浓溶液,将亚硝酸钠 的饱和溶液(⑦)与氯化铵
的饱和溶液(⑦)与氯化铵 的饱和溶液相互作用,或将氨气
的饱和溶液相互作用,或将氨气 (⑧)通过红热的氧化铜
(⑧)通过红热的氧化铜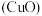 等。
等。(1)上述划线并标有序号的物质中:属于电解质的是
(2)分离液态空气法是指先将空气加压降温变成液态,然后再加热,
 ”或“
”或“ ”)首先从液态空气中蒸发出来。
”)首先从液态空气中蒸发出来。(3)加热亚硝酸铵
 的浓溶液的化学反应方程式为
的浓溶液的化学反应方程式为(4)若在试管中进行氨气与红热的氧化铜反应实验,可观察到实验现象为
您最近一年使用:0次
名校
解题方法
6 . 亚硝酸钠( ,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸(
,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸( )是一种弱酸,不稳定,易分解生成NO(无色)气体和
)是一种弱酸,不稳定,易分解生成NO(无色)气体和 (红棕色)气体;
(红棕色)气体; 是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
(1)人体正常的血红蛋白含有 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中
而中毒,应立即注射美蓝溶液进行治疗。上述过程中 表现出
表现出_______ 性(填“氧化”或“还原”下同),亚硝酸钠作_______ 剂,美蓝溶液被_______ 。
(2)下列有关检验工业食盐中是否混有亚硝酸钠的说法错误的是_______ 。
A.取样品,加碘化钾淀粉溶液,酸化后溶液变蓝,说明样品中含有亚硝酸钠
B.取样品,加稀硫酸,若观察到产生红棕色气体,证明样品中含有亚硝酸钠
C.取样品,加水溶解后,向其中加入 溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
(3)可用适量二氧化氯( )处理鱼塘中过量的亚硝酸钠,
)处理鱼塘中过量的亚硝酸钠, 被还原为
被还原为 ,该反应氧化剂与还原剂的物质的量之比为
,该反应氧化剂与还原剂的物质的量之比为_______ ;若有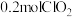 参与反应,则转移电子的数目是
参与反应,则转移电子的数目是_______ 。
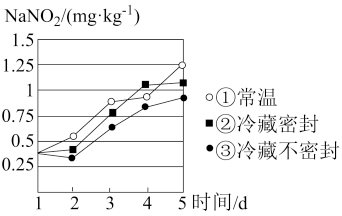
(4)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于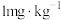 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是_______ (填序号)。
 ,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸(
,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸( )是一种弱酸,不稳定,易分解生成NO(无色)气体和
)是一种弱酸,不稳定,易分解生成NO(无色)气体和 (红棕色)气体;
(红棕色)气体; 是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:(1)人体正常的血红蛋白含有
 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中
而中毒,应立即注射美蓝溶液进行治疗。上述过程中 表现出
表现出(2)下列有关检验工业食盐中是否混有亚硝酸钠的说法错误的是
A.取样品,加碘化钾淀粉溶液,酸化后溶液变蓝,说明样品中含有亚硝酸钠
B.取样品,加稀硫酸,若观察到产生红棕色气体,证明样品中含有亚硝酸钠
C.取样品,加水溶解后,向其中加入
 溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
溶液,若观察到出现白色沉淀,则证明有亚硝酸钠(3)可用适量二氧化氯(
 )处理鱼塘中过量的亚硝酸钠,
)处理鱼塘中过量的亚硝酸钠, 被还原为
被还原为 ,该反应氧化剂与还原剂的物质的量之比为
,该反应氧化剂与还原剂的物质的量之比为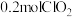 参与反应,则转移电子的数目是
参与反应,则转移电子的数目是(4)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于
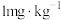 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是
您最近一年使用:0次
名校
7 . 利用如图所示装置进行 的制备及性质探究实验时,下列说法不正确的是
的制备及性质探究实验时,下列说法不正确的是

 的制备及性质探究实验时,下列说法不正确的是
的制备及性质探究实验时,下列说法不正确的是
| A.甲中反应的氧化剂与还原剂的物质的量之比为1∶4 |
B.乙的作用为除去 中的HCl 中的HCl |
| C.丙中紫色石蕊试液先变红后褪色 |
D.为吸收多余的 ,丁中可盛放NaOH溶液 ,丁中可盛放NaOH溶液 |
您最近一年使用:0次
2023-02-19更新
|
1774次组卷
|
6卷引用:安徽省定远县第三中学2022-2023学年高三下学期二模化学试题
安徽省定远县第三中学2022-2023学年高三下学期二模化学试题广东省深圳市2022-2023学年高三第一次调研考试化学试题(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题6-10)(已下线)专题13 化学实验基础四川省成都市第七中学2023-2024学年高一上学期期中考试化学试题四川省广安市华蓥中学2023-2024学年高一上学期12月月考化学试题
8 . CuCl2是一种重要的化工原料,不能采用Cu与稀盐酸直接反应制取CuCl2,但持续通入空气,并向溶液中加入FeCl3,可发生如图所示的反应。
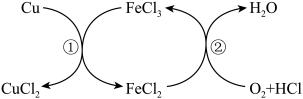
下列说法正确的是

下列说法正确的是
| A.反应①的离子方程式为Cu+Fe3+=Fe2++Cu2+ |
| B.反应②中氧化剂与还原剂的质量比为32∶127 |
| C.整个反应中,每消耗1个O2分子,一定转移4个电子 |
| D.FeCl3充当催化剂,且要不断添加FeCl3溶液 |
您最近一年使用:0次
2022-11-13更新
|
173次组卷
|
2卷引用:安徽省卓越县中联盟2022-2023学年高一上学期期中考试化学试题
9 . 已知:①
② (未配平)
(未配平)
③ (未配平)
(未配平)
下列有关说法正确的是

②
 (未配平)
(未配平)③
 (未配平)
(未配平)下列有关说法正确的是
| A.反应③中硫元素被氧化 |
B.反应②中氧化剂与还原剂的物质的量之比为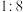 |
C.氧化性: |
D.根据上述反应可知 溶液与 溶液与 溶液不能反应 溶液不能反应 |
您最近一年使用:0次
名校
10 . 溴乙烷是无色油状液体,是制造巴比妥的原料,工业上可用海水制备溴乙烷,部分工艺流程如图:

下列说法错误的是

下列说法错误的是
| A.粗盐提纯时,加入沉淀剂的顺序可以是BaCl2、NaOH和Na2CO3 |
| B.向“母液”中通入热空气,利用溴的易挥发性,将溴吹出 |
| C.“制备”时氧化剂和还原剂的物质的量之比为3:1 |
| D.“精制”时所用的玻璃仪器有分液漏斗、烧杯 |
您最近一年使用:0次
2022-03-22更新
|
1080次组卷
|
3卷引用:安徽省六安市第一中学2021-2022学年高一下学期期末考试化学试题
安徽省六安市第一中学2021-2022学年高一下学期期末考试化学试题山东省济南市2022届高三3月高考模拟考试(一模)化学试题(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题6-10)



