1 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,下列有关说法正确的是
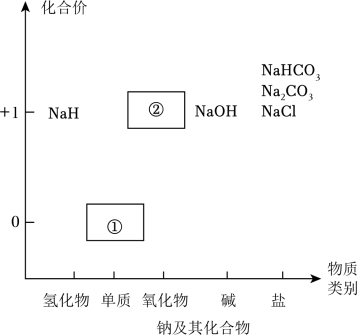

| A.物质①放入硫酸铜溶液中可观察到红色固体析出 |
| B.物质②可与水反应可以转化为NaOH,一定是碱性氧化物 |
| C.NaH中H元素的化合价为-1,可作还原剂 |
| D.在相同条件下,Na2CO3溶液的碱性弱于NaHCO3 |
您最近半年使用:0次
2 . 下列装置完成相关实验,合理的是
| A | B | C | D |
 |  | 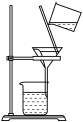 | 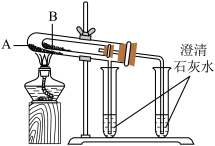 |
| 排空气收集法收集一瓶氯气应用b口进气 | 制备氢氧化铁胶体 | 除去粗盐水中的沙子 | 比较Na2CO3和NaHCO3热稳定性,B中放Na2CO3 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 某兴趣小组获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。将少量柠檬酸和这种白色粉末溶于水,混合后产生了能使澄清石灰水变浑浊的气体。于是对白色粉末的化学成分进行了以下探究:
【提出猜想】
猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氢钠。
【查阅资料】
碳酸钠溶液、碳酸氢钠溶液均呈碱性 。
【实验探究】
(1)小明、小磊分别对有关猜想设计实验方案并进行实验:
【交流反思】
(2)大家一致认为小明和小磊的结论不准确。
I.小明实验结论不准确的原因 是___________ 。
Ⅱ.小磊的实验方案不能 排除白色粉末中是否含有___________ 。
(3)下列关于Na2CO3和NaHCO3的说法中,正确的是___________ (填字母)。
A.Na2CO3和NaHCO3的溶液均显碱性
B.相同温度下,NaHCO3的溶解度大于Na2CO3
C.向等质量的Na2CO3和NaHCO3固体中分别滴加足量的盐酸,相同条件下产生CO2的体积也相同
(4)比较Na2CO3和NaHCO3的稳定性:Na2CO3的稳定性___________ (“强”或“弱”)于NaHCO3的稳定性。
【提出猜想】
猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氢钠。
【查阅资料】
碳酸钠溶液、碳酸氢钠溶液均呈
【实验探究】
(1)小明、小磊分别对有关猜想设计实验方案并进行实验:
| 学生 | 实验操作 | 实验现象 | 实验结论 |
| 小明 | 将白色粉末溶于水后用pH试纸测定其酸碱度 | pH | 溶液呈碱性,猜想1成立 |
| 小磊 | 用如图所示的装置进行实验: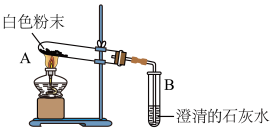 | 试管A中有水珠产生,试管B中液体变浑浊。 | 猜想2成立,试管A中反应的化学方程式为 |
【交流反思】
(2)大家一致认为小明和小磊的结论不准确。
I.小明实验结论不准确的
Ⅱ.小磊的实验方案
(3)下列关于Na2CO3和NaHCO3的说法中,正确的是
A.Na2CO3和NaHCO3的溶液均显碱性
B.相同温度下,NaHCO3的溶解度大于Na2CO3
C.向等质量的Na2CO3和NaHCO3固体中分别滴加足量的盐酸,相同条件下产生CO2的体积也相同
(4)比较Na2CO3和NaHCO3的稳定性:Na2CO3的稳定性
您最近半年使用:0次
4 . 某小组同学进行Na2CO3和NaHCO3性质的探究,实验如下(夹持装置已略去,气密性已检验)。
【实验一】
(1)实验I,能够证明Na2CO3的热稳定性强于NaHCO3的证据是___________ 。
(2)实验II,试剂a为___________ 。
(3)实验II,持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:___________ 。
【实验二】
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱。
(4)实验I中,溶解时吸收热量的物质是___________ (写化学式)。
(5)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为___________ ,(OH-未参与该反应的实验证据是___________ 。
(6)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有___________ 。
【实验一】
| 实验I | 实验II |
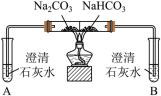 |  |
(2)实验II,试剂a为
(3)实验II,持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:
【实验二】
【查阅资料】pH越小,c(OH-)越小,溶液碱性越弱。
| 编号 | 实验操作 | 实验数据 |
| 实验I | 测量下述实验过程的温度变化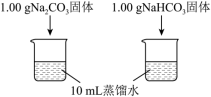 |  |
| 实验操作 | 实验数据 | |
| 实验II | 测量下述实验过程的pH变化 | ②和③中均产生白色沉淀。 各烧杯中pH变化如下图所示 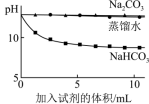 |
(5)实验II中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(6)实验II中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有
您最近半年使用:0次
5 . 下列“实验结论”与“实验操作及现象”不相符 的一组是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 分别向碳酸钠和碳酸氢钠固体中加入少量水 | 伴随着放热现象的是碳酸钠固体 |
| B | 向紫色石蕊溶液中加入氯水,溶液先变红,随后褪色 | 氯水中含有酸性物质和漂白性物质 |
| C | 把蘸有某溶液的洁净铂丝放在酒精灯外焰上灼烧,观察到火焰呈黄色 | 该溶液中含有Na+ |
| D | 向某溶液中加入AgNO3溶液有白色沉淀生成 | 该溶液中一定含有Cl- |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 下列有关钠的化合物的说法正确的是
A.用加热法除去 固体中混有的 固体中混有的 |
B. 与 与 的反应中只有氢氧化钠生成 的反应中只有氢氧化钠生成 |
| C.向酚酞溶液中加入过量的过氧化钠粉末,可以观察到:先变红,后褪色 |
| D.某溶液样品的焰色试验火焰呈黄色,证明原溶液中有钠元素,没有钾元素 |
您最近半年使用:0次
7 .  和
和 分别与
分别与 和
和 性质类似,下列说法正确的是
性质类似,下列说法正确的是
 和
和 分别与
分别与 和
和 性质类似,下列说法正确的是
性质类似,下列说法正确的是A.常温下在水中溶解性比 |
B.热稳定性 |
C.和酸反应放出 的快慢 的快慢 |
| D.水溶液中加入酚酞溶液均无法变红 |
您最近半年使用:0次
解题方法
8 . 根据如图所示装置(部分仪器已略去)回答下列有关问题。
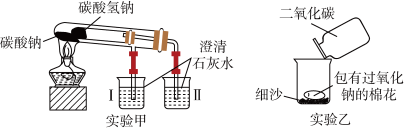
(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是_______ (填“I”或“II”),实验甲中该反应烧杯中发生反应的离子方程式是_______ 。
(2)通过实验甲可证明_______ (填“ ”或“
”或“ ”)更稳定。
”)更稳定。
(3)实验乙用来探究 与
与 的反应,观察到的实验现象为包有
的反应,观察到的实验现象为包有 的棉花着火。写出
的棉花着火。写出 与
与 反应的化学方程式:
反应的化学方程式:_______ ,棉花着火说明该反应的特点是_______ (填“放热反应”、“吸热反应”)。
(4)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的 气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为_______ 。

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是
(2)通过实验甲可证明
 ”或“
”或“ ”)更稳定。
”)更稳定。(3)实验乙用来探究
 与
与 的反应,观察到的实验现象为包有
的反应,观察到的实验现象为包有 的棉花着火。写出
的棉花着火。写出 与
与 反应的化学方程式:
反应的化学方程式:(4)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的
 气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
您最近半年使用:0次
解题方法
9 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
(1)写出钠与水反应的化学方程式________ 。
(2)过氧化钠是否属于碱性氧化物________ (填“是”或“否”);列举过氧化钠的一种用途________ ;
(3)下列关于 的认识正确的是________。(填字母)
的认识正确的是________。(填字母)
(4)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的 和
和 ,因
,因________ (填“ ”或“
”或“ ”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
(5)若面团发得不好,面团内的气孔少,不够膨松,需添加________ (填“ ”或“
”或“ ”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其原理
”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其原理________ 。
(1)写出钠与水反应的化学方程式
(2)过氧化钠是否属于碱性氧化物
(3)下列关于
 的认识正确的是________。(填字母)
的认识正确的是________。(填字母)| A.受热易分解 | B.俗称纯碱、苏打 | C.属于碱 | D.可与酸反应 |
 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的 和
和 ,因
,因 ”或“
”或“ ”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。(5)若面团发得不好,面团内的气孔少,不够膨松,需添加
 ”或“
”或“ ”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其原理
”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其原理
您最近半年使用:0次
10 . 回答下列问题
(1)碳酸钠是白色粉末,俗称________ ,常温下溶解度________ (填大于、小于或等于)碳酸氢钠,水溶液呈________ (填酸性、碱性或中性);电离方程式为________ 。
(2)书写碳酸氢钠与下列物质反应的化学反应方程式:
①与盐酸反应:________ 。
②受热分解:________ 。
③与 反应:
反应:________ 。
(3)焰色试验:若要观察钾元素的焰色,需要透过________ 观察火焰颜色。
(1)碳酸钠是白色粉末,俗称
(2)书写碳酸氢钠与下列物质反应的化学反应方程式:
①与盐酸反应:
②受热分解:
③与
 反应:
反应:(3)焰色试验:若要观察钾元素的焰色,需要透过
您最近半年使用:0次



