1 . 某化学学习小组在学习了Al、Fe的性质后,设计如下实验,探究Cu的常见化合物的性质。
[实验1]探究Cu(OH)2是否具有两性
药品:CuSO4溶液、浓NaOH溶液、稀H2SO4。
实验步骤:
①取少量CuSO4溶液于试管中,逐滴加入浓NaOH溶液至产生较多蓝色沉淀,静置后过滤。
②结论:Cu(OH)2具有两性。
(1)实验步骤②的内容为______
(2)能证明Cu(OH)2具有两性的实验现象为_______
[实验2]探究Cu(I)和Cu(Ⅱ)的稳定性
实验步骤:
①取98gCu(OH)2固体,加热至80~100℃时,得到80g黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A。
②冷却后称量,A的质量为72g。
③向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。
(3)通过计算判断A的化学式为_______ (不需要书写计算过程)
(4)步骤③中发生反应的离子方程式为____________
(5)根据上述实验现象得出Cu(I)和Cu(Ⅱ)的稳定性大小的结论为:固态时___________ ,酸性溶液中________ 。
[实验3]探究CuO被NH3还原的产物
该学习小组同学设计了如图所示的实验装置(夹持及尾气处理装置未面出)。实验中观察到CuO变为红色物质。查资料可知,同时生成一种无污染的气体。

(6)反应产生的无污染气体的化学式为_______
(7)有同学认为NH3与CuO反应后生成的红色物质是Cu,也有同学认为NH3与CuO反应后生成的红色物质是Cu和A的混合物。请你设计个简单的实验方案验证红色物质中是否含有A:_____ 。
[实验1]探究Cu(OH)2是否具有两性
药品:CuSO4溶液、浓NaOH溶液、稀H2SO4。
实验步骤:
①取少量CuSO4溶液于试管中,逐滴加入浓NaOH溶液至产生较多蓝色沉淀,静置后过滤。
②结论:Cu(OH)2具有两性。
(1)实验步骤②的内容为
(2)能证明Cu(OH)2具有两性的实验现象为
[实验2]探究Cu(I)和Cu(Ⅱ)的稳定性
实验步骤:
①取98gCu(OH)2固体,加热至80~100℃时,得到80g黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A。
②冷却后称量,A的质量为72g。
③向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。
(3)通过计算判断A的化学式为
(4)步骤③中发生反应的离子方程式为
(5)根据上述实验现象得出Cu(I)和Cu(Ⅱ)的稳定性大小的结论为:固态时
[实验3]探究CuO被NH3还原的产物
该学习小组同学设计了如图所示的实验装置(夹持及尾气处理装置未面出)。实验中观察到CuO变为红色物质。查资料可知,同时生成一种无污染的气体。

(6)反应产生的无污染气体的化学式为
(7)有同学认为NH3与CuO反应后生成的红色物质是Cu,也有同学认为NH3与CuO反应后生成的红色物质是Cu和A的混合物。请你设计个简单的实验方案验证红色物质中是否含有A:
您最近一年使用:0次
2 . 下列依据实验操作及现象得出的结论不正确的是
| A.将浓氨水滴入盛Cl2的集气瓶,产生白烟,证明NH3有还原性和碱性 |
| B.将白磷加入盛N2O的集气瓶中并微热,产生白烟,证明N2O有还原性 |
| C.将Cu2S在O2中充分灼烧,质量不变,证明Cu2S与O2在高温下不反应 |
| D.将足量SO2通入FeCl3溶液中,黄色逐渐消失,证明还原性:SO2>Fe2+ |
您最近一年使用:0次
名校
3 . 三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4, Cu2O在空气中加热生成CuO
【提出假设】
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
【设计探究实验】
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则预期实验现象是_________ 。
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?___________ 。
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明假设________ 成立,写出发生反应的所有离子方程式____________________ 。
【探究延伸】
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为________________ 。
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾(CuSO4∙5H2O),经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
实验室有下列试剂可供选择:
A.氯水 B.H2O2 C.硝酸 D.NaOH E.氨水 F.Cu2(OH)2CO3
实验小组设计如下实验方案:
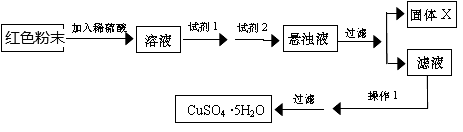
试回答:①试剂1为____________ ,试剂2为_____________ (填字母)。
②固体X的成分为____ ,操作1为 ________________ 。
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4, Cu2O在空气中加热生成CuO
【提出假设】
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
【设计探究实验】
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则预期实验现象是
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明假设
【探究延伸】
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾(CuSO4∙5H2O),经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
A.氯水 B.H2O2 C.硝酸 D.NaOH E.氨水 F.Cu2(OH)2CO3
实验小组设计如下实验方案:

试回答:①试剂1为
②固体X的成分为
您最近一年使用:0次
2017-12-07更新
|
287次组卷
|
2卷引用:福建省福建师范大学第二附属中学2018届高三上学期期中考试化学试题
填空题
|
较难(0.4)
|
4 . 足量锌与浓H2SO4充分在加热下反应生成会SO2和H2的混合气体;锌和稀硫酸反应只有H2生成。现有甲乙两研究小组分别实验探究:
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中SO2和H2,取少量的Zn置于b中,向a中加入100mL18.5mol·L-1的浓硫酸,经过一段时间反应,Zn完全溶解
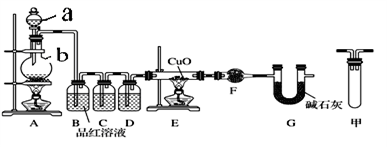
①填写仪器名称:a_____________ 、b_________ 。
②写出装置A中生成能使品红溶液褪色的化学反应方程式:_________________ 。
③装置D中加入的试剂是__________ 。
④U形管G的作用为______________ 。
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为__________ 。
⑥证明反应生成SO2和H2的实验现象是_________________ 。
⑦若A中生成标准状况下的气体33.6L,将A反应后的溶液稀释到1L,测得溶液中H+的浓度为0.1 mol·L-1,则稀释液中SO42-的物质的量浓度是_________ mol·L-1。
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。

实验时,从断开K开始 ,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是形成原电池反应速度快。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_____________________________________ 。
③ 从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是:_______ 。
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中SO2和H2,取少量的Zn置于b中,向a中加入100mL18.5mol·L-1的浓硫酸,经过一段时间反应,Zn完全溶解

①填写仪器名称:a
②写出装置A中生成能使品红溶液褪色的化学反应方程式:
③装置D中加入的试剂是
④U形管G的作用为
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为
⑥证明反应生成SO2和H2的实验现象是
⑦若A中生成标准状况下的气体33.6L,将A反应后的溶液稀释到1L,测得溶液中H+的浓度为0.1 mol·L-1,则稀释液中SO42-的物质的量浓度是
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。

实验时,
| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是形成原电池反应速度快。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是
③ 从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是:
您最近一年使用:0次
2017-07-01更新
|
1295次组卷
|
2卷引用:四川省广安市2016-2017学年高一下学期期末考试化学试题
名校
5 . 某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为________
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3•mCu(OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤。
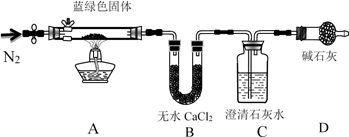
步骤2:甲同学取一定量固体,用气密性良好的下图装置(夹持仪器未画出)进行定性实验。请回答下列问题:
(1)假设2中的沉淀为________________ 。
(2)假设1中沉淀为Cu(OH)2的理论依据是____________________________________ 。
(3)无水乙醇洗涤的目的_________________________ 。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设__ (填写序号)成立。
(5)乙同学认为只要将上图中B装置的试剂改用____________ 试剂后,便可验证上述所有假设。
(6)乙同学更换B试剂后验证假设3成立的实验现象是_________________ 。
(7)在假设3成立的前提下,某同学考虑用Ba(OH)2代替Ca(OH)2,测定蓝绿色固体的化学式,若所取蓝绿色固体质量为27.1g,实验结束后装置B的质量增加2.7g,C中的产生沉淀的质量为19.7g。则该蓝绿色固体的化学式为____________________ 。
【提出假设】
假设1:沉淀为Cu(OH)2
假设2:沉淀为________
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3•mCu(OH)2]
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤。

步骤2:甲同学取一定量固体,用气密性良好的下图装置(夹持仪器未画出)进行定性实验。请回答下列问题:
(1)假设2中的沉淀为
(2)假设1中沉淀为Cu(OH)2的理论依据是
(3)无水乙醇洗涤的目的
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设
(5)乙同学认为只要将上图中B装置的试剂改用
(6)乙同学更换B试剂后验证假设3成立的实验现象是
(7)在假设3成立的前提下,某同学考虑用Ba(OH)2代替Ca(OH)2,测定蓝绿色固体的化学式,若所取蓝绿色固体质量为27.1g,实验结束后装置B的质量增加2.7g,C中的产生沉淀的质量为19.7g。则该蓝绿色固体的化学式为
您最近一年使用:0次
2016-12-09更新
|
230次组卷
|
7卷引用:2016届四川省雅安市三诊理综化学试卷
名校
6 . 某同学想用实验证明硫酸铜溶液显蓝色与 无关,则下列实验无意义的是
无关,则下列实验无意义的是
 无关,则下列实验无意义的是
无关,则下列实验无意义的是| A.观察硫酸钠溶液没有颜色 |
| B.加水稀释硫酸铜溶液,溶液蓝色变浅 |
| C.向硫酸铜溶液中滴加适量的氯化钡溶液,振荡后静置,溶液蓝色未消失 |
| D.向硫酸铜溶液中滴加适量的氢氧化钠溶液,振荡后静置,溶液蓝色消失 |
您最近一年使用:0次
2016-12-09更新
|
224次组卷
|
4卷引用:2015-2016学年江西省上高二中高一上第二次月考化学试卷
7 . 三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。现有一红色粉末可能含有Fe2O3和Cu2O中的一种或两种,设计合理的实验探究样品中Fe2O3、Cu2O的存在。
查阅数据知:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
请完成以下实验探究过程:
(一)提出假设
假设1:红色粉末是Fe2O3;
假设2:红色粉末是__________________;
假设3:红色粉末是___________________。
(二)设计实验方案
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是_________________________。
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?______________。简述你的理由________________________。
(3)若固体粉末完全溶解,向所得溶液中滴加KSCN 试剂时溶液不变红色,则证明原固体粉末是_______________。写出实验过程中发生反应的离子方程式________________、_______________、__________________。
(4)若经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物,欲用加热法测定Cu2O的质量分数,取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为_______。
查阅数据知:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
请完成以下实验探究过程:
(一)提出假设
假设1:红色粉末是Fe2O3;
假设2:红色粉末是__________________;
假设3:红色粉末是___________________。
(二)设计实验方案
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是_________________________。
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?______________。简述你的理由________________________。
(3)若固体粉末完全溶解,向所得溶液中滴加KSCN 试剂时溶液不变红色,则证明原固体粉末是_______________。写出实验过程中发生反应的离子方程式________________、_______________、__________________。
(4)若经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物,欲用加热法测定Cu2O的质量分数,取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为_______。
您最近一年使用:0次
10-11高三上·湖南长沙·阶段练习
名校
8 . 某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为沉淀可能是CuCO3;乙同学认为沉淀可能是Cu(OH)2;丙同学认为沉淀可能是CuCO3和Cu(OH)2的混合物。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.按照甲同学的观点,发生反应的离子反应方程式为_______________________ ;
在探究沉淀成分前,须将沉淀从溶液中分离并净化。其具体操作依次为____________________ 。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。
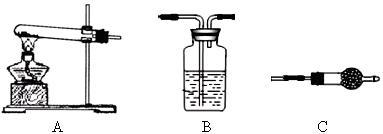
(1)各装置连接顺序为__________________________ 。
(2)能证明生成物中有CuCO3的实验现象是__________________ 。
Ⅲ.若CuCO3和Cu(OH)2两者都有,可利用下列装置通过实验测定其组成。
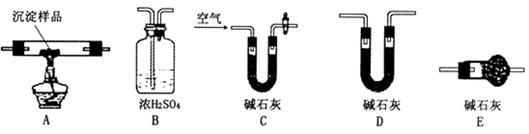

(1)装置C中碱石灰的作用是__________________ ,实验开始和结束时都要通入过量的空气,请说明结束时通入过量空气的作用是____________________________
(2)若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为___________ 。
甲同学认为沉淀可能是CuCO3;乙同学认为沉淀可能是Cu(OH)2;丙同学认为沉淀可能是CuCO3和Cu(OH)2的混合物。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.按照甲同学的观点,发生反应的离子反应方程式为
在探究沉淀成分前,须将沉淀从溶液中分离并净化。其具体操作依次为
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。

(1)各装置连接顺序为
(2)能证明生成物中有CuCO3的实验现象是
Ⅲ.若CuCO3和Cu(OH)2两者都有,可利用下列装置通过实验测定其组成。


(1)装置C中碱石灰的作用是
(2)若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为
您最近一年使用:0次
2016-12-09更新
|
532次组卷
|
4卷引用:2010年湖南省长沙一中高三上学期第三次月考化学试题
(已下线)2010年湖南省长沙一中高三上学期第三次月考化学试题(已下线)2011届广西河池高级中学高三第六次月考理综化学部分2020届高考化学二轮复习大题精准训练 ——定性分析探究实验题河南省商丘市第一高级中学2020届高三上学期期中考试化学试题
9 . 某校化学研究性学习小组的同学在学习了金属的知识后,为了解Cu的常见化合物性质,运用类比学习的思想提出如下的问题,探究。请你协助该小组的同学完成下列研究。
【提出问题】
①Cu的金属活泼性小于Al,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②通常情况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?③CuO能被H2、CO等还原,也能被NH3还原吗?
【实验方案】
(1)解决问题①需用到的药品有:CuSO4溶液、____ (填试剂),同时进行相关实验。
(2)解决问题②的实验步骤和现象如下:取98g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A.冷却后称量A的质量为72g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器还有红色固体存在。据些可推得,A的化学式为___ 。
(3)为解决问题③,设计的实验装置为(夹持及尾气处理装置未画出):
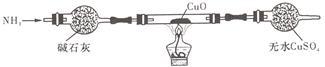
实验中观察到CuO变为红色物质,无水CuSO4变___ 色。同时生成一种对大气无污染的气体。
【实验结论】
(1)Cu(OH)2具有两性,证明Cu(OH)2具有两性的实验现象应是_____ 。
(2)根据“实验方案(2)”,得出的+1价Cu和+2价Cu稳定性大小的结论是____ 。
【问题讨论】
有同学认为NH3与CuO反应生成的红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质是Cu和A的混合物。
请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A___ 。
【提出问题】
①Cu的金属活泼性小于Al,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②通常情况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?③CuO能被H2、CO等还原,也能被NH3还原吗?
【实验方案】
(1)解决问题①需用到的药品有:CuSO4溶液、
(2)解决问题②的实验步骤和现象如下:取98g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A.冷却后称量A的质量为72g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器还有红色固体存在。据些可推得,A的化学式为
(3)为解决问题③,设计的实验装置为(夹持及尾气处理装置未画出):

实验中观察到CuO变为红色物质,无水CuSO4变
【实验结论】
(1)Cu(OH)2具有两性,证明Cu(OH)2具有两性的实验现象应是
(2)根据“实验方案(2)”,得出的+1价Cu和+2价Cu稳定性大小的结论是
【问题讨论】
有同学认为NH3与CuO反应生成的红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质是Cu和A的混合物。
请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A
您最近一年使用:0次
12-13高一上·广东·期末
名校
解题方法
10 . 已知下述三个实验均能发生化学反应
①将铁钉放入硫酸铜溶液中 ②向硫酸亚铁溶液中滴入几滴双氧水
③将铜丝放入氯化铁溶液中
下列判断正确的是( )
①将铁钉放入硫酸铜溶液中 ②向硫酸亚铁溶液中滴入几滴双氧水
③将铜丝放入氯化铁溶液中
下列判断正确的是( )
| A.实验①中铁钉做氧化剂 |
| B.实验②中Fe2+具有还原性 |
| C.实验③中发生的是置换反应 |
| D.上述实验证明氧化性Fe3+>Fe2+>Cu2+ |
您最近一年使用:0次
2016-10-21更新
|
327次组卷
|
10卷引用:2011-2012学年广东省实验中学高一上学期期末考试化学试卷
(已下线)2011-2012学年广东省实验中学高一上学期期末考试化学试卷2014-2015辽宁省大连市第二十高中高一上学期期末化学试卷2014-2015吉林省松原市扶余县一中高一上学期期末化学试卷2017届天津市静海一中高三上学期9月调研化学试卷山东省寿光现代中学2016-2017学年高一下学期第三学段质量监测(期中)化学试题湖南省郴州市2017-2018学年高一上学期期末考试化学试题湖南省长沙市雨花区2018-2019学年高一上学期期末考试化学试题河北省元氏县第四中学2020-2021学年高一10月月考化学试题云南省玉溪第三中学2021-2022学年高一上学期期末考试化学试题云南省开远市第一中学校2023-2024学年高一上学期期中考试化学试题



