名校
解题方法
1 . 工业上在一定条件下可由水煤气合成甲醇,同时有副反应,反应如下:
主反应: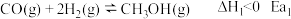
副反应: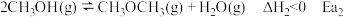
已知: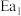 和
和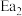 为正反应活化能,且
为正反应活化能,且 。
。
请回答:
(1)有利于主反应平衡正向移动的适宜条件___________ 。
A.高温高压 B.低温高压 C.高温低压 D.低温低压
(2)反应: 的
的
___________ (用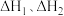 表示)
表示)
(3)若主反应在恒温恒容下进行,下列说法正确的是___________
A.当容器压强不变,反应处于平衡状态
B.K值越大,反应速率一定越快
C. 越小,放热越多,反应速率就越快
越小,放热越多,反应速率就越快
D.使用合适催化剂,可快速提高反应平衡前的转化率
E.正反应活化能越大, 就越大
就越大
(4)在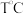 时,
时, 和
和 在体积为
在体积为 的恒温密闭容器中反应,测得2小时和5小时
的恒温密闭容器中反应,测得2小时和5小时 的选择性为80%和60%(
的选择性为80%和60%( 的选择性是指转化的
的选择性是指转化的 中生成
中生成 的百分比)。
的百分比)。 的转化率与时间的关系如图1所示:(不考虑其它副反应)
的转化率与时间的关系如图1所示:(不考虑其它副反应)
则:①2小时 的产率
的产率___________ 。
②副反应的平衡常数___________ 。
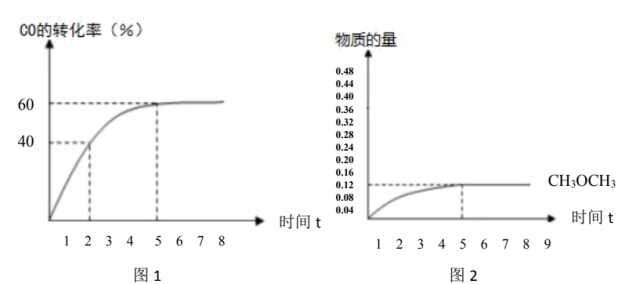
(5) 的物质的量随时间变化如图2所示,请在图2上画出
的物质的量随时间变化如图2所示,请在图2上画出 的物质的量随时间变化曲线
的物质的量随时间变化曲线___________ 。
主反应:
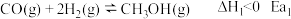
副反应:
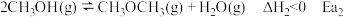
已知:
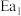 和
和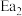 为正反应活化能,且
为正反应活化能,且 。
。请回答:
(1)有利于主反应平衡正向移动的适宜条件
A.高温高压 B.低温高压 C.高温低压 D.低温低压
(2)反应:
 的
的
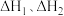 表示)
表示)(3)若主反应在恒温恒容下进行,下列说法正确的是
A.当容器压强不变,反应处于平衡状态
B.K值越大,反应速率一定越快
C.
 越小,放热越多,反应速率就越快
越小,放热越多,反应速率就越快D.使用合适催化剂,可快速提高反应平衡前的转化率
E.正反应活化能越大,
 就越大
就越大(4)在
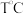 时,
时, 和
和 在体积为
在体积为 的恒温密闭容器中反应,测得2小时和5小时
的恒温密闭容器中反应,测得2小时和5小时 的选择性为80%和60%(
的选择性为80%和60%( 的选择性是指转化的
的选择性是指转化的 中生成
中生成 的百分比)。
的百分比)。 的转化率与时间的关系如图1所示:(不考虑其它副反应)
的转化率与时间的关系如图1所示:(不考虑其它副反应)则:①2小时
 的产率
的产率②副反应的平衡常数

(5)
 的物质的量随时间变化如图2所示,请在图2上画出
的物质的量随时间变化如图2所示,请在图2上画出 的物质的量随时间变化曲线
的物质的量随时间变化曲线
您最近一年使用:0次
2021-04-14更新
|
209次组卷
|
2卷引用:浙江省绍兴市诸暨中学2020-2021学年高一下学期4月期中考试(实验班)化学试题
解答题-原理综合题
|
适中(0.65)
|
名校
解题方法
2 . (1)断裂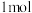 化学键所需要的能量如表所示,腓(
化学键所需要的能量如表所示,腓( )的有关化学反应的能量变化如图所示。
)的有关化学反应的能量变化如图所示。
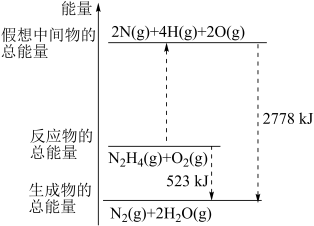
回答下列问题:
①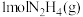 与
与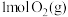 反应生成
反应生成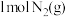 和
和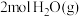 放出的能量为
放出的能量为____ kJ。
②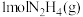 与
与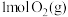 断键吸收的能量为
断键吸收的能量为____ kJ。
③a=____ 。
④当有 生成时,放出的能量
生成时,放出的能量_____ (填“>”“<”或“=”)523kJ。
(2)某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含 的废气和含
的废气和含 的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。
的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。
①分析该镇下酸雨的原因:_______ ;
②举一例说明酸雨对环境造成的危害:_______ ;
③该镇某中学环保小组提出了治理酸雨的下列措施,你认为其中不妥的是_______ ;
④可用熟石灰来处理硫酸厂排出的酸性废水,处理原理的化学方程式是_______ ;
⑤浓硫酸弄到手上后直接用大量水洗,然后涂上碳酸氢钠。这样的处理方法正确吗?_______ (填“正确”或“不正确”),理由是_______ 。
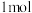 化学键所需要的能量如表所示,腓(
化学键所需要的能量如表所示,腓( )的有关化学反应的能量变化如图所示。
)的有关化学反应的能量变化如图所示。
| 化学键 |  | 氧氧键 |  |  |
能量/( ) ) |  | 498 | 946 | 391 |
①
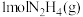 与
与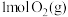 反应生成
反应生成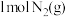 和
和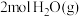 放出的能量为
放出的能量为②
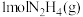 与
与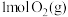 断键吸收的能量为
断键吸收的能量为③a=
④当有
 生成时,放出的能量
生成时,放出的能量(2)某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含
 的废气和含
的废气和含 的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。
的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。①分析该镇下酸雨的原因:
②举一例说明酸雨对环境造成的危害:
③该镇某中学环保小组提出了治理酸雨的下列措施,你认为其中不妥的是
| A.将硫酸厂搬离该镇 |
| B.建议环保部门限令整改 |
C.将硫酸厂排出的废气中的 处理后排放 处理后排放 |
| D.工厂和居民改用较清洁的燃料 |
⑤浓硫酸弄到手上后直接用大量水洗,然后涂上碳酸氢钠。这样的处理方法正确吗?
您最近一年使用:0次
名校
解题方法
3 . (1)有两个反应:a.H2(g)+Cl2(g)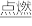 2HCl(g),b.H2(g)+Cl2(g)
2HCl(g),b.H2(g)+Cl2(g)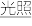 2HCl(g)。这两个反应的能量转化方式主要是
2HCl(g)。这两个反应的能量转化方式主要是___ 能转化为____ 能,相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量___ (填“相等”或“不相等”)。
(2)利用反应4HCl+O2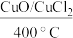 2Cl2+2H2O,可实现氯的循环利用,已知:该反应中,2molHCl被氧化时,放出57.8kJ的热量。
2Cl2+2H2O,可实现氯的循环利用,已知:该反应中,2molHCl被氧化时,放出57.8kJ的热量。
请回答下列有关问题:
①4molHCl被氧化时,放出___ kJ的热量。
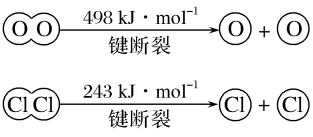
②断开1molH—O键与断开1molH—Cl键所需能量相差___ kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”)___ 。
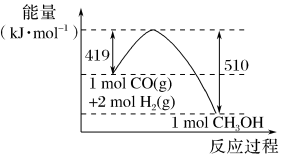
(3)根据图示的能量转化关系判断,生成16gCH3OH(l)____ (填“吸收”或“放出”)___ kJ能量。
 2HCl(g),b.H2(g)+Cl2(g)
2HCl(g),b.H2(g)+Cl2(g) 2HCl(g)。这两个反应的能量转化方式主要是
2HCl(g)。这两个反应的能量转化方式主要是(2)利用反应4HCl+O2
 2Cl2+2H2O,可实现氯的循环利用,已知:该反应中,2molHCl被氧化时,放出57.8kJ的热量。
2Cl2+2H2O,可实现氯的循环利用,已知:该反应中,2molHCl被氧化时,放出57.8kJ的热量。
请回答下列有关问题:
①4molHCl被氧化时,放出
②断开1molH—O键与断开1molH—Cl键所需能量相差
(3)根据图示的能量转化关系判断,生成16gCH3OH(l)

您最近一年使用:0次
解题方法
4 . Ⅰ.以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。回答下列问题:
已知:2Al2O3(s)=4Al(g)+3O2(g) ∆H=3351kJ·mol-1
2C(s)+O2(g)=2CO(g) ∆H=-221kJ·mol-1
2Al(g)+N2(g)=2AlN(s) ∆H=-318kJ·mol-1
碳热还原Al2O3合成AlN的总热化学方程式是_______ 。
II.已知化学反应:①AgNO3+NaCl=AgCl↓+NaNO3②2FeCl3+Cu=2FeCl2+CuCl2。
(1)上述两个化学反应中有一个不可用于设计原电池,它是_______ (填序号),理由是_______ 。
(2)另一个可用于设计原电池,若利用该反应设计如下图所示的原电池,请在如图方框中标明电极材料和电解质溶液的名称①_______ ②_______ ③_______ (图中“I”表示电流)。
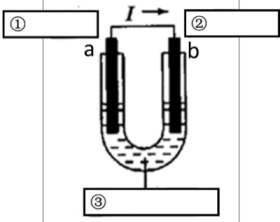
该电池电极a上发生的电极反应式是_______ ,电极b上发生_______ 反应(填“氧化”或“还原”)。
已知:2Al2O3(s)=4Al(g)+3O2(g) ∆H=3351kJ·mol-1
2C(s)+O2(g)=2CO(g) ∆H=-221kJ·mol-1
2Al(g)+N2(g)=2AlN(s) ∆H=-318kJ·mol-1
碳热还原Al2O3合成AlN的总热化学方程式是
II.已知化学反应:①AgNO3+NaCl=AgCl↓+NaNO3②2FeCl3+Cu=2FeCl2+CuCl2。
(1)上述两个化学反应中有一个不可用于设计原电池,它是
(2)另一个可用于设计原电池,若利用该反应设计如下图所示的原电池,请在如图方框中标明电极材料和电解质溶液的名称①

该电池电极a上发生的电极反应式是
您最近一年使用:0次
名校
解题方法
5 . 下图为元素周期表的一部分,根据元素①~⑧在表中的位置回答下列问题。
(1)元素⑧的最高价氧化物对应水化物的分子式为___________ ;
(2)元素①与④形成的18电子的化合物的结构式为___________ ;
(3)用电子式表示元素⑤与⑧形成化合物的过程___________ ;
(4)假设元素⑧的对应元素符号为X,若在一定条件下,X单质能够与硫反应生成一种用途广泛的硫化剂S2X2.该硫化剂S2X2与足量水反应有淡黄色沉淀生成,同时生成能够使品红溶液褪色的无色气体,则该反应的化学方程式是___________ (元素X请用具体元素符号表示)。
(5)元素①与③形成的简单化合物是___________ 分子(填极性或非极性)
(6)丙烷燃烧可以通过以下两种途径:
途径Ⅰ:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)ΔH=-akJ/mol
途径Ⅱ:C3H8(g)=C3H6(g)+H2(g)ΔH=+bkJ/mol
2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l)ΔH=-ckJ/mol
2H2(g)+O2(g)=2H2O(l)ΔH=-dkJ/mol(a、b、c、d均为正值)
判断等量的丙烷通过两种途径放出的热量,途径Ⅰ放出的热量___________ (填“大于”、“等于”或“小于”)途径Ⅱ放出的热量。
族 周期 | Ⅰ | 0 | ||||||
| 1 | ① | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)元素①与④形成的18电子的化合物的结构式为
(3)用电子式表示元素⑤与⑧形成化合物的过程
(4)假设元素⑧的对应元素符号为X,若在一定条件下,X单质能够与硫反应生成一种用途广泛的硫化剂S2X2.该硫化剂S2X2与足量水反应有淡黄色沉淀生成,同时生成能够使品红溶液褪色的无色气体,则该反应的化学方程式是
(5)元素①与③形成的简单化合物是
(6)丙烷燃烧可以通过以下两种途径:
途径Ⅰ:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)ΔH=-akJ/mol
途径Ⅱ:C3H8(g)=C3H6(g)+H2(g)ΔH=+bkJ/mol
2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l)ΔH=-ckJ/mol
2H2(g)+O2(g)=2H2O(l)ΔH=-dkJ/mol(a、b、c、d均为正值)
判断等量的丙烷通过两种途径放出的热量,途径Ⅰ放出的热量
您最近一年使用:0次
名校
6 . (1)已知下列热化学方程式:
a.H2(g)+ O2(g)═H2O(l);△H=-285.8kJ•mol-1
O2(g)═H2O(l);△H=-285.8kJ•mol-1
b.H2(g)+ O2(g)═H2O(g);△H=-241.8kJ•mol-1
O2(g)═H2O(g);△H=-241.8kJ•mol-1
c.CO(g)═C(s)+ O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1
d.C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
①上述反应中属于吸热反应的是________
②CO的燃烧热△H=________ 。表示CO燃烧热的热化学方程式为________ 。
③燃烧10g H2生成液态水,放出的热量为________ 。
(2)可以用反应的△H和△S的正、负来判断该反应自发进行的可能性和自发进行的条件。函数△G就是一个判断的依据:△G=△H-T△S式中T为反应的温度(开尔文温度,没有负值)。
①当一个反应的△G___________ 0(填“>”、“<”或“=”)时,反应一定能自发进行。
②当△H<0,△S<0,温度___________ (填“较高”或“较低”)时能自发反应。
a.H2(g)+
 O2(g)═H2O(l);△H=-285.8kJ•mol-1
O2(g)═H2O(l);△H=-285.8kJ•mol-1b.H2(g)+
 O2(g)═H2O(g);△H=-241.8kJ•mol-1
O2(g)═H2O(g);△H=-241.8kJ•mol-1c.CO(g)═C(s)+
 O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1d.C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
①上述反应中属于吸热反应的是
②CO的燃烧热△H=
③燃烧10g H2生成液态水,放出的热量为
(2)可以用反应的△H和△S的正、负来判断该反应自发进行的可能性和自发进行的条件。函数△G就是一个判断的依据:△G=△H-T△S式中T为反应的温度(开尔文温度,没有负值)。
①当一个反应的△G
②当△H<0,△S<0,温度
您最近一年使用:0次
2020-12-19更新
|
119次组卷
|
2卷引用:广西钦州市第四中学2020-2021学年高一下学期4月月考化学试题1
名校
解题方法
7 . 二甲醚(CH3OCH3)被称为“21 世纪的清洁燃料”。利用甲醇脱水可制得二甲醚,反应方程式如下: 2CH3OH(g)  CH3OCH3(g) + H2O(g) ΔH1
CH3OCH3(g) + H2O(g) ΔH1
(1)二甲醚亦可通过合成气反应制得,相关热化学方程式如下:
2H2(g)+ CO(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
CO(g)+ H2O(g) CO2(g)+ H2(g) ΔH3
CO2(g)+ H2(g) ΔH3
3H2(g)+ 3CO(g) CH3OCH3(g)+ CO2 (g) ΔH4
CH3OCH3(g)+ CO2 (g) ΔH4
则ΔH1=____________ (用含有ΔH2、ΔH3、ΔH4的关系式表示)。
(2)经查阅资料,上述反应平衡状态下 Kp的计算式为: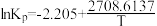 (Kp为以分压表示的平衡常数,T 为热力学温度)。且催化剂吸附 H2O(g)的量会受压强影响,从而进一步影响催化效率。)
(Kp为以分压表示的平衡常数,T 为热力学温度)。且催化剂吸附 H2O(g)的量会受压强影响,从而进一步影响催化效率。)
① 在一定温度范围内,随温度升高,CH3OH(g)脱水转化为二甲醚的倾向______________ (填“增大”、“不变”或“减小”)。
② 某温度下(此时 Kp=100),在密闭容器中加入CH3OH,反应到某时刻测得各组分的分压如下:
此时正、逆反应速率的大小:v正______ v逆 (填“>”、 “<”或“=”)。
③ 200℃时,在密闭容器中加入一定量甲醇 CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数为__________ (填标号)。
A < B
B  C
C  ~
~ D
D  E >
E >
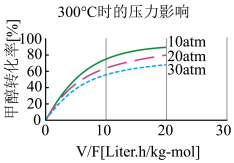
④ 300℃时,使 CH3OH(g)以一定流速通过催化剂,V/F (按原料流率的催化剂量)、压强对甲醇转化率影响如图所示。请解释甲醇转化率随压强(压力)变化的规律和产生这种变化的原因,规律,原因_________ 。
 CH3OCH3(g) + H2O(g) ΔH1
CH3OCH3(g) + H2O(g) ΔH1(1)二甲醚亦可通过合成气反应制得,相关热化学方程式如下:
2H2(g)+ CO(g)
 CH3OH(g) ΔH2
CH3OH(g) ΔH2CO(g)+ H2O(g)
 CO2(g)+ H2(g) ΔH3
CO2(g)+ H2(g) ΔH33H2(g)+ 3CO(g)
 CH3OCH3(g)+ CO2 (g) ΔH4
CH3OCH3(g)+ CO2 (g) ΔH4则ΔH1=
(2)经查阅资料,上述反应平衡状态下 Kp的计算式为:
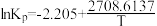 (Kp为以分压表示的平衡常数,T 为热力学温度)。且催化剂吸附 H2O(g)的量会受压强影响,从而进一步影响催化效率。)
(Kp为以分压表示的平衡常数,T 为热力学温度)。且催化剂吸附 H2O(g)的量会受压强影响,从而进一步影响催化效率。)① 在一定温度范围内,随温度升高,CH3OH(g)脱水转化为二甲醚的倾向
② 某温度下(此时 Kp=100),在密闭容器中加入CH3OH,反应到某时刻测得各组分的分压如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 分压/MPa | 0.50 | 0.50 | 0.50 |
③ 200℃时,在密闭容器中加入一定量甲醇 CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数为
A <
 B
B  C
C  ~
~ D
D  E >
E >
④ 300℃时,使 CH3OH(g)以一定流速通过催化剂,V/F (按原料流率的催化剂量)、压强对甲醇转化率影响如图所示。请解释甲醇转化率随压强(压力)变化的规律和产生这种变化的原因,规律,原因

您最近一年使用:0次
2020-11-26更新
|
90次组卷
|
2卷引用:江西省高安中学2020-2021学年高一上学期第一次月考(A)化学试题
名校
解题方法
8 . 甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
Ⅰ甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa 时,1mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出 5518kJ 热量。该反应的热化学方程式为:_____
(2)已知:25℃,101KPa 时,CH3OH(l)+ 3/2 O2(g)=CO2(g)+2H2O(l) ΔH=-726.5 kJ·mol-1
相同质量的甲醇和辛烷分别燃烧时,放出热量最多的是_____ (填化学式)
(3)CH3OH(l)+ O2(g)=CO(g)+2H2O(g) ΔH=-393 kJ·mol-1该反应相关化学键键能数据如下表:
则 X=_____ 。
Ⅱ甲醇的合成
(4)以 CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。
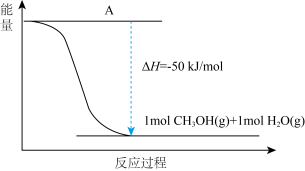
①补全上图:图中A 处应填入_____ 。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应 ΔH_____ (填“变大”“变小”“不变”)。
③已知:
CO(g)+ 1/2 O2(g) = CO2(g) ΔH1=-283kJ·mol-1
H2(g)+ 1/2 O2(g) = H2O(g)ΔH2=-242kJ·mol-1
CH3OH(g)+ 3/2 O2(g)=CO2(g)+2H2O(g) ΔH3=-676 kJ·mol-1
以 CO(g)和 H2(g)为原料合成甲醇的反应为 CO(g)+ 2H2(g) = CH3OH(g),该反应的 ΔH=_____ kJ·mol-1。
Ⅰ甲醇可以替代汽油和柴油作为内燃机燃料
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃,101KPa 时,1mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出 5518kJ 热量。该反应的热化学方程式为:
(2)已知:25℃,101KPa 时,CH3OH(l)+ 3/2 O2(g)=CO2(g)+2H2O(l) ΔH=-726.5 kJ·mol-1
相同质量的甲醇和辛烷分别燃烧时,放出热量最多的是
(3)CH3OH(l)+ O2(g)=CO(g)+2H2O(g) ΔH=-393 kJ·mol-1该反应相关化学键键能数据如下表:
| 化学键 | O=O | C-O | C=O | H-O | C-H |
| E/( kJ·mol-1) | X | 343 | 1076 | 465 | 413 |
Ⅱ甲醇的合成
(4)以 CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如图所示。

①补全上图:图中A 处应填入
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应 ΔH
③已知:
CO(g)+ 1/2 O2(g) = CO2(g) ΔH1=-283kJ·mol-1
H2(g)+ 1/2 O2(g) = H2O(g)ΔH2=-242kJ·mol-1
CH3OH(g)+ 3/2 O2(g)=CO2(g)+2H2O(g) ΔH3=-676 kJ·mol-1
以 CO(g)和 H2(g)为原料合成甲醇的反应为 CO(g)+ 2H2(g) = CH3OH(g),该反应的 ΔH=
您最近一年使用:0次
2020-09-30更新
|
113次组卷
|
3卷引用:陕西省延安市第四中学(宝塔中学)2020-2021学年高一下学期期末考试化学试题
解题方法
9 . 断裂 化学键所需要的能量如表所示,肼(
化学键所需要的能量如表所示,肼( )的有关化学反应的能量变化如图所示。
)的有关化学反应的能量变化如图所示。
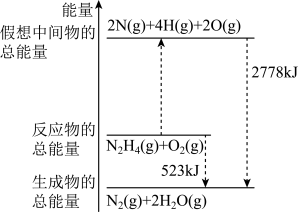
回答下列问题:
(1)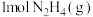 与
与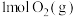 反应生成
反应生成 和
和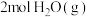 放出的能量为
放出的能量为____________________  。
。
(2)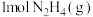 与
与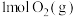 断键吸收的能量为
断键吸收的能量为____________  。
。
(3)
________________________ 。
(4)当有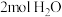 (1)生成时,放出的能量
(1)生成时,放出的能量__________________________ (填“>”“<”或“=”)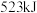 。
。
 化学键所需要的能量如表所示,肼(
化学键所需要的能量如表所示,肼( )的有关化学反应的能量变化如图所示。
)的有关化学反应的能量变化如图所示。| 化学键 |  | 氧氧键 |  |  |
能量/( ) ) | a | 498 | 946 | 391 |

回答下列问题:
(1)
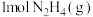 与
与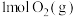 反应生成
反应生成 和
和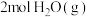 放出的能量为
放出的能量为 。
。(2)
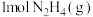 与
与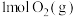 断键吸收的能量为
断键吸收的能量为 。
。(3)

(4)当有
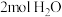 (1)生成时,放出的能量
(1)生成时,放出的能量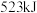 。
。
您最近一年使用:0次
2020-09-24更新
|
342次组卷
|
2卷引用:福建省南安市柳城中学2020-2021学年高一下学期期中考试化学试题
14-15高三上·浙江宁波·期末
10 . 2013年雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO (g) 2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:

①该反应的平衡常数表达式为_______ 。
②该反应的ΔH_______ 0(选填“>”、“<”)。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线____ 。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) =-867kJ·mol-1
=-867kJ·mol-1
2NO2(g) ⇌ N2O4(g) =-56.9kJ·mol-1
=-56.9kJ·mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式_______ 。
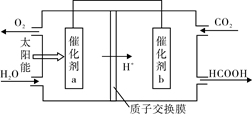
②将燃煤产生的二氧化碳回收利用,可 达到低碳排放的目的。图为通过光电转化原理以廉价原料制备新产品的示意图。写出上述光电转化过程的化学反应方程式_______ 。催化剂a、b之间连接导线上电子流动方向是_______ (填a→b或b→a) 。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO (g)
 2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
①该反应的平衡常数表达式为
②该反应的ΔH
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g)
 =-867kJ·mol-1
=-867kJ·mol-12NO2(g) ⇌ N2O4(g)
 =-56.9kJ·mol-1
=-56.9kJ·mol-1写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式
②将燃煤产生的二氧化碳回收利用,可 达到低碳排放的目的。图为通过光电转化原理以廉价原料制备新产品的示意图。写出上述光电转化过程的化学反应方程式

您最近一年使用:0次
2019-01-30更新
|
1078次组卷
|
5卷引用:河南省商水县第二高中2020-2021学年高一下学期月考化学试题



