1 . 中国科学家在实验室内实现了从二氧化碳到糖的精准全合成,合成过程如图所示。下列说法错误的是
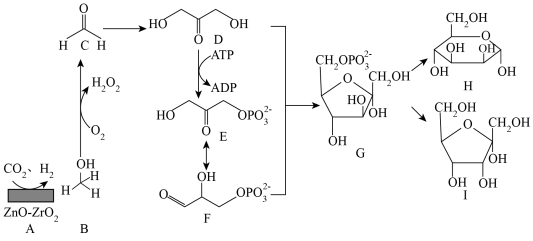

| A.化合物B生成化合物C的反应为氧化反应 |
| B.化合物D中所有原子可能共平面 |
| C.化合物E和F均能使酸性高锰酸钾溶液褪色 |
| D.化合物H、I互为同分异构体 |
您最近半年使用:0次
解题方法
2 . 反应CO2(g)+3H2(g)CH3OH(g)+H2O(g)是我国科学家2021年发布的由CO2人工合成淀粉中的重要反应之一、CO2与H2制备甲醇在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的物种用*标注,TS为过渡态),下列说法不正确的是
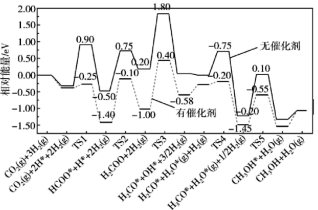

| A.升高温度,CO2与H2制备甲醇的反应v(逆)比v(正)增大的更多 |
| B.催化剂可使反应历程中决速步骤活化能降低0.20eV |
| C.加压、降温对制备甲醇有利,因此应该在高压、低温下进行上述反应 |
| D.CO2与H2制备甲醇反应往往伴随副反应,选择合适催化剂可提高甲醇反应的选择性 |
您最近半年使用:0次
名校
3 .  参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( ,
, 表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,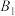 、
、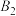 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是
 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( ,
, 表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,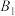 、
、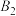 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是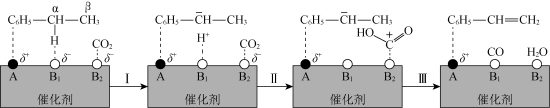
A.乙苯脱氢反应中 作氧化剂 作氧化剂 |
| B.乙苯脱氢后所得有机产物中所有原子可以共平面 |
C.步骤Ⅰ可表述为乙苯 带部分正电荷,被带部分负电荷的 带部分正电荷,被带部分负电荷的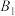 位点吸引,随后解离出 位点吸引,随后解离出 并吸附在 并吸附在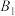 位点上 位点上 |
D.步骤Ⅱ可描述为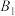 位点上的 位点上的 与 与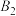 位点上 位点上 中带部分负电荷的C作用生成 中带部分负电荷的C作用生成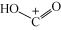 ,带部分正电荷的C吸附在带部分负电荷的 ,带部分正电荷的C吸附在带部分负电荷的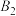 位点上 位点上 |
您最近半年使用:0次
2024-03-14更新
|
477次组卷
|
2卷引用:2024届河北省部分高三下学期一模化学试题
名校
4 . 中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成 的原理示意图如下。下列说法正确的是
的原理示意图如下。下列说法正确的是
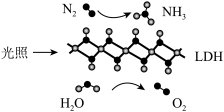
 的原理示意图如下。下列说法正确的是
的原理示意图如下。下列说法正确的是
A.生成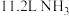 转移电子数约为 转移电子数约为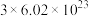 |
| B.该过程中,涉及极性键、非极性键的断裂与生成 |
| C.催化剂可以有效提高反应物的平衡转化率 |
D.该反应合成 的原子利用率为100% 的原子利用率为100% |
您最近半年使用:0次
名校
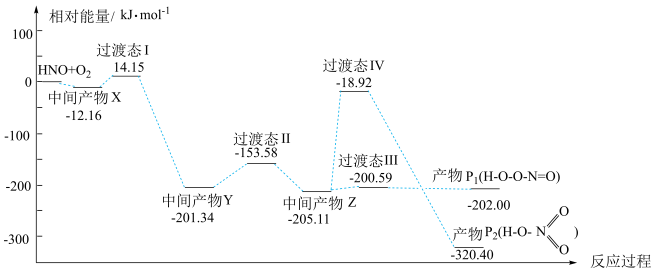
5 . 自由基是化学键断裂时产生的含未成对电子的中间体,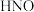 自由基与
自由基与 反应过程的能量变化如图所示。下列说法正确的是
反应过程的能量变化如图所示。下列说法正确的是
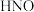 自由基与
自由基与 反应过程的能量变化如图所示。下列说法正确的是
反应过程的能量变化如图所示。下列说法正确的是
A.产物 的键能总和大于产物 的键能总和大于产物 的键能总和 的键能总和 |
B.产物 与 与 的分子式相同,但稳定性 的分子式相同,但稳定性 强于 强于 |
C.可以通过选择合适的催化剂,提高产物中 的含量 的含量 |
D.相同条件下,中间产物 转化为产物的速率: 转化为产物的速率: |
您最近半年使用:0次
名校
解题方法
6 . 丙烯是一种重要的有机化工原料,人们一直在寻求更为广泛和经济的丙烯来源。以丙烷为原料制备丙烯的部分反应机理如图所示(图中体现了由丙烷制备丙烯的2种历程)。下列说法正确的是
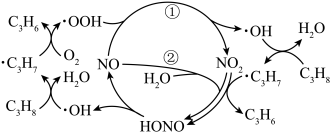

| A.消耗等量的NO时,反应①和②中转移电子的数目相等 |
| B.其他条件相同时,2种反应历程的C3H8的平衡转化率相同 |
C.丙烷制备丙烯的反应为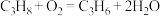 |
| D.反应过程中,N元素呈现的化合价仅有+2价、+4价 |
您最近半年使用:0次
7 . 水氧化反应是水分解反应的决速步骤,章宇超团队利用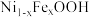 作光催化剂,通过以下转化途径,显著提升光催化水氧化反应速率,为太阳能的高效利用提供了新的策略。下列有关说法正确的是
作光催化剂,通过以下转化途径,显著提升光催化水氧化反应速率,为太阳能的高效利用提供了新的策略。下列有关说法正确的是
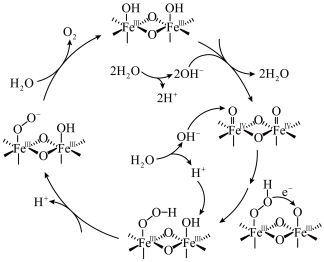
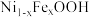 作光催化剂,通过以下转化途径,显著提升光催化水氧化反应速率,为太阳能的高效利用提供了新的策略。下列有关说法正确的是
作光催化剂,通过以下转化途径,显著提升光催化水氧化反应速率,为太阳能的高效利用提供了新的策略。下列有关说法正确的是
| A.转化途径中产生1个O2,理论上转移4个电子 |
| B.转化过程中化合态的O元素价态相同 |
| C.含Fe的化合物均为光电催化剂 |
| D.转化过程中光能最终全部转换为化学能 |
您最近半年使用:0次
名校
解题方法
8 . 氢气是一种理想的清洁能源,在多领域中均有重要的应用。
(1)利用 和
和 反应直接制取
反应直接制取 和
和 是简化制
是简化制 工艺,为
工艺,为 的利用提供便捷条件的新技术途径。其反应方程式为:
的利用提供便捷条件的新技术途径。其反应方程式为: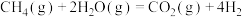
 。已知:部分化学键键能如下表:
。已知:部分化学键键能如下表:
①计算 =
=___________ 。利于此反应自发趋势的条件是___________ 。
②将一定量 和2mol
和2mol 置于2L刚性密闭容器中,进行上述反应,测得平衡体系中部分物质的物质的量浓度随温度变化关系如下图所示。
置于2L刚性密闭容器中,进行上述反应,测得平衡体系中部分物质的物质的量浓度随温度变化关系如下图所示。
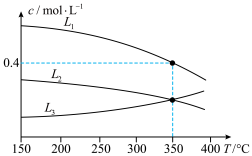
曲线 和
和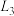 分别是表示
分别是表示___________ (填化学式)的浓度随温度的变化,计算:350°C时,上述反应的平衡常数 =
=___________ 。(填计算结果)。
(2)因上述反应耗能大,因此某研究小组利用 ,
, 和
和 在
在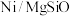 催化剂上进行甲烷部分氧化制氢的反应机理(
催化剂上进行甲烷部分氧化制氢的反应机理(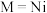 )如图所示:
)如图所示:
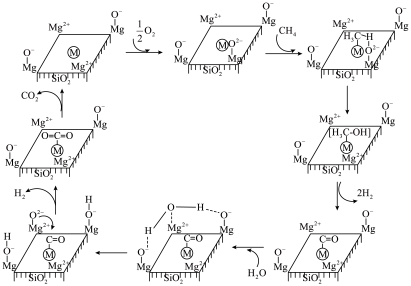
写出甲烷部分氧化制氢总反应方程式___________ ;反应过程中既发生断裂又形成的化学键类型有___________ (填序号)。
a.极性键 b.非极性键 c.离子键
(3)在460℃时,进料比为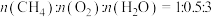 ,以不同空速(
,以不同空速( ,单位简写成
,单位简写成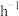 ,且空速越大,气体在催化剂表面停留时间越短),在
,且空速越大,气体在催化剂表面停留时间越短),在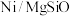 催化剂上发生(2)的转化,同时发生
催化剂上发生(2)的转化,同时发生 的反应,在不同空速时,甲烷转化率以及生成物的选择性(
的反应,在不同空速时,甲烷转化率以及生成物的选择性(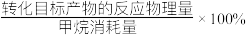 )数据如下表所示:
)数据如下表所示:
随着空速增大,甲烷转化率逐渐降低的可能原因为___________ ;氢气选择性逐渐增大的原因可能为___________ ;为使单位时间H₂产量达到最佳值,应选择空速为___________ 。
(1)利用
 和
和 反应直接制取
反应直接制取 和
和 是简化制
是简化制 工艺,为
工艺,为 的利用提供便捷条件的新技术途径。其反应方程式为:
的利用提供便捷条件的新技术途径。其反应方程式为: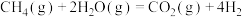
 。已知:部分化学键键能如下表:
。已知:部分化学键键能如下表:| 化学键 |  |  |  |  |
键能( ) ) | 745 | 436 | 413.4 | 462.8 |
 =
=②将一定量
 和2mol
和2mol 置于2L刚性密闭容器中,进行上述反应,测得平衡体系中部分物质的物质的量浓度随温度变化关系如下图所示。
置于2L刚性密闭容器中,进行上述反应,测得平衡体系中部分物质的物质的量浓度随温度变化关系如下图所示。
曲线
 和
和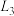 分别是表示
分别是表示 =
=(2)因上述反应耗能大,因此某研究小组利用
 ,
, 和
和 在
在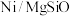 催化剂上进行甲烷部分氧化制氢的反应机理(
催化剂上进行甲烷部分氧化制氢的反应机理(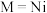 )如图所示:
)如图所示:
写出甲烷部分氧化制氢总反应方程式
a.极性键 b.非极性键 c.离子键
(3)在460℃时,进料比为
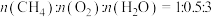 ,以不同空速(
,以不同空速( ,单位简写成
,单位简写成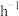 ,且空速越大,气体在催化剂表面停留时间越短),在
,且空速越大,气体在催化剂表面停留时间越短),在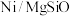 催化剂上发生(2)的转化,同时发生
催化剂上发生(2)的转化,同时发生 的反应,在不同空速时,甲烷转化率以及生成物的选择性(
的反应,在不同空速时,甲烷转化率以及生成物的选择性(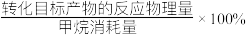 )数据如下表所示:
)数据如下表所示:空速/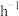 |  转化率/% 转化率/% | 选择性/% | ||
 |  |  | ||
| 600 | 67.8 | 95.8 | 90.2 | 9.8 |
| 1000 | 53.2 | 97.7 | 93.6 | 6.4 |
| 1400 | 39.3 | 99.2 | 98.4 | 1.6 |
| 1800 | 22.4 | 99.4 | 99.1 | 0.9 |
| 2200 | 14.9 | 99.5 | 99.5 | 0.5 |
您最近半年使用:0次
名校
解题方法
9 . 逆水煤气变换体系中存在以下两个反应:
反应Ⅰ: ;
;
反应Ⅱ: 。
。
在恒压条件下,按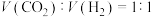 投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。下列说法正确的是
投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。下列说法正确的是
反应Ⅰ:
 ;
;反应Ⅱ:
 。
。在恒压条件下,按
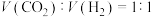 投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。下列说法正确的是
投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所示。下列说法正确的是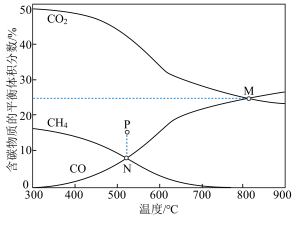
A.反应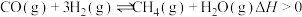 |
B. 点反应Ⅰ的平衡常数 点反应Ⅰ的平衡常数 约为1 约为1 |
C.加入合适的催化剂可由 点到 点到 点 点 |
D. 后,温度升高,反应Ⅰ的改变程度大于反应Ⅱ导致 后,温度升高,反应Ⅰ的改变程度大于反应Ⅱ导致 转化率明显减小 转化率明显减小 |
您最近半年使用:0次
2024-03-02更新
|
502次组卷
|
3卷引用:2024届河北省邢台市部分高中高三下学期二模化学试题
2024届河北省邢台市部分高中高三下学期二模化学试题江苏省海安高级中学2023-2024学年高三下学期开学考试化学试题(已下线)提升练05 化学平衡常数的计算-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
10 . 对于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.该反应的 |
B.反应的平衡常数可表示为 |
| C.使用高效催化剂能降低反应的焓变 |
D.其他条件相同,增大 的转化率下降 的转化率下降 |
您最近半年使用:0次
2024-02-29更新
|
40次组卷
|
2卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题



