解题方法
1 . 乙烯的产量是衡量一个国家石油化工发展水平的标志,乙烯作为现代有机合成的重要原料,研究其合成方法受到科学家的青睐。回答下列问题:
(1)丙烯歧化法
反应原理为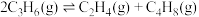
 ,向恒温恒容的密闭容器中通入一定量的
,向恒温恒容的密闭容器中通入一定量的 ,生成
,生成 的物质的量与时间的关系如表所示:
的物质的量与时间的关系如表所示:
①
___________ ;初始时总压强为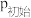 ,
, 时总压强为
时总压强为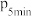 ,则
,则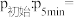
___________ 。
②其他条件不变,若缩小容器的体积,则 的转化率将
的转化率将___________ (填“增大”、“减小”或“不变”)。
(2) 催化加氢法
催化加氢法
反应原理为
 。向2L的恒容密闭容器中通入
。向2L的恒容密闭容器中通入
 和
和
 ,在催化剂作用下发生上述反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示:
,在催化剂作用下发生上述反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示:
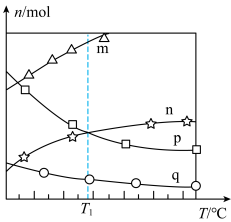
①图中曲线代表乙烯的物质的量随温度的变化关系的是___________ (填字母)。
②下列说法正确的是___________ (填标号)。
A.使用催化剂,可降低反应的活化能,加快反应速率,提高平衡产率
B.其他条件不变时,若扩大容器容积,则平衡逆向移动, 减小,
减小, 增大
增大
C.若容器内混合气体的密度不再随时间改变时,说明反应已达到平衡状态
D.保持其他条件不变,再通入
 ,达到平衡时
,达到平衡时 的转化率增大,平衡常数K保持不变
的转化率增大,平衡常数K保持不变
③ 时,反应的化学平衡常数
时,反应的化学平衡常数
___________ , 的平衡转化率为
的平衡转化率为___________ (保留三位有效数字)%。
(3)柴油裂解法
实验测得柴油裂解得到乙烯和丙烯的收率与温度、柴油在裂解设备内的停留时间的关系如图所示,工业上为获得较多的乙烯应选择较为适宜的温度和停留时间分别为___________ K和___________ s。

(1)丙烯歧化法
反应原理为
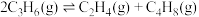
 ,向恒温恒容的密闭容器中通入一定量的
,向恒温恒容的密闭容器中通入一定量的 ,生成
,生成 的物质的量与时间的关系如表所示:
的物质的量与时间的关系如表所示:| 反应时间/min | 5 | 10 | 15 | 20 | 25 |
 的物质的量/mol 的物质的量/mol | 0.8 | 1.2 | 1.5 | a | 1.5 |

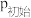 ,
, 时总压强为
时总压强为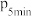 ,则
,则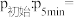
②其他条件不变,若缩小容器的体积,则
 的转化率将
的转化率将(2)
 催化加氢法
催化加氢法反应原理为

 。向2L的恒容密闭容器中通入
。向2L的恒容密闭容器中通入
 和
和
 ,在催化剂作用下发生上述反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示:
,在催化剂作用下发生上述反应,测得平衡时体系中各气体的物质的量随温度的变化关系如图所示:
①图中曲线代表乙烯的物质的量随温度的变化关系的是
②下列说法正确的是
A.使用催化剂,可降低反应的活化能,加快反应速率,提高平衡产率
B.其他条件不变时,若扩大容器容积,则平衡逆向移动,
 减小,
减小, 增大
增大C.若容器内混合气体的密度不再随时间改变时,说明反应已达到平衡状态
D.保持其他条件不变,再通入

 ,达到平衡时
,达到平衡时 的转化率增大,平衡常数K保持不变
的转化率增大,平衡常数K保持不变③
 时,反应的化学平衡常数
时,反应的化学平衡常数
 的平衡转化率为
的平衡转化率为(3)柴油裂解法
实验测得柴油裂解得到乙烯和丙烯的收率与温度、柴油在裂解设备内的停留时间的关系如图所示,工业上为获得较多的乙烯应选择较为适宜的温度和停留时间分别为

您最近一年使用:0次
名校
解题方法
2 . 工业合成氨是氮的活化重要途径之一。
(1)在一定条件下,将 和
和 通入到体积为1L的恒容容器中,下列说法能说明该可逆反应达到平衡状态的是______。
通入到体积为1L的恒容容器中,下列说法能说明该可逆反应达到平衡状态的是______。
(2)下列关于合成氨工艺的理解,正确的是______。
(3)比较合成氨工业与接触法制硫酸中SO2催化氧化的生产过程,下列说法错误的是______。
(1)在一定条件下,将
 和
和 通入到体积为1L的恒容容器中,下列说法能说明该可逆反应达到平衡状态的是______。
通入到体积为1L的恒容容器中,下列说法能说明该可逆反应达到平衡状态的是______。| A.容器中气体密度不变 | B.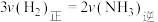 |
| C.容器中压强不变 | D. 、 、 、 、 分子数之比为1:3:2 分子数之比为1:3:2 |
| A.当温度、压强一定时,在原料气中添加少量惰性气体,有利于提高平衡转化率 |
| B.增大体系的压强能增大活化分子的百分数,从而加快反应速率 |
| C.合成氨反应选择在高温条件下进行时为了使平衡向正反应方向 |
| D.原料气须经过净化处理,以防止催化剂中毒和安全事故发生 |
| A.都使用了合适的催化剂 |
| B.都选择了较高的温度 |
| C.都采用了原料循环使用以提高原料利用率的方法 |
| D.都采用了高压的生产条件 |
您最近一年使用:0次
名校
解题方法
3 . 铬元素及其化合物在生产、生活中具有广泛的用途。醋酸亚铬水合物{[Cr(CH3COO)2]2⋅2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水和醚,易溶于盐酸。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价络(二价铬不稳定,极易被氧气氧化)
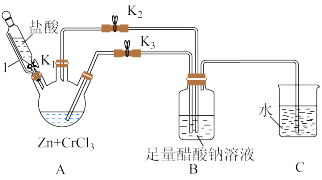
(1)仪器1的名称是___________ ,该装置的优点是 ___________ 。
(2)本实验中所用的溶液,配制用的蒸馏水都需事先煮沸,同时还要与C装置相连___________ 。
(3)本实验中锌粒要过量,其原因除了锌与CrCl3充分反应得到CrCl2外,另一个作用是___________ 。
(4)实验中,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应___________ 阀门K2、___________ 阀门K3(填“打开”或“关闭”)。
(5)为洗涤[Cr(CH3COO)2]2⋅2H2O产品,下列方法中最适合的是 ___________。
(6)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质6.34g,实验后得干燥纯净的[Cr(CH3COO)2]2⋅2H2O5.64g,请计算该实验所得产品的产率___________ 。

(1)仪器1的名称是
(2)本实验中所用的溶液,配制用的蒸馏水都需事先煮沸,同时还要与C装置相连
(3)本实验中锌粒要过量,其原因除了锌与CrCl3充分反应得到CrCl2外,另一个作用是
(4)实验中,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应
(5)为洗涤[Cr(CH3COO)2]2⋅2H2O产品,下列方法中最适合的是 ___________。
| A.先用盐酸洗,后用冷水洗 |
| B.先用冷水洗,后用乙醇洗 |
| C.先用冷水洗,后用乙醚洗 |
| D.先用乙醇洗涤,后用乙醚洗 |
(6)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质6.34g,实验后得干燥纯净的[Cr(CH3COO)2]2⋅2H2O5.64g,请计算该实验所得产品的产率
您最近一年使用:0次
名校
解题方法
4 . 工业合成氨是人类科学技术的一项重大突破。其合成原理为:
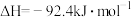

(1)下列关于工业合成氨的说法正确的是___________。
(2)一定温度下,在密闭容器中充入 和
和 并发生反应,若容器容积恒定,达到平衡时,气体的压强为原来的
并发生反应,若容器容积恒定,达到平衡时,气体的压强为原来的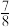 ,则
,则 的转化率为
的转化率为___________ 。
(3)工业上合成氨的部分工艺流程如图:
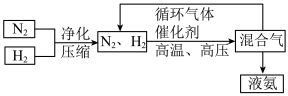
请用平衡移动原理来解释在流程中及时分离出氨气和循环使用气体的原因___________ 。
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响,实验结果如图所示(图中T表示温度)。则:
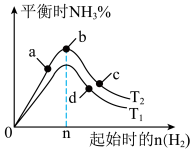
图象中 和
和 的关系是:
的关系是:
___________  (填“>、<或=”,下同);a、b、c、d四点所处的平衡状态中,反应物
(填“>、<或=”,下同);a、b、c、d四点所处的平衡状态中,反应物 的转化率最高的是
的转化率最高的是___________ (填字母)。
(5)恒温下,往一个 的密闭容器中充入
的密闭容器中充入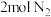 和
和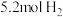 ,反应过程中对
,反应过程中对 的浓度进行检测,得到的数据如表所示:
的浓度进行检测,得到的数据如表所示:
此条件下该反应的化学平衡常数
___________ ;若维持容器体积不变,温度不变,往原平衡体系中加入 、
、 和
和 各
各 ,化学平衡将向
,化学平衡将向___________ 反应方向移动(填“正”或“逆”)。

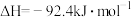

(1)下列关于工业合成氨的说法正确的是___________。
A.因为 ,所以该反应一定能自发进行 ,所以该反应一定能自发进行 |
| B.工业合成氨的反应是熵减小的放热反应,在常温时可自发进行 |
| C.合成氨反应选择在400~500℃进行的重要原因是此温度下氨的产率最高 |
| D.生产中在考虑动力和设备材料承受能力的前提下,压强越大越好 |
(2)一定温度下,在密闭容器中充入
 和
和 并发生反应,若容器容积恒定,达到平衡时,气体的压强为原来的
并发生反应,若容器容积恒定,达到平衡时,气体的压强为原来的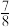 ,则
,则 的转化率为
的转化率为(3)工业上合成氨的部分工艺流程如图:

请用平衡移动原理来解释在流程中及时分离出氨气和循环使用气体的原因
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响,实验结果如图所示(图中T表示温度)。则:

图象中
 和
和 的关系是:
的关系是:
 (填“>、<或=”,下同);a、b、c、d四点所处的平衡状态中,反应物
(填“>、<或=”,下同);a、b、c、d四点所处的平衡状态中,反应物 的转化率最高的是
的转化率最高的是(5)恒温下,往一个
 的密闭容器中充入
的密闭容器中充入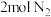 和
和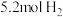 ,反应过程中对
,反应过程中对 的浓度进行检测,得到的数据如表所示:
的浓度进行检测,得到的数据如表所示:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
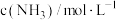 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |

 、
、 和
和 各
各 ,化学平衡将向
,化学平衡将向
您最近一年使用:0次
名校
5 . 研究小组以无水正己烷为溶剂,使用特定引发剂在 下,利用异丁烯(
下,利用异丁烯(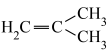 ,沸点为
,沸点为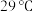 )在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
)在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
(1)正己烷溶剂的处理。正己烷干燥和收集的回流装置如图甲所示(夹持及加热装置略)。以 为指示剂,体系无水时呈现蓝色。
为指示剂,体系无水时呈现蓝色。

①仪器A的名称为___________ 。
②用钠丝除去正己烷中微量的水,其化学方程式为___________ 。
③若下列两过程开始时,活塞 、
、 、
、 均处于关闭状态,则:除水过程中,应打开的活塞为
均处于关闭状态,则:除水过程中,应打开的活塞为___________ ;当体系的颜色变为___________ 时,开始收集正己烷;收集过程中,应打开的活塞为___________ 。
(2)聚异丁烯的制备
①聚异丁烯的制备装置如图乙所示(夹持装置略)。三颈瓶中生成聚异丁烯的化学反应方程式为___________ 。
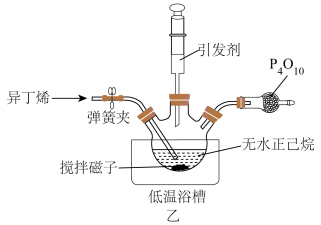
② 的作用为
的作用为___________ 。在低温浴槽中加入的最佳冷却剂为___________ (填序号)。
③将实验操作步骤补充完整:___________→d→___________→a→c→b(填序号)。________
a.搅拌下通过注射器滴加引发剂 b.经后续处理得成品
c.一定时间后加入反应终止剂停止反应 d.待三颈瓶中温度下降至既定温度
e.向三颈瓶中加入一定量无水正己烷 f.向三颈瓶中通入一定量异丁烯
(3)有研究发现,所得聚异丁烯的平均相对分子质量(M)与反应温度(T)的关系如图所示。已知T(K)=t(℃)+273,其中T为热力学温度,单位为K;t为摄氏温度,单位为℃。
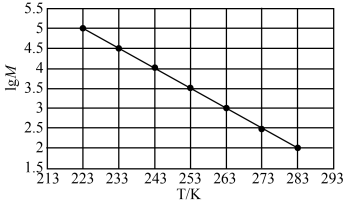
①欲合成平均相对分子质量为105的产品,则需控制反应温度t=___________ ℃。
②若控制反应温度为-30℃,则得到产品的平均聚合度为___________ (保留整数)。
 下,利用异丁烯(
下,利用异丁烯(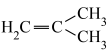 ,沸点为
,沸点为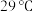 )在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。
)在无水条件下合成聚异丁烯。该物质常用作润滑油添加剂。(1)正己烷溶剂的处理。正己烷干燥和收集的回流装置如图甲所示(夹持及加热装置略)。以
 为指示剂,体系无水时呈现蓝色。
为指示剂,体系无水时呈现蓝色。
①仪器A的名称为
②用钠丝除去正己烷中微量的水,其化学方程式为
③若下列两过程开始时,活塞
 、
、 、
、 均处于关闭状态,则:除水过程中,应打开的活塞为
均处于关闭状态,则:除水过程中,应打开的活塞为(2)聚异丁烯的制备
①聚异丁烯的制备装置如图乙所示(夹持装置略)。三颈瓶中生成聚异丁烯的化学反应方程式为

②
 的作用为
的作用为| 序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| 冷却剂 | 冰水混合物 | 液氮 | 氯化钙晶体/冰 | 丙酮/干冰 | 液氨 |
| 最低温度/℃ | 0 | -195 | -55 | -78 | -33 |
a.搅拌下通过注射器滴加引发剂 b.经后续处理得成品
c.一定时间后加入反应终止剂停止反应 d.待三颈瓶中温度下降至既定温度
e.向三颈瓶中加入一定量无水正己烷 f.向三颈瓶中通入一定量异丁烯
(3)有研究发现,所得聚异丁烯的平均相对分子质量(M)与反应温度(T)的关系如图所示。已知T(K)=t(℃)+273,其中T为热力学温度,单位为K;t为摄氏温度,单位为℃。

①欲合成平均相对分子质量为105的产品,则需控制反应温度t=
②若控制反应温度为-30℃,则得到产品的平均聚合度为
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题。
(1)请根据下列信息判断氢气燃烧生成水蒸气时热量变化。
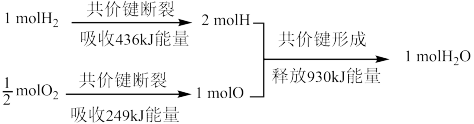
生成1mol水释放的能量___________ kJ。
(2)2SO2(g)+O2(g) 2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
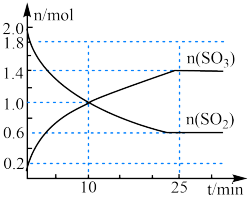
①0到10 min内, v(O2)=___________ 。
②下列情况能说明该反应达到化学平衡状态的是___________ (填字母)。
A. n(SO2) = n(SO3) B. v正 (SO2)=v逆 (SO2)
C. O2的含量保持不变 D.SO2、O2、SO3的浓度之比为2:1:2
③在密闭容器里,通入a mol SO2 (g)、b mol O2 (g)、c mol SO3 (g),发生上述反应,当改变某种条件时,反应速率会减小的是___________ (填字母)。
A.降低温度 B.加入催化剂
C.增大容器体积 D.恒容下,充入He
④工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
化工生产中,为了提高反应进行的程度而调控反应条件时,需要考虑控制反应条件的成本和实际可能性。催化氧化的生产时:温度较低时,反应速率小,需要很长时间才能达到化学平衡,生产成本高;而压强越大,对动力和生产设备的要求也越高。请结合上表,分析工业生产SO2催化氧化过程的适宜条件为:___________ 。
(1)请根据下列信息判断氢气燃烧生成水蒸气时热量变化。

生成1mol水释放的能量
(2)2SO2(g)+O2(g)
 2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
①0到10 min内, v(O2)=
②下列情况能说明该反应达到化学平衡状态的是
A. n(SO2) = n(SO3) B. v正 (SO2)=v逆 (SO2)
C. O2的含量保持不变 D.SO2、O2、SO3的浓度之比为2:1:2
③在密闭容器里,通入a mol SO2 (g)、b mol O2 (g)、c mol SO3 (g),发生上述反应,当改变某种条件时,反应速率会减小的是
A.降低温度 B.加入催化剂
C.增大容器体积 D.恒容下,充入He
④工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
 | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
您最近一年使用:0次
2023-09-09更新
|
248次组卷
|
2卷引用:四川省泸县第五中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
7 . 五氧化二钒(V2O5)是广泛用于冶金、化工等行业的催化剂。由富钒废渣制备V2O5的一种流程如下:
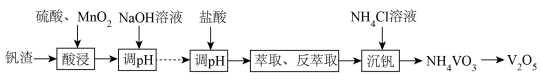
已知:i.NaVO3溶于水,NH4VO3难溶于水。
ii.部分含钒(五价)物质在水溶液中的主要存在形式:
(1)“酸浸”时,MnO2将VO+转化为 的离子反应方程式为
的离子反应方程式为___________ 。
(2)通过“调pH、萃取、反萃取”等过程,可制得NaVO3溶液。
已知 能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为:
能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为: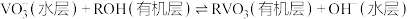 。
。
①萃取前,加盐酸调节溶液的pH为7的目的是___________ 。
②反萃取中, 反萃取率随着pH的升高呈现先增大后减小的趋势的原因是
反萃取率随着pH的升高呈现先增大后减小的趋势的原因是___________ 。
(3)“沉钒”时,向pH为8的NaVO3溶液中加入NH4Cl溶液,析出NH4VO3沉淀。沉钒温度需控制在70℃左右,温度不能过高的原因是___________ 。
(4)NH4VO3在空气中灼烧得V2O5。为测定回收所得V2O5样品的纯度,进行如下实验:称取1.000g灼烧后的样品,用稀硫酸溶解、定容得100mL(VO2)2SO4溶液。量取20.00mL溶液放入锥形瓶中,加入过量的5.00mL0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液12.00mL。
已知: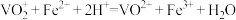 ;
;
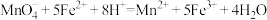 。
。
计算V2O5样品的纯度(写出计算过程)。___________ 。
(5)用活化后的V2O5作催化剂,NH3将NO还原为N2的一种反应历程如图所示。V2O5与H2O形成能提供质子的酸性位,NH3以“氢键”形式吸附在酸性位上生成“中间体X”;NO与X反应生成不稳定的“过渡态”物质,随后分解生成N2和H2O。“中间体X”的结构式可表示为:___________ 。


已知:i.NaVO3溶于水,NH4VO3难溶于水。
ii.部分含钒(五价)物质在水溶液中的主要存在形式:
| pH | <1.0 | 1.0~4.0 | 4.0~6.0 | 6.0~8.5 | 8.5~13.0 | >13.0 |
| 主要存在形式 |  | V2O5 | 多钒酸根 |  | 多钒酸根 |  |
| 备注 | 多钒酸盐在水中溶解度较小 | |||||
 的离子反应方程式为
的离子反应方程式为(2)通过“调pH、萃取、反萃取”等过程,可制得NaVO3溶液。
已知
 能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为:
能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为: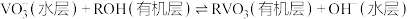 。
。①萃取前,加盐酸调节溶液的pH为7的目的是
②反萃取中,
 反萃取率随着pH的升高呈现先增大后减小的趋势的原因是
反萃取率随着pH的升高呈现先增大后减小的趋势的原因是(3)“沉钒”时,向pH为8的NaVO3溶液中加入NH4Cl溶液,析出NH4VO3沉淀。沉钒温度需控制在70℃左右,温度不能过高的原因是
(4)NH4VO3在空气中灼烧得V2O5。为测定回收所得V2O5样品的纯度,进行如下实验:称取1.000g灼烧后的样品,用稀硫酸溶解、定容得100mL(VO2)2SO4溶液。量取20.00mL溶液放入锥形瓶中,加入过量的5.00mL0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液12.00mL。
已知:
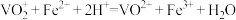 ;
;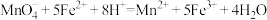 。
。计算V2O5样品的纯度(写出计算过程)。
(5)用活化后的V2O5作催化剂,NH3将NO还原为N2的一种反应历程如图所示。V2O5与H2O形成能提供质子的酸性位,NH3以“氢键”形式吸附在酸性位上生成“中间体X”;NO与X反应生成不稳定的“过渡态”物质,随后分解生成N2和H2O。“中间体X”的结构式可表示为:

您最近一年使用:0次
2023-09-09更新
|
475次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高二上学期12月月考化学试题
8 . 工业合成氨反应为N2(g)+3H2(g)⇌2NH3(g),氨在工农业生产中应用广泛。
(1)已知:键能是1mol化学键完全断裂形成气态原子所需要吸收的能量,部分化学键的键能如表格所示。计算每合成2molNH3可以_______ (填“放出”或“吸收”)热量_______ kJ。
(2)实验室中模拟合成氨过程,将1mol 和2.7mol
和2.7mol 置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是_______ (填序号)。
a.反应不再进行,已经停止
b.单位时间内生成nmol 的同时生成3nmol
的同时生成3nmol
c.2υ(H2)=υ(NH3)
d. 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2
e.混合气体的压强不再改变
f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2 mol∙L−1,则用氨气表示的0~10min内的平均化学反应速率为_______ 。
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
实际生产时,通常采用铁触媒作为催化剂、在400~500℃和10~30MPa的条件下合成氨。结合所学知识以及上述表格数据分析,工业上采用400~500℃反应的原因是_______ 。
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。
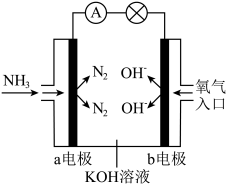
a电极是_______ (填“正极”或“负极”)。b电极的电极反应式是_______ 。
| 化学键 | H−H | N−H | N≡N |
键能( ) ) | 436 | 391 | 945.6 |
(1)已知:键能是1mol化学键完全断裂形成气态原子所需要吸收的能量,部分化学键的键能如表格所示。计算每合成2molNH3可以
(2)实验室中模拟合成氨过程,将1mol
 和2.7mol
和2.7mol 置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是a.反应不再进行,已经停止
b.单位时间内生成nmol
 的同时生成3nmol
的同时生成3nmol
c.2υ(H2)=υ(NH3)
d.
 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2e.混合气体的压强不再改变
f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2 mol∙L−1,则用氨气表示的0~10min内的平均化学反应速率为
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
压强(MPa)氨的平衡 含量(%) 温度(摄氏度) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。

a电极是
您最近一年使用:0次
名校
9 . 在一定温度和压强下,在密闭容器中充入H2、N2、NH3,开始时其物质的量之比为3∶1∶1,反应达平衡后,H2、N2、NH3的物质的量之比为9∶3∶4,则此时氮气的转化率为
| A.10% | B.20% |
| C.15% | D.30% |
您最近一年使用:0次
2023-08-27更新
|
452次组卷
|
3卷引用:吉林省长春市东北师范大学附属中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
10 . 以废银(主要含Ag,以及少量SiO2、α-Al2O3杂质)为原料提取高纯度银的流程如图1所示,其他条件相同,浸出率与温度、时间的关系分别如图2和图3所示:
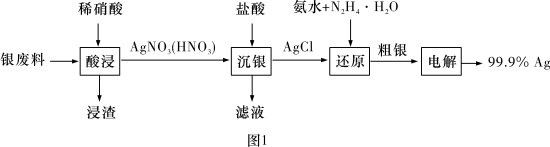
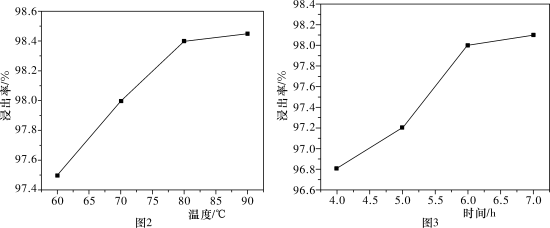
| A.最佳生产条件是温度为80℃、时间为6.0 h |
| B.浸渣的主要成分是SiO2 |
| C.“电解”中向AgNO3溶液中添加少量NaNO3能增强导电性 |
| D.理论上制备21.6 g Ag需要消耗2.5gN2H4·H2O |
您最近一年使用:0次
2023-08-16更新
|
173次组卷
|
2卷引用:福建省福建师范大学附属中学2023-2024学年高三上学期10月月考化学试题



