名校
1 . 以[Cu(H2O)]2+(蓝)+4Cl- [CuCl4]2-(黄)+4H2O △H>0为例,探究影响平衡移动的因素。取相同浓度的CuCl2溶液,分别进行下列实验,对实验现象的分析不正确的是
[CuCl4]2-(黄)+4H2O △H>0为例,探究影响平衡移动的因素。取相同浓度的CuCl2溶液,分别进行下列实验,对实验现象的分析不正确的是
 [CuCl4]2-(黄)+4H2O △H>0为例,探究影响平衡移动的因素。取相同浓度的CuCl2溶液,分别进行下列实验,对实验现象的分析不正确的是
[CuCl4]2-(黄)+4H2O △H>0为例,探究影响平衡移动的因素。取相同浓度的CuCl2溶液,分别进行下列实验,对实验现象的分析不正确的是| 操作和现象 | 分析 | |
| A. | 观察溶液为绿色 | [Cu(H2O)]2+和[CuCl4]2-同时存在 |
| B. | 升高温度,溶液变为黄绿色 | 平衡正移,[CuCl4]2-的浓度增大 |
| C. | 加几滴AgNO3溶液,静置,上层清液为蓝色 | 平衡逆移,[CuCl4]2-的浓度减小 |
| D. | 加少量Zn片,静置,上层清液为浅黄绿色 | 平衡正移,[CuCl4]2-的浓度增大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-11-30更新
|
121次组卷
|
4卷引用:陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(三)化学试题
真题
名校
2 . 在恒温恒容密闭容器中充入一定量 ,发生如下反应:
,发生如下反应: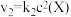 和
和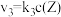 ,其中
,其中 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。
下列说法正确的是
 ,发生如下反应:
,发生如下反应: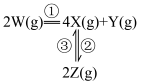
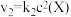 和
和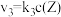 ,其中
,其中 分别为反应②和③的速率常数,反应③的活化能大于反应②。测得
分别为反应②和③的速率常数,反应③的活化能大于反应②。测得 的浓度随时间的变化如下表。
的浓度随时间的变化如下表。 | 0 | 1 | 2 | 3 | 4 | 5 |
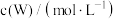 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 |
A. 内,X的平均反应速率为 内,X的平均反应速率为 |
| B.若增大容器容积,平衡时Y的产率增大 |
C.若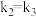 ,平衡时 ,平衡时 |
D.若升高温度,平衡时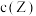 减小 减小 |
您最近半年使用:0次
2023-11-29更新
|
2879次组卷
|
3卷引用:陕西省西安中学2023-2024学年高三(实验版)上学期12月练考理科综合试题
名校
3 . 下列事实能用平衡移动原理解释的是
A. 溶液中加入少量 溶液中加入少量 固体,促进 固体,促进 分解 分解 |
B.锌片与稀 反应过程中,加入少量 反应过程中,加入少量 固体,促进 固体,促进 的产生 的产生 |
C.铁钉放入浓 中,待不再变化后,加热能产生大量红棕色气体 中,待不再变化后,加热能产生大量红棕色气体 |
D.密闭烧瓶内的 和 和 的混合气体,受热后颜色加深 的混合气体,受热后颜色加深 |
您最近半年使用:0次
2023-11-04更新
|
164次组卷
|
2卷引用:陕西师范大学附属中学2024届高三上学期第一次月考化学试题
名校
4 . 下列事实不能用勒夏特列原理解释的是
| A.实验室中常用排饱和食盐水的方式收集氯气 |
B.红棕色的 气体,加压后颜色先变深后变浅 气体,加压后颜色先变深后变浅 |
| C.合成氨工业中使用铁触媒作催化剂 |
D. 溶液加热后颜色由蓝绿色变为黄绿色 溶液加热后颜色由蓝绿色变为黄绿色 |
您最近半年使用:0次
2023-10-26更新
|
157次组卷
|
2卷引用:陕西省西安中学2023-2024学年高二上学期第一次综合评价化学试题
名校
解题方法
5 . 某课外活动小组为了探究外界条件对化学平衡的影响,做了如下实验:
(1)已知颜色深浅(I)与有色物质浓度(c)和观察深度(L)的乘积成正比: (式中k为常数)。在a、b两支容积均为30mL的针筒中分别抽入
(式中k为常数)。在a、b两支容积均为30mL的针筒中分别抽入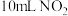 气体,将针筒前端封闭。
气体,将针筒前端封闭。

①将a针筒活塞迅速推至5mL处,从视线1处观察到的现象是___________ ;
②将b针筒活塞迅速拉至20mL处,从视线2处观察到的现象是___________ 。
(2)探究浓度对 平衡的影响。将
平衡的影响。将 溶液(接近无色)和
溶液(接近无色)和 溶液等体积混合,将得到的红色溶液分为两等份。甲、乙两同学分别取一份向其中加入少量KCl(s)。
溶液等体积混合,将得到的红色溶液分为两等份。甲、乙两同学分别取一份向其中加入少量KCl(s)。
①甲同学根据中学所掌握知识预测红色应该___________ (填“变深”“变浅”或“不变”)。
②乙同学查阅资料得知该反应为配位反应,且学习到更多配离子,如冰晶石中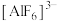 、银氨溶液中
、银氨溶液中 、
、 、
、 等。因此预测红色应该
等。因此预测红色应该___________ (填“变深”“变浅”或“不变”),理由:___________ 。
(1)已知颜色深浅(I)与有色物质浓度(c)和观察深度(L)的乘积成正比:
 (式中k为常数)。在a、b两支容积均为30mL的针筒中分别抽入
(式中k为常数)。在a、b两支容积均为30mL的针筒中分别抽入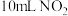 气体,将针筒前端封闭。
气体,将针筒前端封闭。
①将a针筒活塞迅速推至5mL处,从视线1处观察到的现象是
②将b针筒活塞迅速拉至20mL处,从视线2处观察到的现象是
(2)探究浓度对
 平衡的影响。将
平衡的影响。将 溶液(接近无色)和
溶液(接近无色)和 溶液等体积混合,将得到的红色溶液分为两等份。甲、乙两同学分别取一份向其中加入少量KCl(s)。
溶液等体积混合,将得到的红色溶液分为两等份。甲、乙两同学分别取一份向其中加入少量KCl(s)。①甲同学根据中学所掌握知识预测红色应该
②乙同学查阅资料得知该反应为配位反应,且学习到更多配离子,如冰晶石中
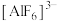 、银氨溶液中
、银氨溶液中 、
、 、
、 等。因此预测红色应该
等。因此预测红色应该
您最近半年使用:0次
2023-10-12更新
|
120次组卷
|
3卷引用:陕西省西安市鄠邑区2023-2024学年高二上学期期中质量检测化学试题
6 . 下列关于“化学反应速率和化学平衡”的说法正确的是
A.在恒温恒容条件下,当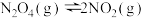 达到平衡后,再充入一定量的Ar后,反应速率减慢 达到平衡后,再充入一定量的Ar后,反应速率减慢 |
| B.向锌和稀硫酸反应的试管中滴加几滴CuSO4溶液,气泡生成速率加快,CuSO4是该反应的催化剂 |
C.某温度下,在恒容密闭容器中加入一定量X,发生反应 ,一段时间后达到平衡,再加入一定量X,达新平衡后X的物质的量分数增大 ,一段时间后达到平衡,再加入一定量X,达新平衡后X的物质的量分数增大 |
D.对于反应 达平衡后,缩小容器体积,N2的浓度增大 达平衡后,缩小容器体积,N2的浓度增大 |
您最近半年使用:0次
名校
7 . 工业上冶炼钙的原理如下。方法1:电解法。电解熔融 制备钙。方法2:铝热法。铝与氧化钙在高温、真空条件下反应生成钙蒸气,收集、冷凝得到钙,如
制备钙。方法2:铝热法。铝与氧化钙在高温、真空条件下反应生成钙蒸气,收集、冷凝得到钙,如 。已知部分物质的熔点和沸点如表所示:
。已知部分物质的熔点和沸点如表所示:
下列说法错误的是
 制备钙。方法2:铝热法。铝与氧化钙在高温、真空条件下反应生成钙蒸气,收集、冷凝得到钙,如
制备钙。方法2:铝热法。铝与氧化钙在高温、真空条件下反应生成钙蒸气,收集、冷凝得到钙,如 。已知部分物质的熔点和沸点如表所示:
。已知部分物质的熔点和沸点如表所示:| 物质 |  | CaO |  |  | Al | Ca |
| 熔点/℃ | 2054 | 2580 | 194 | 782 | 660 | 842 |
| 沸点/℃ | 2980 | 2850 | 178 | 1600 | 2467 | 1484 |
A.方法1的阴极产物为 |
B.方法2保持“真空”条件,避免钙与 等物质反应 等物质反应 |
| C.工业上用方法1的副产物可制备盐酸、漂粉精等 |
| D.用平衡移动原理可以解释方法2的化学原理 |
您最近半年使用:0次
2023-09-06更新
|
38次组卷
|
2卷引用:陕西省商洛市部分学校联考2023-2024学年高三上学期10月月考化学试题
名校
8 . 下列事实不能用勒夏特列原理解释的是
| A.新制氯水光照后颜色变浅 |
| B.氢气与碘蒸气反应的平衡混合气,经压缩后颜色变深 |
| C.工业合成氨,反应条件选择高压 |
| D.饮用汽水后常常出现“打嗝”现象 |
您最近半年使用:0次
2023-08-09更新
|
299次组卷
|
6卷引用:陕西省西安市西北工业大学附属中学2023-2024学年高二上学期期中考试化学试题
9 . 探究外界条件变化化学平衡的影响。向一密闭容器中通入1 mol N2、3 mol H2发生反应N2(g)+3H2(g) 2NH3(g) ΔH<0,一段时间后达到平衡。
2NH3(g) ΔH<0,一段时间后达到平衡。
(1)若增大N2的浓度,平衡移动的方向是_____________ ;达新平衡时,氮气的浓度与改变时相比较,其变化是________ 。
(2)若升高温度,平衡移动的方向是__________ ;达新平衡时的温度与改变时相比较,其变化是________ 。
(3)若增大压强,平衡移动的方向是__________ ;达新平衡时的压强与改变时相比较,其变化是________ 。
 2NH3(g) ΔH<0,一段时间后达到平衡。
2NH3(g) ΔH<0,一段时间后达到平衡。(1)若增大N2的浓度,平衡移动的方向是
(2)若升高温度,平衡移动的方向是
(3)若增大压强,平衡移动的方向是
您最近半年使用:0次
2023-07-15更新
|
68次组卷
|
2卷引用:陕西省渭南市蒲城县蒲城中学2023-2024学年高二上学期期中考试化学试题
名校
10 . 在恒温密闭的条件下进行反应:
 ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是| A.加入高效催化剂,即可增大反应速率,也可增大反应物的平衡转化率 |
| B.若为恒压容器,充入惰性气体,平衡不移动 |
C.达到平衡后,保持 的浓度不变,扩大容器体积,平衡逆向移动 的浓度不变,扩大容器体积,平衡逆向移动 |
| D.若将容器改为绝热恒容,如果反应从正向开始,则到达平衡的时间缩短 |
您最近半年使用:0次
2023-07-10更新
|
337次组卷
|
2卷引用:陕西省西北工业大学附属中学2022-2023学年高一下学期期末考试化学试题



