名校
1 . 25℃时,下列有关电解质溶液的说法正确的是
| A.氯水存在Cl2(g)+H2O(l)⇌HClO(aq)+H+(aq)+Cl-(aq),向平衡体系加水,c(Cl-)/c(HClO)不变 |
B.室温下向10mL0.1mo1•L-1的氨水中加水稀释后,溶液中 的值增大 的值增大 |
| C.等体积等浓度的盐酸、硫酸、醋酸三种溶液中,c(H+)相等 |
| D.向醋酸溶液中加入少量冰醋酸,醋酸电离平衡向右移动,电离程度增大 |
您最近一年使用:0次
2023-10-26更新
|
862次组卷
|
3卷引用:重庆市育才中学校2023-2024学年高三上学期三校联考模拟考化学试题(清北班)
解题方法
2 . 甲烷水蒸气重整反应是工业制备氢气的重要方式,在催化剂(如镍)表面发生的主要反应有:
①
 kJ⋅mol-1
kJ⋅mol-1
②

副反应: ,
,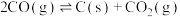 ,
,
Ⅰ.已知: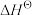 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其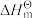 为零。
为零。
例如C(石墨)
 kJ·mol-1,则
kJ·mol-1,则 的标准生成焓为-393.5 kJ⋅mol-1。
的标准生成焓为-393.5 kJ⋅mol-1。
(1)
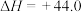 kJ⋅mol-1,结合表中数据计算反应
kJ⋅mol-1,结合表中数据计算反应
___________ 。
(2)在镍催化剂表面甲烷和水蒸气发生反应,最后生成CO、 和
和 ,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
a. ;
;
b.___________ ;
c. ;
;
d.___________ ;
e.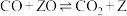
Ⅱ.在一体积可变的密闭容器中,投入一定量的 和
和 发生甲烷水蒸气重整反应。
发生甲烷水蒸气重整反应。
(3)下列有关说法正确的是___________。
(4)维持压强100 kPa,平衡时 、
、 、CO、
、CO、 的体积分数分别为a、b、c、d,反应①的平衡常数
的体积分数分别为a、b、c、d,反应①的平衡常数
___________  (用含字母的式子表示。
(用含字母的式子表示。 是以分压表示的平衡常数,分压=总压×体积分数)。
是以分压表示的平衡常数,分压=总压×体积分数)。
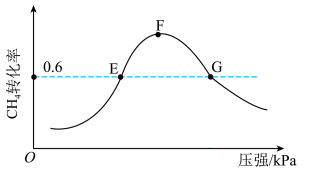
(5)500℃时,反应相同时间后测得 的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)___________ c(G)(填“>”“<”或“=”)。
(6)通过甲烷水蒸气重整反应的平衡含量计算,以及析碳条件的判断,该转化需适当增大水碳比[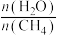 ],请分析可能的原因:
],请分析可能的原因:___________ 。
①

 kJ⋅mol-1
kJ⋅mol-1②


副反应:
 ,
,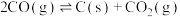 ,
,
Ⅰ.已知:
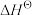 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其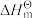 为零。
为零。例如C(石墨)

 kJ·mol-1,则
kJ·mol-1,则 的标准生成焓为-393.5 kJ⋅mol-1。
的标准生成焓为-393.5 kJ⋅mol-1。| 物质 |  |  | CO |
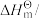 /kJ⋅mol-1 /kJ⋅mol-1 | -285.8 | -393.5 | -110.5 |

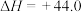 kJ⋅mol-1,结合表中数据计算反应
kJ⋅mol-1,结合表中数据计算反应
(2)在镍催化剂表面甲烷和水蒸气发生反应,最后生成CO、
 和
和 ,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。
,反应机理如下,请补充其中的两个反应方程式(Z表示催化剂的活性中心)。a.
 ;
; b.
c.
 ;
;d.
e.
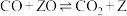
Ⅱ.在一体积可变的密闭容器中,投入一定量的
 和
和 发生甲烷水蒸气重整反应。
发生甲烷水蒸气重整反应。(3)下列有关说法正确的是___________。
A. 浓度不变,说明体系已达平衡状态 浓度不变,说明体系已达平衡状态 |
| B.反应②前后气体物质的量不变,所以此反应熵变为0 |
C.在催化剂表面, 、 、 分子中的化学键被削弱 分子中的化学键被削弱 |
D.在体系中通入适量的 ,有利于减少积碳,从而有利于反应进行 ,有利于减少积碳,从而有利于反应进行 |
 、
、 、CO、
、CO、 的体积分数分别为a、b、c、d,反应①的平衡常数
的体积分数分别为a、b、c、d,反应①的平衡常数
 (用含字母的式子表示。
(用含字母的式子表示。 是以分压表示的平衡常数,分压=总压×体积分数)。
是以分压表示的平衡常数,分压=总压×体积分数)。(5)500℃时,反应相同时间后测得
 的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
的转化率随压强的变化如图所示。则图中E点和G点CH4的浓度大小关系为c(E)
(6)通过甲烷水蒸气重整反应的平衡含量计算,以及析碳条件的判断,该转化需适当增大水碳比[
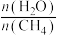 ],请分析可能的原因:
],请分析可能的原因:
您最近一年使用:0次
3 .  -
- 干重整技术(简称“DRM技术”)在转化利用
干重整技术(简称“DRM技术”)在转化利用 的同时可以大量利用
的同时可以大量利用 ,从而成为一项“绿色”的化工技术而受到科研人员的广泛关注。该过程中涉及的反应如下:
,从而成为一项“绿色”的化工技术而受到科研人员的广泛关注。该过程中涉及的反应如下:
主反应:

副反应:

回答下列问题:
(1)已知 、CO和
、CO和 的燃烧热分别为-890.3kJ/mol、-283.0kJ/mol和-285.8kJ/mol,DRM技术主反应的
的燃烧热分别为-890.3kJ/mol、-283.0kJ/mol和-285.8kJ/mol,DRM技术主反应的
_____ kJ/mol。
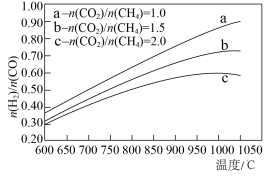
(2)在刚性密闭容器中,反应达到平衡状态时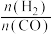 随温度变化的关系如图甲所示,随着进料比
随温度变化的关系如图甲所示,随着进料比 的增加,
的增加,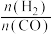 值的变化趋势及原因是
值的变化趋势及原因是_____ 。
(3)在1000℃、压强为P时,按投料比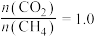 加入刚性密闭容器中,达平衡时甲烷的转化率为80%,二氧化碳的转化率为90%,则反应前后气体的总物质的量之比为
加入刚性密闭容器中,达平衡时甲烷的转化率为80%,二氧化碳的转化率为90%,则反应前后气体的总物质的量之比为_____ ,副反应的压强平衡常数
_____ (注:对于可逆反应: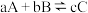 达到化学平衡时,
达到化学平衡时, )
)
(4)DRM技术主反应的催化转化原理的如图乙所示:
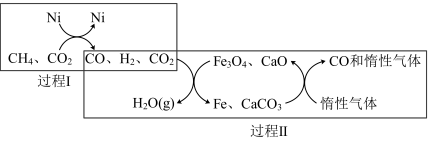
①过程Ⅱ实现了含氢物种与含碳物种的分离。生成 (g)的化学方程式是
(g)的化学方程式是_____ 。
②过程Ⅱ的催化剂是_____ ,只有过程Ⅰ投料比
_____ ,含铁催化剂组成才会保持不变,维持循环使用。
 -
- 干重整技术(简称“DRM技术”)在转化利用
干重整技术(简称“DRM技术”)在转化利用 的同时可以大量利用
的同时可以大量利用 ,从而成为一项“绿色”的化工技术而受到科研人员的广泛关注。该过程中涉及的反应如下:
,从而成为一项“绿色”的化工技术而受到科研人员的广泛关注。该过程中涉及的反应如下:主反应:


副反应:


回答下列问题:
(1)已知
 、CO和
、CO和 的燃烧热分别为-890.3kJ/mol、-283.0kJ/mol和-285.8kJ/mol,DRM技术主反应的
的燃烧热分别为-890.3kJ/mol、-283.0kJ/mol和-285.8kJ/mol,DRM技术主反应的
(2)在刚性密闭容器中,反应达到平衡状态时
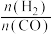 随温度变化的关系如图甲所示,随着进料比
随温度变化的关系如图甲所示,随着进料比 的增加,
的增加,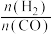 值的变化趋势及原因是
值的变化趋势及原因是
(3)在1000℃、压强为P时,按投料比
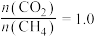 加入刚性密闭容器中,达平衡时甲烷的转化率为80%,二氧化碳的转化率为90%,则反应前后气体的总物质的量之比为
加入刚性密闭容器中,达平衡时甲烷的转化率为80%,二氧化碳的转化率为90%,则反应前后气体的总物质的量之比为
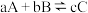 达到化学平衡时,
达到化学平衡时, )
)(4)DRM技术主反应的催化转化原理的如图乙所示:

①过程Ⅱ实现了含氢物种与含碳物种的分离。生成
 (g)的化学方程式是
(g)的化学方程式是②过程Ⅱ的催化剂是

您最近一年使用:0次
4 . 为研究工业废水(含有 和Cu2+,且
和Cu2+,且 的浓度远大于Cu2+)的处理方法,某实验小组用NaOH溶液调节该废水的pH(溶液体积变化忽略不计),测得上层清液中铜元素的含量随pH变化如图所示:
的浓度远大于Cu2+)的处理方法,某实验小组用NaOH溶液调节该废水的pH(溶液体积变化忽略不计),测得上层清液中铜元素的含量随pH变化如图所示:
下列有关说法正确的是
 和Cu2+,且
和Cu2+,且 的浓度远大于Cu2+)的处理方法,某实验小组用NaOH溶液调节该废水的pH(溶液体积变化忽略不计),测得上层清液中铜元素的含量随pH变化如图所示:
的浓度远大于Cu2+)的处理方法,某实验小组用NaOH溶液调节该废水的pH(溶液体积变化忽略不计),测得上层清液中铜元素的含量随pH变化如图所示:| 图表 | 查阅资料 |
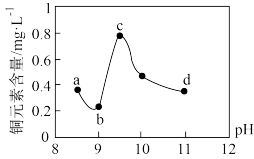 | 存在平衡Ⅰ: 存在平衡Ⅱ:  |
| A.处理工业废水中的Cu2+最佳点应选择c点 |
| B.bc段:随pH升高,Cu2+的量增加,平衡Ⅰ正向移动 |
C.cd段:随pH升高, 增大,再次有Cu(OH)2成 增大,再次有Cu(OH)2成 |
| D.d点以后,随pH升高,铜元素含量下降并保持不变 |
您最近一年使用:0次
名校
解题方法
5 . 铟(In)是一种稀散金属,常与其他金属矿石伴生,回收氧化锌烟尘(主要成分是ZnO,还含少量PbO、FeS、FeSiO3、 In2O3、 In2S3等)中的金属铟的工艺流程如下:
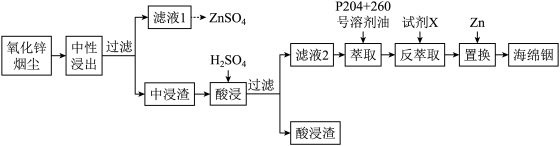
已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
回答下列问题:
(1)In2O3中In的化合价是_______________________ 。
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为____________________________________________ 。
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为 ,该反应的离子方程式为
,该反应的离子方程式为____________________ 。
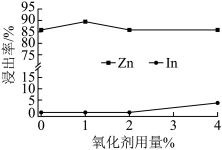
③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为_________________ 。
④“中浸渣”的主要成分为In(OH)3、________________ 。 (写化学式)
(3)萃取时,发生反应In3+ +3H2A2 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。
①反萃取时,宜选用的试剂X为_____________________ (写化学式)
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有_________________________ 。
(4)“置换”后的滤液可返回________________________ (填“滤液 1”或“滤液2”)中利用。
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉___ _kg (结果保留1位小数)

已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
金属离子 | Fe3+ | Fe2+ | In3+ |
开始沉淀pH(离子浓度为0.1mol·L-1时) | 1.3 | 6 | 3 |
完全沉淀pH | 2.7 | 8 | 4.3 |
(1)In2O3中In的化合价是
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为
 ,该反应的离子方程式为
,该反应的离子方程式为③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为

④“中浸渣”的主要成分为In(OH)3、
(3)萃取时,发生反应In3+ +3H2A2
 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。①反萃取时,宜选用的试剂X为
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有
(4)“置换”后的滤液可返回
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉
您最近一年使用:0次
名校
6 . 卤族元素单质及其化合物应用广泛。 具有与卤素单质相似的化学性质。
具有与卤素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成硫酰氟(
反应生成硫酰氟( )。
)。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37.
与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37. 通入
通入 酸性溶液中可制得黄绿色气体
酸性溶液中可制得黄绿色气体 ,该气体常用作自来水消毒剂。工业用
,该气体常用作自来水消毒剂。工业用 制备
制备 的热化学方程式为
的热化学方程式为

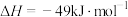 。下列关于反应
。下列关于反应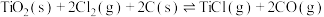 的说法
的说法不正确 的是
 具有与卤素单质相似的化学性质。
具有与卤素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成硫酰氟(
反应生成硫酰氟( )。
)。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37.
与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37. 通入
通入 酸性溶液中可制得黄绿色气体
酸性溶液中可制得黄绿色气体 ,该气体常用作自来水消毒剂。工业用
,该气体常用作自来水消毒剂。工业用 制备
制备 的热化学方程式为
的热化学方程式为

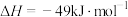 。下列关于反应
。下列关于反应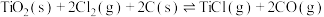 的说法
的说法A.保持其他条件不变,平衡时升高温度, |
B.保持其他条件不变,平衡时通入 ,达到新平衡时 ,达到新平衡时 变小 变小 |
C.反应生成1mol ,转移电子数目为 ,转移电子数目为 |
D.及时分离出CO,有利于 生成 生成 |
您最近一年使用:0次
名校
7 . 钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是 、
、 ,含有的杂质有
,含有的杂质有 、
、 及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
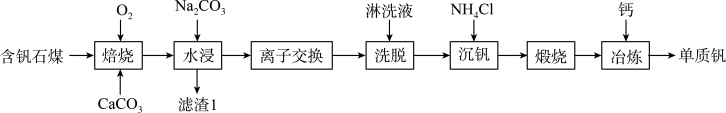
已知:
①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
② ,
, ,
, 远大于
远大于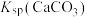 。
。
回答下列问题:
(1)为了提高“焙烧”效率,可采取的措施有___________ 、___________ 。
(2)“焙烧”时, 、
、 都转化为
都转化为 ,写出
,写出 转化为
转化为 的化学方程式:
的化学方程式:___________ 。
(3)“水浸”加入 调节溶液的pH为8.5,可完全除去的金属离子有
调节溶液的pH为8.5,可完全除去的金属离子有___________ ,部分除去的金属离子有___________ 。“水浸”加入过量 不能使
不能使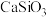 完全转化为
完全转化为 ,原因是
,原因是___________ 。
(4)“离子交换”与“洗脱”可表示为 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂, 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用___________ 。
(5)“沉钒”过程析出 晶体,需要加入过量
晶体,需要加入过量 ,目的是
,目的是___________ 。
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是___________(填字母)。
 、
、 ,含有的杂质有
,含有的杂质有 、
、 及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
已知:
①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
| 金属离子 |  |  |  |  |
| 开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
 ,
, ,
, 远大于
远大于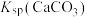 。
。回答下列问题:
(1)为了提高“焙烧”效率,可采取的措施有
(2)“焙烧”时,
 、
、 都转化为
都转化为 ,写出
,写出 转化为
转化为 的化学方程式:
的化学方程式:(3)“水浸”加入
 调节溶液的pH为8.5,可完全除去的金属离子有
调节溶液的pH为8.5,可完全除去的金属离子有 不能使
不能使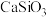 完全转化为
完全转化为 ,原因是
,原因是(4)“离子交换”与“洗脱”可表示为
 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂, 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(5)“沉钒”过程析出
 晶体,需要加入过量
晶体,需要加入过量 ,目的是
,目的是(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是___________(填字母)。
| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
解题方法
8 . 化合物X由四种元素组成,按如下流程进行实验。混合气体A由气体E和元素种类相同的另两种气体组成,且气体C的平均相对分子质量为8.5。混合物B中有两种固体。
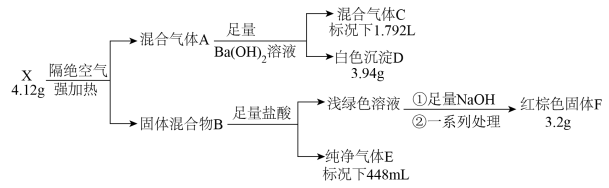
请回答:
(1)组成X的四种元素为_______ ;X的化学式为_______ 。
(2)写出由X到A的化学方程式_______ 。
(3)用盐酸溶解固体F,滴加一定量KSCN溶液,得到血红色溶液Y。往溶液Y中加入一定量KCl固体,溶液Y颜色变淡,请结合离子方程式说明原因_______ 。
(4)设计实验检验混合气体A中相对分子量较小的两种气体_______ 。

请回答:
(1)组成X的四种元素为
(2)写出由X到A的化学方程式
(3)用盐酸溶解固体F,滴加一定量KSCN溶液,得到血红色溶液Y。往溶液Y中加入一定量KCl固体,溶液Y颜色变淡,请结合离子方程式说明原因
(4)设计实验检验混合气体A中相对分子量较小的两种气体
您最近一年使用:0次
解题方法
9 . 某铜矿酸性废水除去不溶性固体杂质后,仍含有c(H+)=0.1mol•L-1,c(Cu2+)=0.05mol•L-1,需净化处理。
已知:①含铜污水的排放标准为pH=7,c(Cu2+)≤1×10-7mol•L-1。
②Ksp[Cu(OH)2]=2.2×10-20,Ksp(CuS)=6.4×10-36,Ksp(FeS)=6.3×10-18;Kb(NH3•H2O)=1.7×10-25,Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.0×10-15。
(1)中和沉淀法处理。
①向酸性废水中加入氨水,调节pH,溶液中铜的去除率与pH关系如图所示。则pH由7到10时,铜的去除率下降的主要原因为_______ (用离子方程式表示)。

②若加入石灰乳处理废水,结合计算判断生成氢氧化铜沉淀能否达到排放标准______ (写出计算过程)。
(2)硫化物沉淀法处理。
①加入Na2S处理废水,pH=7时,Na2S溶液中硫元素的主要存在的微粒为_______ 。
②用FeS处理含铜废水比Na2S效果好。请通过必要的计算和说明采用FeS处理的优点的原因______ 。
(3)溶剂萃取法。用萃取剂RH可萃取废水中的铜离子,再加入20%的硫酸进行反萃取。
①实验室进行萃取操作时,振荡静置后,需对分液漏斗放气,正确放气的图示为_______ (填标号)。
A.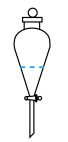 B.
B. 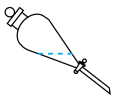 C.
C.
②萃取时,适度增大溶液的pH,Cu2+萃取率升高的原因是_______ 。
(4)实验中需测定废液中铜离子含量。
已知:2Cu2++4I-=2CuI↓+I2,I2+2S2O =2I-+S4O
=2I-+S4O 。
。
请运用上述原理完成测定某弱酸性溶液中铜离子含量的实验方案:量取25.00mL废水于锥形瓶中,_______ (实验中须使用的试剂:0.1mol•L-1KI溶液、0.05000mol•L-1Na2S2O3标准溶液、0.5%淀粉溶液)。
已知:①含铜污水的排放标准为pH=7,c(Cu2+)≤1×10-7mol•L-1。
②Ksp[Cu(OH)2]=2.2×10-20,Ksp(CuS)=6.4×10-36,Ksp(FeS)=6.3×10-18;Kb(NH3•H2O)=1.7×10-25,Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.0×10-15。
(1)中和沉淀法处理。
①向酸性废水中加入氨水,调节pH,溶液中铜的去除率与pH关系如图所示。则pH由7到10时,铜的去除率下降的主要原因为

②若加入石灰乳处理废水,结合计算判断生成氢氧化铜沉淀能否达到排放标准
(2)硫化物沉淀法处理。
①加入Na2S处理废水,pH=7时,Na2S溶液中硫元素的主要存在的微粒为
②用FeS处理含铜废水比Na2S效果好。请通过必要的计算和说明采用FeS处理的优点的原因
(3)溶剂萃取法。用萃取剂RH可萃取废水中的铜离子,再加入20%的硫酸进行反萃取。
①实验室进行萃取操作时,振荡静置后,需对分液漏斗放气,正确放气的图示为
A.
 B.
B.  C.
C.
②萃取时,适度增大溶液的pH,Cu2+萃取率升高的原因是
(4)实验中需测定废液中铜离子含量。
已知:2Cu2++4I-=2CuI↓+I2,I2+2S2O
 =2I-+S4O
=2I-+S4O 。
。请运用上述原理完成测定某弱酸性溶液中铜离子含量的实验方案:量取25.00mL废水于锥形瓶中,
您最近一年使用:0次
10 . 利用某一工业钴渣(主要成分为 ,含少量
,含少量 、
、 、MgO、CuO)制备金属钴的流程如图所示:
、MgO、CuO)制备金属钴的流程如图所示:
①沉淀1为黄钠铁矾,化学式为: 。
。
②当某离子浓度 时认为沉淀完全,
时认为沉淀完全, ,
, ,
, ,
, ,
,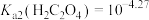
③氧化性:
(1)“浸出”过程中 元发生反应的离子方程式为
元发生反应的离子方程式为_______ ,用盐酸代替硫酸的缺点是_______ 。
(2)“浸出液”中加入 的作用是
的作用是_______ ,试剂a为_______ 。
(3)有机萃取剂用HR表示,发生萃取的反应可表示为 ,为回收
,为回收 ,可向有机相中加入一定浓度的
,可向有机相中加入一定浓度的 ,将其反萃取到水相,其原理是
,将其反萃取到水相,其原理是_______ 。
(4)沉淀2为 ,当
,当 恰好沉淀完全时,溶液中HF浓度为
恰好沉淀完全时,溶液中HF浓度为 ,则此时溶液的pH=
,则此时溶液的pH=_______ 。用 溶液沉钴,其水溶液中存在反应
溶液沉钴,其水溶液中存在反应 ,其平衡常数为K,则K=
,其平衡常数为K,则K=_______ 。
(5)已知氧化性: 。工业上采用惰性电极电解
。工业上采用惰性电极电解 溶液制取钴,不用
溶液制取钴,不用 溶液代替
溶液代替 溶液的原因是
溶液的原因是_______ 。
 ,含少量
,含少量 、
、 、MgO、CuO)制备金属钴的流程如图所示:
、MgO、CuO)制备金属钴的流程如图所示: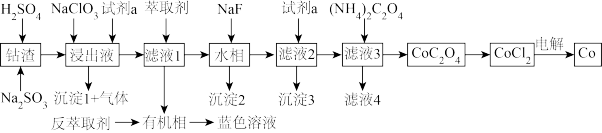
①沉淀1为黄钠铁矾,化学式为:
 。
。②当某离子浓度
 时认为沉淀完全,
时认为沉淀完全, ,
, ,
, ,
, ,
,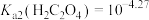
③氧化性:

(1)“浸出”过程中
 元发生反应的离子方程式为
元发生反应的离子方程式为(2)“浸出液”中加入
 的作用是
的作用是(3)有机萃取剂用HR表示,发生萃取的反应可表示为
 ,为回收
,为回收 ,可向有机相中加入一定浓度的
,可向有机相中加入一定浓度的 ,将其反萃取到水相,其原理是
,将其反萃取到水相,其原理是(4)沉淀2为
 ,当
,当 恰好沉淀完全时,溶液中HF浓度为
恰好沉淀完全时,溶液中HF浓度为 ,则此时溶液的pH=
,则此时溶液的pH= 溶液沉钴,其水溶液中存在反应
溶液沉钴,其水溶液中存在反应 ,其平衡常数为K,则K=
,其平衡常数为K,则K=(5)已知氧化性:
 。工业上采用惰性电极电解
。工业上采用惰性电极电解 溶液制取钴,不用
溶液制取钴,不用 溶液代替
溶液代替 溶液的原因是
溶液的原因是
您最近一年使用:0次



