解题方法
1 . 下列说法错误的是
A.反应 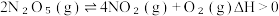 能自发进行的原因为△S>0 能自发进行的原因为△S>0 |
B. 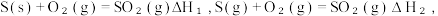 则 则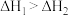 |
| C.合成氨反应采取循环操作的主要原因是为了提高化学反应速率 |
D.一定温度下,对 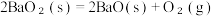 平衡体系缩小体积,再次达到平衡时 c 平衡体系缩小体积,再次达到平衡时 c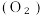 不变 不变 |
您最近一年使用:0次
解题方法
2 . 甲醇是重要的化工原料,工业上可利用 生产甲醇,同时可降低温室气体二氧化碳的排放。
生产甲醇,同时可降低温室气体二氧化碳的排放。
已知:①
②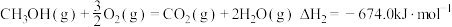
③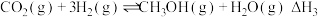
(1)
___________  ,反应③在
,反应③在___________ (填“高温”、“低温”或“任何温度”)下能自发进行。
(2)下列措施中,能提高 平衡转化率的是___________(填标号)。
平衡转化率的是___________(填标号)。
(3)在一密闭容器中加入 和
和 ,在一定条件下进行反应③,测得CO2(g)的平衡转化率与温度、压强的关系如图所示。
,在一定条件下进行反应③,测得CO2(g)的平衡转化率与温度、压强的关系如图所示。
___________ (填“>”“=”或“<”,下同) ,理由是
,理由是___________ 。
②当压强为 时,B点
时,B点
___________  。
。
③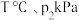 下,
下, 的平衡体积分数为
的平衡体积分数为___________ %,该条件下反应③的压强平衡常数
___________  (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
 生产甲醇,同时可降低温室气体二氧化碳的排放。
生产甲醇,同时可降低温室气体二氧化碳的排放。已知:①

②
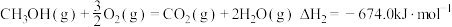
③
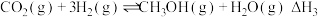
(1)

 ,反应③在
,反应③在(2)下列措施中,能提高
 平衡转化率的是___________(填标号)。
平衡转化率的是___________(填标号)。| A.压缩容器体积 | B.将 液化分离出来 液化分离出来 | C.恒容下充入 | D.使用高效催化剂 |
(3)在一密闭容器中加入
 和
和 ,在一定条件下进行反应③,测得CO2(g)的平衡转化率与温度、压强的关系如图所示。
,在一定条件下进行反应③,测得CO2(g)的平衡转化率与温度、压强的关系如图所示。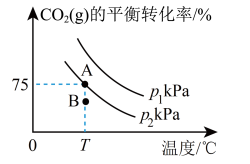

 ,理由是
,理由是②当压强为
 时,B点
时,B点
 。
。③
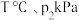 下,
下, 的平衡体积分数为
的平衡体积分数为
 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
您最近一年使用:0次
名校
解题方法
3 . 光催化是新发展的一个催化技术,TiO2是目前研究成功的应用广泛的光催化剂,它是由金红石矿(主要成分为TiO2)先制备为TiCl4,再转化为纯TiO2。
请根据表中数据作答:
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行___________ ?
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向___________ 。
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向___________ 。
| 物种 | TiO2(s) | TiCl4(g) | Cl2(g) | O2(g) | C(s) | CO(g) |
| ΔrΗΘm /kJ∙molˉ1 | –944.7 | –763.2 | 0 | 0 | 0 | –110.5 |
| SΘm/J∙molˉ1∙Kˉ1 | 55.02 | 354.9 | 223.1 | 205.1 | 5.74 | 197.7 |
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向
您最近一年使用:0次
4 . 甲烷水蒸气重整制取合成气的反应如下: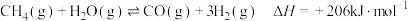 。请回答下列问题:
。请回答下列问题:
(1)上述反应能自发进行的理由是___________ ,条件是___________ (填“低温”“高温”或“任何条件”)。
(2)向容积为2L的密闭容器中,按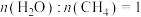 投料,
投料,
a.保持温度为 时,测得
时,测得 的浓度随时间变化曲线如图1所示。
的浓度随时间变化曲线如图1所示。
b.其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后, 的转化率随反应温度的变化如图2所示。
的转化率随反应温度的变化如图2所示。

①结合图1,写出反应达到平衡的过程中的能量变化:吸收___________ 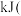 用含有x、y的代数式表示)。
用含有x、y的代数式表示)。
②在图1中画出:起始条件相同,保持温度为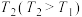 时,
时,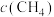 随时间的变化曲线
随时间的变化曲线___________ 。
③根据图2判断: 的转化率:
的转化率: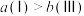 ,原因是
,原因是___________ 。
(3)①设起始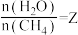 ,在恒压
,在恒压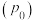 下,平衡时
下,平衡时 与
与 和
和 (温度)的关系如图3所示:[其中
(温度)的关系如图3所示:[其中 为
为 的体积分数]
的体积分数]
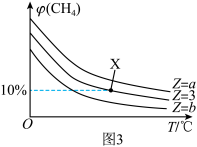
比较图3中a、b与3的大小关系___________ (请按从大到小的顺序书写)。
②对于气相反应,用某组分B的平衡压强 代替物质的量浓度
代替物质的量浓度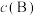 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如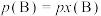 ,p为平衡总压强,
,p为平衡总压强,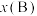 为平衡系统中B的物质的量分数。则图3中X点时,
为平衡系统中B的物质的量分数。则图3中X点时,
___________ 。
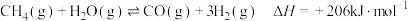 。请回答下列问题:
。请回答下列问题:(1)上述反应能自发进行的理由是
(2)向容积为2L的密闭容器中,按
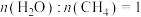 投料,
投料,a.保持温度为
 时,测得
时,测得 的浓度随时间变化曲线如图1所示。
的浓度随时间变化曲线如图1所示。b.其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,
 的转化率随反应温度的变化如图2所示。
的转化率随反应温度的变化如图2所示。
①结合图1,写出反应达到平衡的过程中的能量变化:吸收
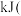 用含有x、y的代数式表示)。
用含有x、y的代数式表示)。②在图1中画出:起始条件相同,保持温度为
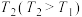 时,
时,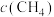 随时间的变化曲线
随时间的变化曲线③根据图2判断:
 的转化率:
的转化率: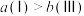 ,原因是
,原因是(3)①设起始
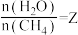 ,在恒压
,在恒压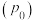 下,平衡时
下,平衡时 与
与 和
和 (温度)的关系如图3所示:[其中
(温度)的关系如图3所示:[其中 为
为 的体积分数]
的体积分数]
比较图3中a、b与3的大小关系
②对于气相反应,用某组分B的平衡压强
 代替物质的量浓度
代替物质的量浓度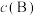 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如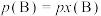 ,p为平衡总压强,
,p为平衡总压强,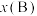 为平衡系统中B的物质的量分数。则图3中X点时,
为平衡系统中B的物质的量分数。则图3中X点时,
您最近一年使用:0次
解题方法
5 . 反应 可用于纯硅的制备。下列有关该反应的说法正确的是
可用于纯硅的制备。下列有关该反应的说法正确的是
 可用于纯硅的制备。下列有关该反应的说法正确的是
可用于纯硅的制备。下列有关该反应的说法正确的是A.该反应 、 、 |
B.该反应的平衡常数 |
C.高温下反应每生成 需消耗 需消耗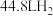 |
D.用E表示键能,该反应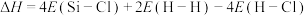 |
您最近一年使用:0次
解题方法
6 . 下列各说法中,正确的是
| A.能够自发进行的反应不一定都是放热反应 |
| B.能够自发进行的反应就一定能够发生并完成 |
| C.同一物质:固体→液体→气体变化是焓减和熵增的过程 |
| D.-10℃的水结成冰,可用熵变判据来解释该变化过程的自发性 |
您最近一年使用:0次
解题方法
7 . 当∆H_____ 0,∆S_____ 0时,反应在低温条件下才自发进行;
当∆H_____ 0,∆S_____ 0时,反应在高温条件下才能自发进行;
当∆H_____ 0,∆S_____ 0时,反应在任意温度下都能自发进行;
当∆H_____ 0,∆S_____ 0时,反应在任意温度下都不能自发进行。
当∆H
当∆H
当∆H
您最近一年使用:0次
解题方法
8 . 焓变和熵变综合判据为∆G=_____ 。∆G_____ 0反应正向能自发进行;∆G_____ 0反应达到平衡状态;∆G_____ 0反应正向不能自发进行。
您最近一年使用:0次
解题方法
9 . 自发进行的化学反应大多数是熵_____ 的反应,也有些是熵_____ 的反应。(填“增加”或“减小”)
您最近一年使用:0次
解题方法
10 . 自发进行的化学反应大多数是_____ 反应,也有些是_____ 反应。(填“吸热”或“放热”)
您最近一年使用:0次



