解题方法
1 . Ⅰ.习近平总书记十分重视生态环境保护,多次对生态文明建设作出重要指示,其中研究 、
、 、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
(1)处理含CO、 烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
①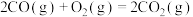
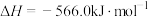
②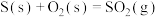

则CO与 反应生成S的热化学方程式是
反应生成S的热化学方程式是_______ 。
(2)在一绝热体系且容积固定的密闭容器中,用 催化还原
催化还原 也可以消除氮氧化物的污染,其中发生化学反应之一为:
也可以消除氮氧化物的污染,其中发生化学反应之一为: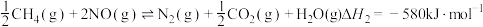 ,能说明上反应达到平衡状态的是
,能说明上反应达到平衡状态的是_______ 。
a.平均摩尔质量不变 b. 和
和 的体积比保持不变
的体积比保持不变
c.体系压强保持不变 d.每生成1mol 同时生成2molNO
同时生成2molNO
Ⅱ.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(3)生产氢气:将水蒸气通过红热的炭即产生水煤气;
 ,
,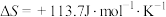 ,该反应在(填“高温”或“低温”或“任何温度”)
,该反应在(填“高温”或“低温”或“任何温度”)_______ 下,才能自发进行。
(4)合成氨工业中的主要反应是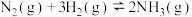
 ,从温度和压强的角度回答:要加快合成氨的反应速率应选择
,从温度和压强的角度回答:要加快合成氨的反应速率应选择_______ ;要提高氨的产率应选择_______ 。
 、
、 、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。
、CO等气体的无害化处理对治埋大气污染、建设生态文明具有重要意义。(1)处理含CO、
 烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气的一种方法是将其在催化剂作用下转化为单质S。已知:①
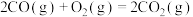
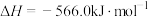
②
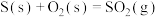

则CO与
 反应生成S的热化学方程式是
反应生成S的热化学方程式是(2)在一绝热体系且容积固定的密闭容器中,用
 催化还原
催化还原 也可以消除氮氧化物的污染,其中发生化学反应之一为:
也可以消除氮氧化物的污染,其中发生化学反应之一为: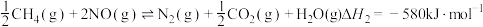 ,能说明上反应达到平衡状态的是
,能说明上反应达到平衡状态的是a.平均摩尔质量不变 b.
 和
和 的体积比保持不变
的体积比保持不变c.体系压强保持不变 d.每生成1mol
 同时生成2molNO
同时生成2molNOⅡ.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(3)生产氢气:将水蒸气通过红热的炭即产生水煤气;

 ,
,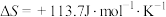 ,该反应在(填“高温”或“低温”或“任何温度”)
,该反应在(填“高温”或“低温”或“任何温度”)(4)合成氨工业中的主要反应是
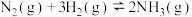
 ,从温度和压强的角度回答:要加快合成氨的反应速率应选择
,从温度和压强的角度回答:要加快合成氨的反应速率应选择
您最近一年使用:0次
名校
解题方法
2 . 2023年10月8日第19届亚运会在杭州圆满闭幕,本届亚运会秉持“绿色、智能、节俭、文明”的办会理念。下列说法正确的是
| A.零碳甲醇作为本届亚运会的火炬燃料,甲醇的燃烧(常温条件测定)属于熵增的放热反应 |
| B.吉祥物“江南忆”机器人所采用芯片的主要成分为硅单质 |
| C.亚运会纪念章“琮琮”是由锌合金镀金制成的,锌合金镀金属于合成材料 |
| D.场馆全部使用绿色能源,打造首届碳中和亚运会,碳中和就是不排放二氧化碳 |
您最近一年使用:0次
名校
解题方法
3 . 神舟十五号顺利发射升空,标志着我国航天事业的飞速发展。
Ⅰ.火箭推进剂的研究是航天工业中的重要课题,常见推进剂的燃料包括汽油液肼(N2H4)、液氢等,具有不同的推进效能。回答下列问题:
(1)火箭推进剂可用N2H4作燃料,N2O4作氧化剂,反应的热化学方程式可表示为2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H1。
相关物质的摩尔生成焓∆HfHm如下表所示。
注:一定温度下,由元素的最稳定单质生成1mol纯物质的热效应称为该物质的摩尔生成焓,用∆HfHm表示。如N2H4(1)的摩尔生成焓:N2(g)+2H2(g)=N2H4(l) ∆HfHm =+165.8kJ/mol
①∆H1=___________ kJ/mol。
②结合化学反应原理分析,N2H4(l)作推近剂燃料可与N2O4(g)自发进行反应的原因是___________ 。
(2)火箭推进器内氢氧燃烧的简化反应历程如下图所示,分析其反应机理。
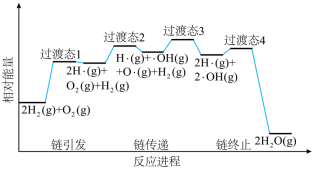
该历程分步进行,其中氢氧燃烧决速步对应的反应方程式为___________ 。
Ⅱ.在温度T下,容积固定的密闭容器中充入3 mol NO和2 mol H2发生2H2(g)+2NO(g) N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
(3)则NO的平衡转化率α(NO)=___________ (结果保留三位有效数字),该反应的平衡常数Kp=___________ (用含P0的代数式表示)
Ⅰ.火箭推进剂的研究是航天工业中的重要课题,常见推进剂的燃料包括汽油液肼(N2H4)、液氢等,具有不同的推进效能。回答下列问题:
(1)火箭推进剂可用N2H4作燃料,N2O4作氧化剂,反应的热化学方程式可表示为2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H1。
相关物质的摩尔生成焓∆HfHm如下表所示。
| 物质 | N2O4(g) | N2H4(l) | H2O(g) |
| 摩尔生成焓∆HfHm(kJ/mol) | +10.8 | +165.8. | -242.0 |
①∆H1=
②结合化学反应原理分析,N2H4(l)作推近剂燃料可与N2O4(g)自发进行反应的原因是
(2)火箭推进器内氢氧燃烧的简化反应历程如下图所示,分析其反应机理。

该历程分步进行,其中氢氧燃烧决速步对应的反应方程式为
Ⅱ.在温度T下,容积固定的密闭容器中充入3 mol NO和2 mol H2发生2H2(g)+2NO(g)
 N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,
N2(g)+2H2O(g),起始压强为p0,一段时间后,反应达到平衡,此时压强p=0.9p0,(3)则NO的平衡转化率α(NO)=
您最近一年使用:0次
名校
4 . 下列有关化学平衡和速率的说法正确的是
| A.H2、I2、HI平衡混合气体加压后颜色不变 |
| B.恒温恒压的密闭体系中进行的合成氨反应,达到平衡后,充入惰性气体,氨气的体积分数增大 |
| C.红棕色的NO2气体加压后,颜色先变深,后变浅 |
| D.任意温度下都能自发的反应一定是放热和熵减的反应 |
您最近一年使用:0次
名校
5 . 已知:ΔG=ΔH-TΔS,当ΔG<0,反应能自发进行,ΔG>0反应不能自发进行。下列说法中正确的是
| A.熵增加且放热的反应一定是自发反应 |
| B.非自发反应在任何条件下都不能发生 |
| C.自发反应一定是熵增加的反应,非自发反应一定是熵减小或不变的反应 |
| D.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 |
您最近一年使用:0次
2023-12-27更新
|
103次组卷
|
2卷引用:宁夏开元学校2023-2024学年高二上学期期末考试化学试题
6 . 2023年8月24日,日本向海洋中排放了大量的核废水,这一举动引起了国际社会的广泛关注和讨论,其中最为担忧的是核废水会对海洋中的物种造成变异和影响。下列有关说法正确的是
| A.核电站发电的核反应属于放热反应 |
| B.核电站发电是将化学能转化为电能和热能 |
| C.核废水扩散到海水中的过程属于熵增过程 |
D.核废水中含 , , 基态原子的轨道表示式为 基态原子的轨道表示式为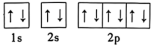 |
您最近一年使用:0次
2023-12-24更新
|
304次组卷
|
4卷引用:宁夏银川一中2023-2024学年高二上学期期末考试化学试题
名校
解题方法
7 . 下列推论正确的是
| A.S(g)+O2(g)=SO2(g) ΔH1,S(s)+O2(g)=SO2(g) ΔH2;则:ΔH1>ΔH2 |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.4kJ/mol,则:含20gNaOH的溶液与稀盐酸完全反应,放出的热量为28.7kJ |
| C.C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ/mol,则:金刚石比石墨稳定 |
| D.CaCO3(s)=CaO(s)+CO2(g) ΔH>0,ΔS>0,则:该反应任何温度下都能自发进行 |
您最近一年使用:0次
名校
8 . 关于反应
 ,下列说法正确的是
,下列说法正确的是

 ,下列说法正确的是
,下列说法正确的是| A.该反应在高温条件下可以自发进行 |
| B.向反应容器中加入催化剂,反应自发进行的温度会改变 |
| C.恒容条件下,通入He气,压强会增大,反应的速率会加快 |
D.恒容条件下,可通入过量的 气体来提高 气体来提高 转化率 转化率 |
您最近一年使用:0次
2023-12-16更新
|
110次组卷
|
2卷引用:宁夏六盘山高级中学2023-2024学年高二上学期第二次月考化学试题
名校
解题方法
9 . 下列表述中正确的是
| A.任何能使熵值增大的过程都能自发进行 |
B.已知热化学方程式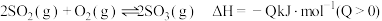 ,则将 ,则将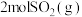 和 和 置于一密闭容器中充分反应后放出 置于一密闭容器中充分反应后放出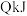 的热量 的热量 |
| C.自发反应一定熵增大,非自发反应一定熵减小或不变 |
| D.使用催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率增大 |
您最近一年使用:0次
2023-12-13更新
|
151次组卷
|
3卷引用:宁夏育才中学2023-2024学年高二上学期1月期末化学试题
名校
10 . 下列有关叙述正确的是
①工业上通常采用铁触媒、400~500℃和10MPa~30Mpa的条件下合成氨
②等体积、等pH的盐酸和醋酸,分别与等浓度的NaOH反应,醋酸消耗的NaOH体积大
③化学平衡常数变化,化学平衡不一定发生移动
④通过压缩体积增大压强,可以提高单位体积内活化分子百分数,从而提高反应速率
⑤在中和反应反应热的测定实验中,每组实验至少三次使用温度计
⑥反应CaSO4(s)=CaO(s)+SO3(g) ∆H>0在高温下能自发进行
①工业上通常采用铁触媒、400~500℃和10MPa~30Mpa的条件下合成氨
②等体积、等pH的盐酸和醋酸,分别与等浓度的NaOH反应,醋酸消耗的NaOH体积大
③化学平衡常数变化,化学平衡不一定发生移动
④通过压缩体积增大压强,可以提高单位体积内活化分子百分数,从而提高反应速率
⑤在中和反应反应热的测定实验中,每组实验至少三次使用温度计
⑥反应CaSO4(s)=CaO(s)+SO3(g) ∆H>0在高温下能自发进行
| A.①②③⑥ | B.①②⑤⑥ | C.②④⑤⑥ | D.①③④⑤ |
您最近一年使用:0次
2023-12-06更新
|
126次组卷
|
3卷引用:宁夏银川一中2023-2024学年高二上学期期末考试化学试题



