1 . 已知某反应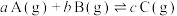 ,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且
,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且 ,
, 表示转化率)。下列说法正确的是
表示转化率)。下列说法正确的是
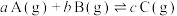 ,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且
,在其他条件不变的情况下,改变某一条件后的化学平衡图像如图(T表示温度,p表示压强且 ,
, 表示转化率)。下列说法正确的是
表示转化率)。下列说法正确的是
A. , , | B. , , |
C. , , | D. , , |
您最近一年使用:0次
名校
2 . 回答下列问题:
(1)某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、B、C均为气体)。
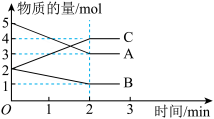
①该反应的化学方程式为_______ 。
②反应开始至2min时,B的平均反应速率为_______ 。
(2)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积气体所需的时间。
①请完成此实验设计:其中
_______ ,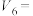
_______ 。
②该同学最后得出的结论为当加入少量 溶液时,生成氢气的速率会大大提高,但当加入的
溶液时,生成氢气的速率会大大提高,但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:_______ 。
(3)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO: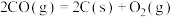 。已知该反应的
。已知该反应的 ,该设想能否实现?
,该设想能否实现?_______ (填“能”或“否”),依据是:_______ 。
(1)某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、B、C均为气体)。

①该反应的化学方程式为
②反应开始至2min时,B的平均反应速率为
(2)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积气体所需的时间。
实验 混合溶液 | A | B | C | D | E | F |
4 mol·L  溶液/mL 溶液/mL | 30 |  |  |  |  | 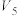 |
饱和 溶液/mL 溶液/mL | 0 | 0.5 | 2.5 | 5 |  | 20 |
 /mL /mL | 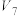 | 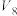 |  | 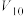 | 10 | 0 |

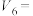
②该同学最后得出的结论为当加入少量
 溶液时,生成氢气的速率会大大提高,但当加入的
溶液时,生成氢气的速率会大大提高,但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:(3)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
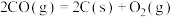 。已知该反应的
。已知该反应的 ,该设想能否实现?
,该设想能否实现?
您最近一年使用:0次
名校
3 . 一碳化学是以分子中只含一个碳原子的化合物为原料生产化工产品的方法。合成气( 和
和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
I:
II:
III:
(1)当反应I达到平衡后,下列措施可提高正反应速率的是_______(填标号)。
(2)若在恒温恒容容器中仅发生反应II,则下列能说明反应达到平衡状态的是_______。
(3)向容积为 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应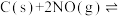
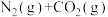 ,
, 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。
① 内,以
内,以 表示的该反应速率
表示的该反应速率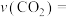
___________ ,最终达平衡时 的转化率
的转化率
___________ ,该温度 ℃下的平衡常数
℃下的平衡常数
___________ 。
②保持温度 ℃不变,向该
℃不变,向该 密闭容器中加入该四种反应混合物各
密闭容器中加入该四种反应混合物各 ,该时刻,正、逆反应速率的大小关系为:
,该时刻,正、逆反应速率的大小关系为: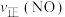
___________ 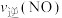 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)已知4CO(g) +2NO2(g) 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
 和
和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:I:

II:

III:

(1)当反应I达到平衡后,下列措施可提高正反应速率的是_______(填标号)。
| A.加入焦炭 | B.通入CO | C.升高温度 | D.分离出氢气 |
| A.容器内气体的压强不变 |
| B.容器内气体的总质量不变 |
| C.容器内气体的平均相对分子质量不变 |
D.单位时间内,每有2 mol  键断裂,同时有1 mol 键断裂,同时有1 mol  键断裂 键断裂 |
 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应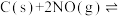
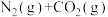 ,
, 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。| 条件 | 保持温度为 /℃ /℃ | ||||||
| 时间 | 0 | 5min | 10min | 15min | 20min | 25min | 30min |
 物质的量 物质的量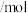 | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
 物质的量 物质的量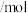 | 0 | 0.3 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
 内,以
内,以 表示的该反应速率
表示的该反应速率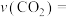
 的转化率
的转化率
 ℃下的平衡常数
℃下的平衡常数
②保持温度
 ℃不变,向该
℃不变,向该 密闭容器中加入该四种反应混合物各
密闭容器中加入该四种反应混合物各 ,该时刻,正、逆反应速率的大小关系为:
,该时刻,正、逆反应速率的大小关系为: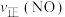
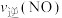 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)已知4CO(g) +2NO2(g)
 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
您最近一年使用:0次
2023-12-14更新
|
171次组卷
|
3卷引用:甘肃省天水市第一中学2023-2024学年高二下学期开学化学试题
4 . 在恒温下,向容积为2L的恒容容器中加入一定量的碳单质和2molH2O(g),初始压强为105Pa。发生反应: ∆H>0。经过2min后达到平衡,容器的压强增加了20%。
∆H>0。经过2min后达到平衡,容器的压强增加了20%。
(1)该反应自发进行的条件是__________ 。(填“高温”或“低温”或“任意条件”)
(2)2min内H2O的平均反应速率为__________ mol/(L·min)。
(3)2min平衡时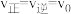 ,采取下列措施后,使
,采取下列措施后,使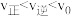 的是__________。
的是__________。
(4)平衡常数Kp=__________ Pa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)下列说法正确的是__________。
 ∆H>0。经过2min后达到平衡,容器的压强增加了20%。
∆H>0。经过2min后达到平衡,容器的压强增加了20%。(1)该反应自发进行的条件是
(2)2min内H2O的平均反应速率为
(3)2min平衡时
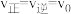 ,采取下列措施后,使
,采取下列措施后,使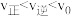 的是__________。
的是__________。| A.恒温恒容下,除去部分H2O | B.降低温度 |
| C.恒温恒容下,充入Ar | D.恒温恒压下,充入Ar |
(5)下列说法正确的是__________。
| A.增加碳单质,可以加快该反应速率 |
| B.2min时,H2O的转化率为20% |
| C.当混合气体的平均摩尔质量不再变化时,可以判断该反应达到了平衡 |
| D.平衡后向体系内补加0.4molH2O(g)和0.4molCO(g),反应向逆反应方向进行 |
您最近一年使用:0次
2023-12-11更新
|
176次组卷
|
2卷引用:甘肃省武威第七中学2023-2024学年高二上学期期末考试化学试题
5 . 二甲醚(DME)被誉为“21世纪的清洁燃料”,由合成气制备二甲醚的主要原理如下:
①
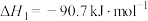

②
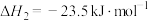

③
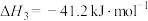

回答下列问题:
(1)反应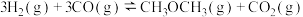 的
的
___________  ;该反应在
;该反应在___________ (填“低温”或“高温”)下能够自发进行,反应的平衡常数K=___________ (用含 、
、 、
、 的式子表示)。
的式子表示)。
(2)将合成气以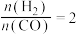 通入1L的反应器中,一定条件下发生反应:
通入1L的反应器中,一定条件下发生反应: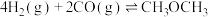

 ,其中CO的平衡转化率随温度、压强的变化关系如下图所示,下列说法正确的是(填字母)
,其中CO的平衡转化率随温度、压强的变化关系如下图所示,下列说法正确的是(填字母)___________ 。
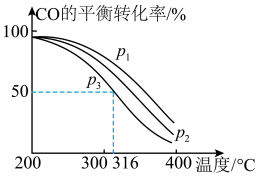
A.
B.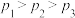
C.若在 和316℃时,起始时
和316℃时,起始时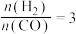 ,则平衡时,
,则平衡时,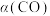 小于50%
小于50%
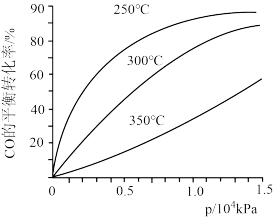
(3)CO合成甲醇时,在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、 kPa左右,选择此压强的理由是
kPa左右,选择此压强的理由是___________ 。
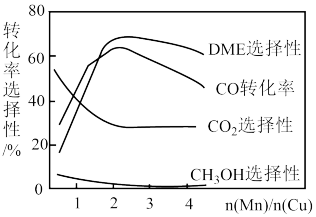
(4)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和 制备二甲醚(DME)。观察下图,当
制备二甲醚(DME)。观察下图,当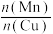 约为
约为___________ 时最有利于二甲醚的合成。
(5)高温时二甲醚蒸气发生分解反应: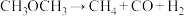 。迅速将二甲醚引入一个504℃的抽成真空的瓶中,在不同时刻测定瓶内压强
。迅速将二甲醚引入一个504℃的抽成真空的瓶中,在不同时刻测定瓶内压强 如下表:
如下表:
①该反应达到平衡状态时,二甲醚的转化率为___________ 。
②该反应的平衡常数
___________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
①

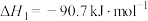

②

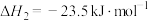

③

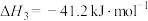

回答下列问题:
(1)反应
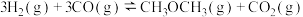 的
的
 ;该反应在
;该反应在 、
、 、
、 的式子表示)。
的式子表示)。(2)将合成气以
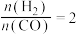 通入1L的反应器中,一定条件下发生反应:
通入1L的反应器中,一定条件下发生反应: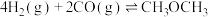

 ,其中CO的平衡转化率随温度、压强的变化关系如下图所示,下列说法正确的是(填字母)
,其中CO的平衡转化率随温度、压强的变化关系如下图所示,下列说法正确的是(填字母)
A.

B.
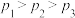
C.若在
 和316℃时,起始时
和316℃时,起始时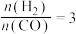 ,则平衡时,
,则平衡时,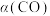 小于50%
小于50%(3)CO合成甲醇时,在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、
 kPa左右,选择此压强的理由是
kPa左右,选择此压强的理由是
(4)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和
 制备二甲醚(DME)。观察下图,当
制备二甲醚(DME)。观察下图,当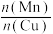 约为
约为
(5)高温时二甲醚蒸气发生分解反应:
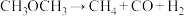 。迅速将二甲醚引入一个504℃的抽成真空的瓶中,在不同时刻测定瓶内压强
。迅速将二甲醚引入一个504℃的抽成真空的瓶中,在不同时刻测定瓶内压强 如下表:
如下表:| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
 /kPa /kPa | 50.0 | 78.0 | 92.0 | 99.0 | 100 | 100 |
②该反应的平衡常数

您最近一年使用:0次
名校
解题方法
6 . 化学反应的方向问题对于理论研究与生产实践都有重要的意义。下列说法错误的是
A. 时,熵减小 时,熵减小 |
B.恒温恒压下, 且 且 的反应一定能自发进行 的反应一定能自发进行 |
C. 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的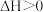 |
D.反应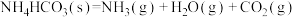 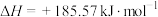 能自发进行,原因是熵增效应大于焓增效应 能自发进行,原因是熵增效应大于焓增效应 |
您最近一年使用:0次
2023-11-05更新
|
157次组卷
|
5卷引用:甘肃省酒泉市四校联考2023-2024学年高二上学期11月期中化学试题
7 . 在化学反应A(g)+B(g) 2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。

(1)Q___________ 0 (填“>”“<”或“=”)。
(2)熵变ΔS___________ 0(填“>”“<”或“=”)。
(3)该反应___________ 自发进行(填“能”或“不能”)。
(4)升高温度,平衡常数K___________ (填“增大”“减小”或“不变”),平衡向___________ 方向移动,平衡向该方向移动的理由是___________ 。
 2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
(1)Q
(2)熵变ΔS
(3)该反应
(4)升高温度,平衡常数K
您最近一年使用:0次
名校
8 . 氮化硼 是重要的无机材料,可通过下面两种反应制得:
是重要的无机材料,可通过下面两种反应制得:
反应I:
反应II:
已知反应 常温下自发,反应II常温下不自发,
常温下自发,反应II常温下不自发, 、
、 、
、 熔点分别约为2300℃、3100℃、450℃,下列说法正确的是
熔点分别约为2300℃、3100℃、450℃,下列说法正确的是
 是重要的无机材料,可通过下面两种反应制得:
是重要的无机材料,可通过下面两种反应制得:反应I:

反应II:

已知反应
 常温下自发,反应II常温下不自发,
常温下自发,反应II常温下不自发, 、
、 、
、 熔点分别约为2300℃、3100℃、450℃,下列说法正确的是
熔点分别约为2300℃、3100℃、450℃,下列说法正确的是A.反应I的, , , |
B.常温下反应I的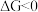 ,因此化学反应速率快 ,因此化学反应速率快 |
| C.性能优良的催化剂可使反应II在常温下自发进行 |
| D.由各物质熔点可推测在实际生产中反应I所需的温度高于反应II |
您最近一年使用:0次
名校
解题方法
9 . 化学反应进行的方向是一个比较复杂的问题。下列有关说法正确的是
A.反应 的 的 |
B. 或 或 的反应一定能自发进行 的反应一定能自发进行 |
C.  在不同状态时的熵值: 在不同状态时的熵值: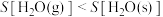 |
D.反应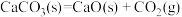  能否自发进行与温度有关 能否自发进行与温度有关 |
您最近一年使用:0次
2023-10-03更新
|
56次组卷
|
2卷引用:甘肃省白银市靖远县2023-2024学年高二上学期11月期中联考化学试题
名校
解题方法
10 . 下列不属于自发过程的是
| A | B | C | D |
 |  |  |  |
| 石墨转化为金刚石 | 冰在常温下融化 | 铁在潮湿空气中生锈 | 水从高处往低处流 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-26更新
|
35次组卷
|
3卷引用:甘肃省天祝藏族自治县第一中学2023-2024学年高二上学期9月月考化学试题



