解题方法
1 . 下列不属于自发过程的是
| A | B | C | D |
 |  |  |  |
| 水从高处往低处流 | 冰在常温下融化 | 石墨转化为金刚石 | 铁在潮湿空气中生锈 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列说法不正确的是
| A.ΔH<0、ΔS>0的反应在任何温度下都能自发进行 |
| B.NH4HCO3(s) = NH3(g)+H2O(g)+CO2(g) ΔH=+185.57 kJ/mol 能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D.自发反应也可能需要加热才能进行 |
您最近一年使用:0次
2024-03-15更新
|
35次组卷
|
2卷引用:陕西省汉中市城固县城固县第二中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
3 . 我国的能源消费结构以燃煤为主,将煤气化可减少环境污染。
(1)将煤与水蒸气在恒容密闭容器中反应,可制合成气。制备过程中的主要反应(a)、(b)的 (
( 为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
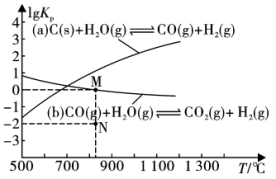
①下列能说明反应(a)
 已达到平衡状态的是
已达到平衡状态的是___________ (填字母)。
A. B.混合气体的总压强不再变化
B.混合气体的总压强不再变化
C. 不再变化 D.混合气体的密度不再变化
不再变化 D.混合气体的密度不再变化
②在容积为1L的密闭容器中充入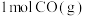 、
、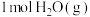 只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
___________  ;已知反应速率
;已知反应速率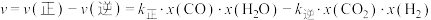 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,N处的
分别为正、逆反应速率常数,x为物质的量分数,N处的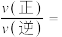
___________ 。
(2)一种新型煤气化燃烧集成制氢发生的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.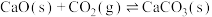

Ⅳ.
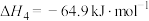
副反应:
Ⅴ.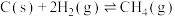
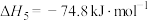
Ⅵ.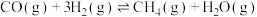
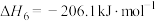
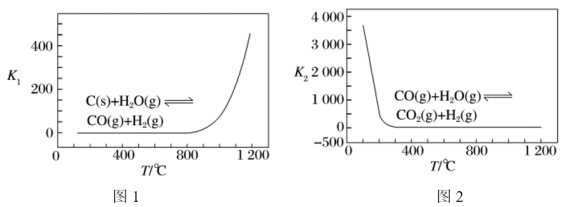
已知反应Ⅰ、Ⅱ的平衡常数 ,
, 随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。
①由反应Ⅴ和反应Ⅵ可知,
___________  ;反应Ⅰ的
;反应Ⅰ的
___________ (填“>”或“<”)0。
②温度小于800℃时, ,原因是
,原因是___________ 。
③为提高反应Ⅱ中CO的转化率,可采取的措施是___________ (写一条)。
④ 时,向密闭容器中充入
时,向密闭容器中充入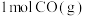 和
和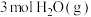 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数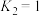 ,CO的平衡转化率为
,CO的平衡转化率为___________ 。
⑤从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是___________ 。
(1)将煤与水蒸气在恒容密闭容器中反应,可制合成气。制备过程中的主要反应(a)、(b)的
 (
( 为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
为以分压表示的平衡常数)与温度T的关系如图所示。回答下列问题:
①下列能说明反应(a)

 已达到平衡状态的是
已达到平衡状态的是A.
 B.混合气体的总压强不再变化
B.混合气体的总压强不再变化C.
 不再变化 D.混合气体的密度不再变化
不再变化 D.混合气体的密度不再变化②在容积为1L的密闭容器中充入
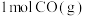 、
、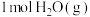 只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
只发生反应(b),反应5 min到达图中M点,请计算0~5 min内,平均反应速率
 ;已知反应速率
;已知反应速率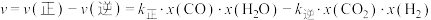 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,N处的
分别为正、逆反应速率常数,x为物质的量分数,N处的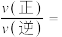
(2)一种新型煤气化燃烧集成制氢发生的主要反应如下:
Ⅰ.


Ⅱ.


Ⅲ.
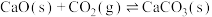

Ⅳ.

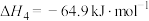
副反应:
Ⅴ.
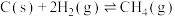
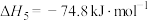
Ⅵ.
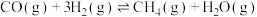
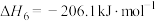
已知反应Ⅰ、Ⅱ的平衡常数
 ,
, 随温度的变化如图1、图2所示。
随温度的变化如图1、图2所示。
①由反应Ⅴ和反应Ⅵ可知,

 ;反应Ⅰ的
;反应Ⅰ的
②温度小于800℃时,
 ,原因是
,原因是③为提高反应Ⅱ中CO的转化率,可采取的措施是
④
 时,向密闭容器中充入
时,向密闭容器中充入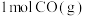 和
和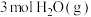 ,只发生反应Ⅱ,此时该反应的平衡常数
,只发生反应Ⅱ,此时该反应的平衡常数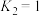 ,CO的平衡转化率为
,CO的平衡转化率为⑤从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是
您最近一年使用:0次
4 . 汽车尾气在稀土催化剂作用下通过反应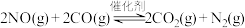 能实现转化。下列说法正确的是
能实现转化。下列说法正确的是
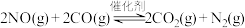 能实现转化。下列说法正确的是
能实现转化。下列说法正确的是A.该反应 |
B.该反应的平衡常数可表示为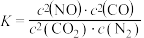 |
C.其它条件相同, 越大,CO的平衡转化率越大 越大,CO的平衡转化率越大 |
| D.若反应在恒温体积固定的条件下进行,平衡后充入氦气,压强增大,平衡正向移动 |
您最近一年使用:0次
解题方法
5 . 反应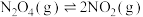
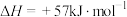 ,在温度为
,在温度为 、
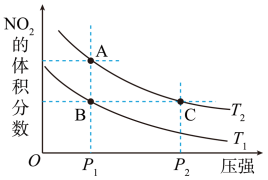
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化曲线如图所示。下列说法正确的是
的体积分数随压强变化曲线如图所示。下列说法正确的是
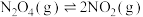
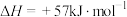 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化曲线如图所示。下列说法正确的是
的体积分数随压强变化曲线如图所示。下列说法正确的是
A.由图可知,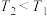 |
B.从A点变到 点,平衡逆移,气体的颜色: 点,平衡逆移,气体的颜色: 深, 深, 浅 浅 |
| C.该反应在低温下能自发进行 |
D. 、 、 两点气体的平均相对分子质量: 两点气体的平均相对分子质量: |
您最近一年使用:0次
解题方法
6 . 氢能源是最具应用前景的能源之一,甲烷-水蒸气催化重整制氢(SMR)是一种制高纯氢的方法,其涉及的主要反应如下:
反应Ⅰ:
反应Ⅱ: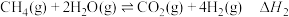
反应Ⅲ:
回答下列问题:
(1)
___________  ,反应Ⅱ能在
,反应Ⅱ能在___________ (填“高温”或“低温”)的条件下自发进行。
(2)某温度下,按照投料比 加入密闭容器中发生反应Ⅰ,平衡时
加入密闭容器中发生反应Ⅰ,平衡时 的体积分数为
的体积分数为 ,则
,则 的转化率为
的转化率为___________ (填分数);实际生产中反应物投料比小于反应的化学计量数之比,目的是___________ 。
(3)在常压、600℃条件下,向体系中加入适量生石灰后可提高 的产率。应用化学平衡移动原理解释原因
的产率。应用化学平衡移动原理解释原因___________ 。
(4)在T℃、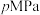 条件下,向恒温恒容密闭容器中充入
条件下,向恒温恒容密闭容器中充入 水蒸气和
水蒸气和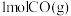 ,发生反应Ⅲ,达平衡时,
,发生反应Ⅲ,达平衡时, 的转化率为
的转化率为 。平衡时,
。平衡时, 的平衡分压为
的平衡分压为___________  ,此温度下,该反应的平衡常数
,此温度下,该反应的平衡常数
___________ (用平衡分压代替平衡浓度计算,分压=总压 物质的量分数)。
物质的量分数)。
(5)调整CO和 初始投料比发生反应Ⅲ,测得CO的平衡转化率如图:
初始投料比发生反应Ⅲ,测得CO的平衡转化率如图:

A、B、C、D、E中温度最高的点是___________ 。
反应Ⅰ:

反应Ⅱ:
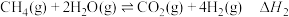
反应Ⅲ:

回答下列问题:
(1)

 ,反应Ⅱ能在
,反应Ⅱ能在(2)某温度下,按照投料比
 加入密闭容器中发生反应Ⅰ,平衡时
加入密闭容器中发生反应Ⅰ,平衡时 的体积分数为
的体积分数为 ,则
,则 的转化率为
的转化率为(3)在常压、600℃条件下,向体系中加入适量生石灰后可提高
 的产率。应用化学平衡移动原理解释原因
的产率。应用化学平衡移动原理解释原因(4)在T℃、
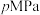 条件下,向恒温恒容密闭容器中充入
条件下,向恒温恒容密闭容器中充入 水蒸气和
水蒸气和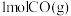 ,发生反应Ⅲ,达平衡时,
,发生反应Ⅲ,达平衡时, 的转化率为
的转化率为 。平衡时,
。平衡时, 的平衡分压为
的平衡分压为 ,此温度下,该反应的平衡常数
,此温度下,该反应的平衡常数
 物质的量分数)。
物质的量分数)。(5)调整CO和
 初始投料比发生反应Ⅲ,测得CO的平衡转化率如图:
初始投料比发生反应Ⅲ,测得CO的平衡转化率如图:
A、B、C、D、E中温度最高的点是
您最近一年使用:0次
名校
7 . 依据图示关系,下列说法正确的是
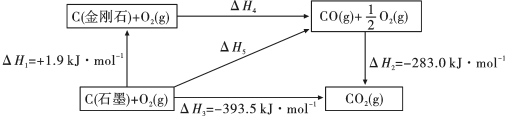

A.石墨的燃烧热 |
B.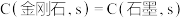  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C. 石墨或 石墨或 金刚石分别完全燃烧,金刚石放出热量多 金刚石分别完全燃烧,金刚石放出热量多 |
D.反应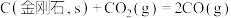 在任何温度下均能自发进行 在任何温度下均能自发进行 |
您最近一年使用:0次
名校
解题方法
8 . 中华传统文化蕴含着丰富的化学知识,下列说法错误的是
| A.“青蒿一握,以水二升渍,绞取汁”,这种提取青蒿素的方法属于物理变化 |
| B.“投泥泼水愈光明,烁玉流金见精悍”,所指高温时碳与水蒸气的反应为放热反应 |
| C.“爝火燃回春浩浩,烘炉照破夜沉沉”,这里的能量变化是化学能转化为热能和光能 |
| D.“千锤万凿出深山,烈火焚烧若等闲”,涉及的反应在高温下自发进行 |
您最近一年使用:0次
名校
解题方法
9 . 已知:在 、
、 下白锡转化为灰锡的反应焓变和嫡变分别为
下白锡转化为灰锡的反应焓变和嫡变分别为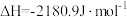 ,
,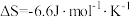 。现把白锡制成的器皿放在常温、
。现把白锡制成的器皿放在常温、 的室内,它会不会变成灰锡而不能再继续使用
的室内,它会不会变成灰锡而不能再继续使用
 、
、 下白锡转化为灰锡的反应焓变和嫡变分别为
下白锡转化为灰锡的反应焓变和嫡变分别为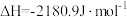 ,
,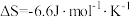 。现把白锡制成的器皿放在常温、
。现把白锡制成的器皿放在常温、 的室内,它会不会变成灰锡而不能再继续使用
的室内,它会不会变成灰锡而不能再继续使用| A.会变成灰锡 |
| B.只有继续升高温度才会变成灰锡 |
| C.只有继续降低温度才会变成灰锡 |
| D.无法确定 |
您最近一年使用:0次
名校
10 . 合成氨反应为 ΔH=-92.4kJ/mol。下列有关该反应的说法正确的是
ΔH=-92.4kJ/mol。下列有关该反应的说法正确的是
 ΔH=-92.4kJ/mol。下列有关该反应的说法正确的是
ΔH=-92.4kJ/mol。下列有关该反应的说法正确的是| A.催化剂不改变反应焓变(ΔH),但能增大正、逆反应的活化能 |
| B.增大压强,反应速率增大,平衡常数也增大 |
| C.升高温度,反应的活化分子百分数增大,正、逆反应速率都增大 |
| D.该反应的ΔS>0、ΔH<0,在低温下自发进行 |
您最近一年使用:0次



