解题方法
1 . 氯及其化合物在工业生产中具有很重要的作用。
(1)舍勒制氯气的方法至今仍是实验室制氯气的常用方法,其离子方程式为:_______ 。制得的 中有大量的
中有大量的 气体,通入饱和食盐水可除去
气体,通入饱和食盐水可除去 ,且溶液中有白色固体产生,这个固体是
,且溶液中有白色固体产生,这个固体是_______ (填化学式)。
(2) 可用于生产一种化工产品
可用于生产一种化工产品 。已知有关反应如下:
。已知有关反应如下:
①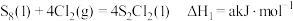
②
③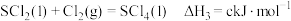
④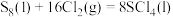
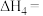
_______  (用含
(用含 和
和 的式子表示)。已知
的式子表示)。已知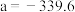 ,则反应①
,则反应①_______ (填字母)
A.一定自发 B.一定不自发 C.高温自发 D.低温自发
(3) 还可在工业上用于生产亚硝酰氯:
还可在工业上用于生产亚硝酰氯: 。
。 时,在
时,在 密闭容器中充入
密闭容器中充入
 与
与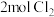 ,一段时间后反应达到平衡。
,一段时间后反应达到平衡。
①该反应达到化学平衡的标志有_______ (填字母)。
A.单位时间内消耗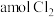 的同时,生成
的同时,生成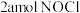
B.容器内总压强不再变化
C.混合气体的密度保持不变
D.混合气体的平均相对分子质量保持不变
E.NO与NOCl的体积分数相等
②已知上述反应中正、逆反应速率的表达式为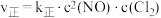 、
、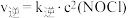 ,
, 、
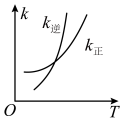
、 变化如图所示,则该反应
变化如图所示,则该反应
_______ 0(填“>”、“<”)。 时,
时, 平衡转化率为
平衡转化率为 ,则
,则 与
与 的比值为
的比值为_______ 。
③若在温度为 ,容积为
,容积为 的容器中,充入
的容器中,充入 、
、 、
、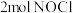 ,则
,则
_______  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
(4)氯气—铝电池是一种新型的燃料电池,若电解质溶液为 溶液,电极分别用铝条和碳棒,负极反应为
溶液,电极分别用铝条和碳棒,负极反应为_______ 。
(1)舍勒制氯气的方法至今仍是实验室制氯气的常用方法,其离子方程式为:
 中有大量的
中有大量的 气体,通入饱和食盐水可除去
气体,通入饱和食盐水可除去 ,且溶液中有白色固体产生,这个固体是
,且溶液中有白色固体产生,这个固体是(2)
 可用于生产一种化工产品
可用于生产一种化工产品 。已知有关反应如下:
。已知有关反应如下:①
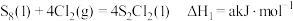
②

③
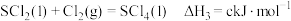
④
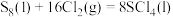
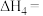
 (用含
(用含 和
和 的式子表示)。已知
的式子表示)。已知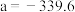 ,则反应①
,则反应①A.一定自发 B.一定不自发 C.高温自发 D.低温自发
(3)
 还可在工业上用于生产亚硝酰氯:
还可在工业上用于生产亚硝酰氯: 。
。 时,在
时,在 密闭容器中充入
密闭容器中充入
 与
与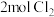 ,一段时间后反应达到平衡。
,一段时间后反应达到平衡。①该反应达到化学平衡的标志有
A.单位时间内消耗
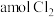 的同时,生成
的同时,生成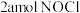
B.容器内总压强不再变化
C.混合气体的密度保持不变
D.混合气体的平均相对分子质量保持不变
E.NO与NOCl的体积分数相等
②已知上述反应中正、逆反应速率的表达式为
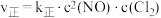 、
、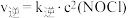 ,
, 、
、 变化如图所示,则该反应
变化如图所示,则该反应
 时,
时, 平衡转化率为
平衡转化率为 ,则
,则 与
与 的比值为
的比值为
③若在温度为
 ,容积为
,容积为 的容器中,充入
的容器中,充入 、
、 、
、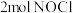 ,则
,则
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。(4)氯气—铝电池是一种新型的燃料电池,若电解质溶液为
 溶液,电极分别用铝条和碳棒,负极反应为
溶液,电极分别用铝条和碳棒,负极反应为
您最近一年使用:0次
2 . 1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才,现将1molN2和3molH2投入1L的密闭容器,在一定条件下,利用反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:
(1)合成氨反应平衡常数的表达式为_______ 。温度升高,K值_______ (填“增大”“减小”或“不变"):使用催化剂,K值_______ (填“增大“减小”或“不变”)。
(2)反应的 S
S_______ 0(填“>”“<"或“=”)
(3)有利于提高平衡混合物中氨含量的条件有_______ (填序号)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡_______ 移动(填“正向”“逆向”或“不”);给体系升温,
_______ (填“增大”“减小”或不变”),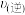
_______ (填“增大”“减小”或“不变”),平衡_______ 移动(填“正向”“逆向”或“不”)。
 2NH3(g)
2NH3(g)  H<0. 回答下列问题:
H<0. 回答下列问题:(1)合成氨反应平衡常数的表达式为
(2)反应的
 S
S(3)有利于提高平衡混合物中氨含量的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡

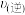
您最近一年使用:0次
解题方法
3 . 下列对熵的理解错误的是
| A.等质量的同种物质气态时熵值最大,固态时熵值最小 |
| B.体系越有序,熵值越小;越混乱,熵值越大 |
| C.从焓判据来看,△H<0有利于反应的自发进行 |
| D.25℃、 1.01×105Pa时,2N2O5(g)=4NO2(g)+O2(g)是熵减反应 |
您最近一年使用:0次
名校
4 . 向 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,发生反应:
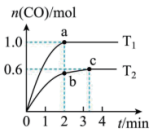
,发生反应: 。在不同温度下测得
。在不同温度下测得 随时间变化的曲线如图所示。下列说法正确的是
随时间变化的曲线如图所示。下列说法正确的是
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 各
各 ,发生反应:
,发生反应: 。在不同温度下测得
。在不同温度下测得 随时间变化的曲线如图所示。下列说法正确的是
随时间变化的曲线如图所示。下列说法正确的是
| A.该反应在任意温度下均可自发进行 |
B. 温度下, 温度下, 的平衡转化率是30% 的平衡转化率是30% |
C. 、 、 两点平衡常数: 两点平衡常数: |
D. 温度下,0到 温度下,0到 内,用 内,用 表示的平均反应速率为0.1mol·L-1·min-1 表示的平均反应速率为0.1mol·L-1·min-1 |
您最近一年使用:0次
名校
解题方法
5 . 在一定条件下,某可逆反应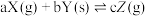 达到平衡后,X的转化率
达到平衡后,X的转化率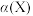 与温度
与温度 、压强
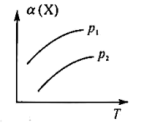
、压强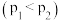 的关系如图所示。根据图像,下列判断正确的是
的关系如图所示。根据图像,下列判断正确的是
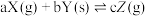 达到平衡后,X的转化率
达到平衡后,X的转化率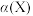 与温度
与温度 、压强
、压强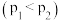 的关系如图所示。根据图像,下列判断正确的是
的关系如图所示。根据图像,下列判断正确的是
| A.a+b<c |
B.该反应的 |
| C.该反应在高温下具有自发性 |
| D.向平衡体系中加入适量Y,平衡向右移动 |
您最近一年使用:0次
6 . 合成氨工业中原料气进入合成塔前需经过铜氨溶液“净化”,除去其中的CO,原理为
 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是| A.该反应在任何温度下均能自发进行 | B.降低温度有利于吸收CO |
| C.增大压强有利于铜氨溶液再生 | D.为节约成本,原料气可以不进行净化 |
您最近一年使用:0次
2024-01-24更新
|
66次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高二上学期1月考试化学试卷
名校
7 . 下列说法正确的是
A.反应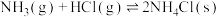 在低温下能自发进行,则该反应的 在低温下能自发进行,则该反应的 |
B.对于反应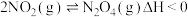 ,恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 ,恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 |
C.反应 ,在恒温恒压下,加入催化剂,平衡常数增大 ,在恒温恒压下,加入催化剂,平衡常数增大 |
| D.升高温度或加入催化剂能使单位体积内活化分子的百分数增大,但原因不同 |
您最近一年使用:0次
8 . 2023年8月24日,日本向海洋中排放了大量的核废水,这一举动引起了国际社会的广泛关注和讨论,其中最为担忧的是核废水会对海洋中的物种造成变异和影响。下列有关说法正确的是
| A.核电站发电的核反应属于放热反应 |
| B.核电站发电是将化学能转化为电能和热能 |
| C.核废水扩散到海水中的过程属于熵增过程 |
D.核废水中含 , , 基态原子的轨道表示式为 基态原子的轨道表示式为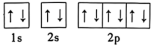 |
您最近一年使用:0次
2023-12-24更新
|
304次组卷
|
4卷引用:广西钦州市第四中学2023-2024学年高二上学期12月考试化学试卷
名校
9 . 一碳化学是以分子中只含一个碳原子的化合物为原料生产化工产品的方法。合成气( 和
和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
I:
II:
III:
(1)当反应I达到平衡后,下列措施可提高正反应速率的是_______(填标号)。
(2)若在恒温恒容容器中仅发生反应II,则下列能说明反应达到平衡状态的是_______。
(3)向容积为 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应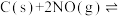
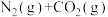 ,
, 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。
① 内,以
内,以 表示的该反应速率
表示的该反应速率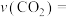
___________ ,最终达平衡时 的转化率
的转化率
___________ ,该温度 ℃下的平衡常数
℃下的平衡常数
___________ 。
②保持温度 ℃不变,向该
℃不变,向该 密闭容器中加入该四种反应混合物各
密闭容器中加入该四种反应混合物各 ,该时刻,正、逆反应速率的大小关系为:
,该时刻,正、逆反应速率的大小关系为: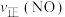
___________ 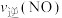 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)已知4CO(g) +2NO2(g) 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
 和
和 的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:
的混合气体)是一碳化学的重要原料,焦炭与水蒸气在恒容密闭容器中会发生如下三个反应:I:

II:

III:

(1)当反应I达到平衡后,下列措施可提高正反应速率的是_______(填标号)。
| A.加入焦炭 | B.通入CO | C.升高温度 | D.分离出氢气 |
| A.容器内气体的压强不变 |
| B.容器内气体的总质量不变 |
| C.容器内气体的平均相对分子质量不变 |
D.单位时间内,每有2 mol  键断裂,同时有1 mol 键断裂,同时有1 mol  键断裂 键断裂 |
 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应
,发生反应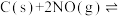
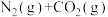 ,
, 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。| 条件 | 保持温度为 /℃ /℃ | ||||||
| 时间 | 0 | 5min | 10min | 15min | 20min | 25min | 30min |
 物质的量 物质的量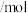 | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
 物质的量 物质的量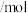 | 0 | 0.3 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
 内,以
内,以 表示的该反应速率
表示的该反应速率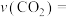
 的转化率
的转化率
 ℃下的平衡常数
℃下的平衡常数
②保持温度
 ℃不变,向该
℃不变,向该 密闭容器中加入该四种反应混合物各
密闭容器中加入该四种反应混合物各 ,该时刻,正、逆反应速率的大小关系为:
,该时刻,正、逆反应速率的大小关系为: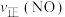
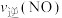 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)已知4CO(g) +2NO2(g)
 4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
4CO2(g)+N2 (g) ΔH1 = -1200kJ•mol-1 ,该反应在
您最近一年使用:0次
2023-12-14更新
|
171次组卷
|
3卷引用:广西百色市德保高中2023-2024学年高二上学期11月期中考试化学试题
10 . 金属钛具有良好的耐高低温、抗酸碱、高强度和低密度等优良特性,广泛应用于航空航天、医疗器械等领域。 的一种制备方法为
的一种制备方法为
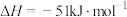 。下列说法中正确的是
。下列说法中正确的是
 的一种制备方法为
的一种制备方法为
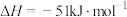 。下列说法中正确的是
。下列说法中正确的是| A.该反应只有在高温下才能自发进行 |
| B.恒温恒容条件下,混合气体的密度保持不变能说明该反应达到平衡状态 |
| C.该反应在工业生产中的适宜条件是低温、低压 |
D.恒温恒容条件下,向平衡体系中再加入少量 , ,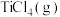 的体积分数将增大 的体积分数将增大 |
您最近一年使用:0次
2023-11-22更新
|
155次组卷
|
3卷引用:广西贵港市部分学校2023-2024学年高二上学期期中联考化学试题



