1 . 反应SiCl4(g)+2H2(g)=Si(s)+4HCl(g)∆H>0,可用于纯硅的制备,下列有关反应的说法不正确的是( )
| A.该反应能自发进行的原因熵增效应大于焓变效应 |
| B.高温下,每生成1molSi,需消耗标准状况下44.8LH2 |
| C.用E表示键能,该反应∆H=4E(Si-Cl)+2E(H-H)-E(Si-Si)-4E(H-Cl) |
| D.该反应是工业制硅的最后一步反应,获得高纯硅 |
您最近一年使用:0次
2020-11-23更新
|
114次组卷
|
2卷引用:广西钦州市第四中学2020-2021学年下学期高二3月月考化学(体艺班)试题
20-21高三上·江苏徐州·期中
2 . 甲烷转化为一氧化碳和氢气的反应:CH4(g)+H2O(g) CO(g)+3H2(g) ∆H>0。下列有关该反应的说法正确的是
CO(g)+3H2(g) ∆H>0。下列有关该反应的说法正确的是
 CO(g)+3H2(g) ∆H>0。下列有关该反应的说法正确的是
CO(g)+3H2(g) ∆H>0。下列有关该反应的说法正确的是| A.∆S>0 |
B.平衡常数K=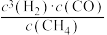 |
| C.升高温度过程中,v(正)<v(逆) |
| D.平衡状态时,CH4(g)与H2O(g)的物质的量浓度相等 |
您最近一年使用:0次
名校
解题方法
3 . 利用CH4可消除NO2的污染,反应原理为:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
 N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是| 组别 | 温度/K | 物质的量/mol 时间/min | 0 | 10 | 20 | 40 | 50 |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | M | 0.15 |
A.组别①中0∼20min内,NO2降解速率为0.25mol L−1 L−1 min−1 min−1 |
| B.由实验数据可知温度T1>T2 |
| C.40min时,表格中M对应的数据为0.15 |
| D.该反应在高温下不能自发进行 |
您最近一年使用:0次
2020-11-14更新
|
2233次组卷
|
9卷引用:广西钦州市第四中学2023-2024学年高二上学期10月考试化学试卷
广西钦州市第四中学2023-2024学年高二上学期10月考试化学试卷湖南省常德市外国语学校2020-2021学年高二上学期第二次月考化学试题广东省汕头市金山中学2020-2021学年高二上学期期末考试化学试题浙江省宁波市奉化区2020-2021学年高二下学期期末统考化学试题河南省焦作市第十一中学2023-2024学年高二上学期10月份月考 化学试卷浙江省杭州学军中学2021届高三上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高三上】【期中】【HD-LP423】【化学】(已下线)【浙江新东方】120(已下线)小题必刷27 化学反应速率、图像及其影响因素——2021年高考化学一轮复习小题必刷(通用版本)
解题方法
4 . 下列说法完全正确的是( )
| A.自发进行的反应均是放热反应 | B.ΔS为正值的反应均能自发进行 |
| C.物质的量增加的反应,ΔS为正值 | D.CaCO3(s)受热分解为CaO(s)和CO2(g):ΔS>0 |
您最近一年使用:0次
2020-11-10更新
|
84次组卷
|
4卷引用:广西贺州市平桂管理区公会中学2021-2022学年上学期高二第二次月考化学(理)试题
5 . 金属锡的冶炼常用焦炭作还原剂:SnO2(s)+2C(s)═Sn(s)+2CO(g)↑,反应过程中能量的变化如图所示.下列有关该反应的△H、△S的说法中正确的是
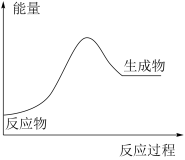

| A.△H<0,△S<0 | B.△H>0,△S<0 | C.△H<0,△S>0 | D.△H>0,△S>0 |
您最近一年使用:0次
2020-10-26更新
|
495次组卷
|
27卷引用:广西桂林市2019-2020学年高二下学期期末质量检测化学试题
广西桂林市2019-2020学年高二下学期期末质量检测化学试题广西南宁市第十中学2020-2021学年高二上学期期中考试化学(理)试题(已下线)2013-2014学年甘肃省兰州一中高二上学期期末考试化学试卷2015-2016学年甘肃省兰州一中高二上学期期末化学试卷2016-2017学年福建省宁德市部分中学高二上期中化学试卷(已下线)2.4 化学反应进行的方向人教版高二化学选修4 第二章 第四节 化学反应进行的方向练习题【全国百强校】福建省莆田市第一中学2018-2019学年高二上学期期中考试化学试题江苏省江阴市第一中学2018-2019学年高二下学期期中考试化学试题河北省唐山一中2019-2020学年高二上学期10月月考化学试题福建省泉州市永春华侨中学2019-2020学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市第八中学2019-2020学年高二上学期期中考试化学试题(已下线)2.3 化学反应的方向(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)(已下线)第二章 化学反应速率和化学平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)2.4+化学反应进行的方向-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)2.4化学反应进行的方向(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第二章检测-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河北省祖冲之中学2020-2021学年高二上学期阶段性测试化学试题甘肃省临夏县中学2020-2021学年高二上学期期末考试化学试题安徽省宿州市砀山中学2021-2022学年高二上学期第一次质量检测化学试题(已下线)2.3 化学反应的方向(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)宁夏石嘴山市平罗中学2021-2022学年高二下学期期中考试化学试题黑龙江省牡丹江市第一中学2022-2023学年高二10月月考化学试题新疆乌鲁木齐市第八十中学2022-2023学年高二上学期期中考试化学试题湖南省张家界市民族中学2023-2024学年高二上学期第一次月考化学试题高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第四节 化学反应进行的方向 化学反应进行的方向(已下线)第5讲 化学反应的调控
名校
6 . 下列说法正确的是( )
| A.非自发反应在任何条件下都不能实现 |
| B.熵增的放热反应一定是自发反应 |
| C.NH4NO3溶于水时吸热,故该过程不是自发的 |
| D.碳与二氧化碳反应生成一氧化碳的反应是熵减反应 |
您最近一年使用:0次
2020-10-05更新
|
703次组卷
|
4卷引用:广西钦州市第四中学2023-2024学年高二上学期10月考试化学试卷
解题方法
7 . 碳、氮化合物在生产、生活中具有重要作用。回答下列问题:
(1)已知在298K和101KPa条件下,有如下反应:
反应Ⅰ:C(s)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
反应Ⅱ:2C(s)+O2(g)=2CO(g)△H2=-221kJ•mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)△H3=+180.5kJ•mol-1
①汽车尾气净化原理为反应Ⅳ:2NO(g)+2CO(g)⇌N2(g)+2CO2(g),其反应热ΔH=______ ,该反应能自发进行的条件是______ (填“低温”或“高温”)。
②在恒容密闭容器中发生Ⅳ的反应,下列有关该反应的说法中正确的是____ (填字母)。
A.升高温度,平衡常数减小
B.体系达到平衡后,加入催化剂,平衡正向移动
C.增大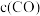 ,平衡逆向移动,NO的转化率降低
,平衡逆向移动,NO的转化率降低
D.其他条件不变,向平衡体系充入CO2气体,K值减小
E.该反应过程中,气体的密度始终保持不变
(2)氮的一种氢化物是HN3,其水溶液酸性与醋酸相似,常温下,将a mol·L-1的HN3与b mol·L-1的Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N ),则该混合物溶液呈
),则该混合物溶液呈_____ (填“酸”“碱”或“中”)性,混合液中c(HN3)=_____ mol·L-1。
(3)利用电解法可以消除废水溶液中CN-,其原理为:碱性条件下,阳极Cl-先转化为ClO-,再将CN-氧化为两种无污染的气体。
①阳极电极反应式为_____ 。
②阳极附近溶液中除去CN-的离子方程式为______ 。
(1)已知在298K和101KPa条件下,有如下反应:
反应Ⅰ:C(s)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
反应Ⅱ:2C(s)+O2(g)=2CO(g)△H2=-221kJ•mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)△H3=+180.5kJ•mol-1
①汽车尾气净化原理为反应Ⅳ:2NO(g)+2CO(g)⇌N2(g)+2CO2(g),其反应热ΔH=
②在恒容密闭容器中发生Ⅳ的反应,下列有关该反应的说法中正确的是
A.升高温度,平衡常数减小
B.体系达到平衡后,加入催化剂,平衡正向移动
C.增大
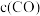 ,平衡逆向移动,NO的转化率降低
,平衡逆向移动,NO的转化率降低D.其他条件不变,向平衡体系充入CO2气体,K值减小
E.该反应过程中,气体的密度始终保持不变
(2)氮的一种氢化物是HN3,其水溶液酸性与醋酸相似,常温下,将a mol·L-1的HN3与b mol·L-1的Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N
 ),则该混合物溶液呈
),则该混合物溶液呈(3)利用电解法可以消除废水溶液中CN-,其原理为:碱性条件下,阳极Cl-先转化为ClO-,再将CN-氧化为两种无污染的气体。
①阳极电极反应式为
②阳极附近溶液中除去CN-的离子方程式为
您最近一年使用:0次
8 . 已知:4CO(g)+2NO2(g)⇌4CO2(g)+N2(g) ΔH=-1200 kJ·mol−1。在2 L恒容密闭容器中,按照下表中甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%。下列说法中正确的是
| 甲 | 乙 |
| 0.2 mol NO2 | 0.1 mol NO2 |
| 0.4 mol CO | 0.2 mol CO |
| A.放热反应,一定能自发进行 |
| B.该温度下,反应的平衡常数为5 |
| C.达平衡时,NO2的浓度:甲>乙 |
| D.达平衡时,N2的体积分数:甲<乙 |
您最近一年使用:0次
2020-06-06更新
|
389次组卷
|
4卷引用:广西桂林市第十八中学2019-2020学年高二下学期期中考试化学试题
名校
解题方法
9 . 下列说法错误的是( )
| A.碳酸钙的分解能否自发进行与温度有关 |
| B.硝酸铵溶于水可自发进行是因为ΔS>0 |
| C.已知S(g)+O2(g)=SO2(g) ΔH1 ,S(s)+O2(g)=SO2(g) ΔH2,则ΔH1<ΔH2 |
| D.若正反应的活化能为EakJ/mol,逆反应的活化能为EbkJ/mol,则△H=(Eb-Ea)kJ/mol |
您最近一年使用:0次
2020-01-17更新
|
143次组卷
|
3卷引用:广西南宁市第三中学2019-2020学年高二上学期期末考试化学试题
名校
10 . 下列说法中错误的是
| A.凡是放热反应而且熵增加的反应,就更易自发进行 |
| B.对于同一物质在不同状态时的熵值是:气态>液态>固态 |
| C.对同一反应来说,平衡常数K值越大,则正反应进行越完全 |
| D.凡是能量较高的分子发生的碰撞均为有效碰撞 |
您最近一年使用:0次
2020-01-14更新
|
220次组卷
|
5卷引用:广西北海市北海中学2019-2020学年高二上学期期末考试化学试题
广西北海市北海中学2019-2020学年高二上学期期末考试化学试题(已下线)2.3 化学反应的方向(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)天津市宝坻九中2020-2021学年高二上学期第一次月考化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题福建省福州市三校2022-2023学年高二上学期期中联考化学试题



