名校
解题方法
1 . 最近科学家提出CO2利用新途径:首先用氨水吸收大量CO2,然后把CO2从溶液中再生出来,在一定条件下,再与H2反应合成甲烷。合成甲烷的反应原理为: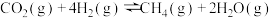
 。
。
(1)已知:
ⅰ.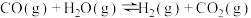
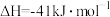
ⅱ.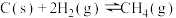
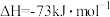
ⅲ.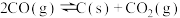
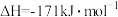
①x=_______ 。
②有利于反应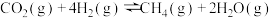 自发进行的条件是
自发进行的条件是_______ (填“高温”或“低温”)
(2)工业上可利用甲烷脱硝(除去NOx),已知脱硝时生成N2、CO2等无害物质,写出甲烷与NO反应的化学方程式:_______ 。
(3)将CO2和H2混合气体 置于一密闭容器中合成甲烷,测得水蒸气的物质的量分数随温度变化如下图所示:
置于一密闭容器中合成甲烷,测得水蒸气的物质的量分数随温度变化如下图所示:

①该反应的平衡常数:K(300℃)_______ K(500℃)(选填“>”或“<”)。
②a→b段的物质的量分数不是对应温度下水蒸气的平衡物质的量分数,说明理由_______ 。
③若c点平衡体系的总压强为p,则该温度下反应的Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,只列出算式即可)。
(4)常温下,用氨水吸收CO2最终生成NH4HCO3,写出 NH4HCO3溶液水解的离子方程式:_______ ,该水解离子方程式的平衡常数为_______ [已知: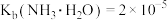 ,
,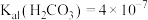 ]。
]。
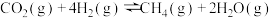
 。
。(1)已知:
ⅰ.
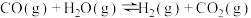
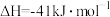
ⅱ.
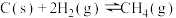
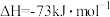
ⅲ.
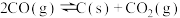
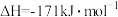
①x=
②有利于反应
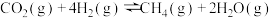 自发进行的条件是
自发进行的条件是(2)工业上可利用甲烷脱硝(除去NOx),已知脱硝时生成N2、CO2等无害物质,写出甲烷与NO反应的化学方程式:
(3)将CO2和H2混合气体
 置于一密闭容器中合成甲烷,测得水蒸气的物质的量分数随温度变化如下图所示:
置于一密闭容器中合成甲烷,测得水蒸气的物质的量分数随温度变化如下图所示:
①该反应的平衡常数:K(300℃)
②a→b段的物质的量分数不是对应温度下水蒸气的平衡物质的量分数,说明理由
③若c点平衡体系的总压强为p,则该温度下反应的Kp=
(4)常温下,用氨水吸收CO2最终生成NH4HCO3,写出 NH4HCO3溶液水解的离子方程式:
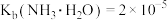 ,
,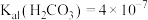 ]。
]。
您最近一年使用:0次
名校
2 . 对于反应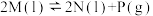
 ,下列说法正确的是
,下列说法正确的是
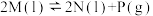
 ,下列说法正确的是
,下列说法正确的是| A.该反应在高温条件下才能自发进行 |
| B.升高温度,在平衡移动过程中,v逆大于v正 |
C.增大M的浓度,反应速率加快,平移常数 也增大 也增大 |
| D.增大压强,平衡向正反应方向移动 |
您最近一年使用:0次
2021-03-20更新
|
145次组卷
|
2卷引用:广西钦州市2020-2021学年高二下学期期末考试化学试题
解题方法
3 . 类推是学习化学的一种重要方法,下列类推一定正确的是
| A.Al在纯氧中燃烧生成Al2O3,所以Fe在纯氧中燃烧生成Fe2O3 |
| B.Na和H2O反应是熵增放热的自发反应,所以K和H2O反应也是熵增放热的自发反应 |
| C.CaCO3分解为吸热反应,所以分解反应都为吸热反应 |
| D.MgCl2在熔融状态下能导电,所以AlCl3在熔融状态下也能导电 |
您最近一年使用:0次
2021-02-19更新
|
91次组卷
|
2卷引用:广西贵港市2020-2021学年高二上学期期末教学质量监测化学试题
4 . I.在一恒容的密闭容器中充入0.1 mol L-1CO2、0.1 mol L-1 CH4,在一定条件下发生反应:CH4(g)+CO2(g)⇌2CO(g)+2H2(g),测得CH4平衡转化率与温度、压强关系如图
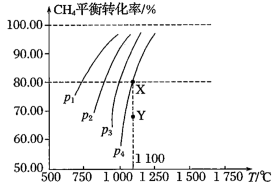
(1)该反应的△S___________ 0,△H__________ 0(填“>”或“<”)
(2) 、
、 、
、 、
、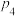 压强由大到小的顺序是:
压强由大到小的顺序是:_________________________ ,压强为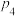 时,在y点:v正
时,在y点:v正_______ v逆(填“>”或“<”或“=”)
(3)1100℃时该反应的平衡常数为________________ (保留小数点后两位)
Ⅱ.常温下,0.1000 mol L-1 NaOH溶液滴定20.00 mL 0.100 0 mol﹒L-1CH3COOH溶液所得滴定曲线如下图。
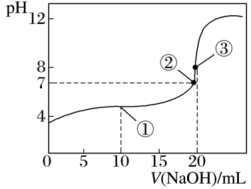
(4)下列说法正确的是_____________ (填字母)
A.点①所示溶液中:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B.点②所示溶液中:c(CH3COO-)=c(Na+)=c(OH-)=c(H+)
C.点③所示溶液中离子浓度的大小关系为:
c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.水的电离程度:③>②>①
(5)若pH=2的CH3COOH与pH=12的NaOH等体积混合,离子浓度由大到小的顺序为____________________________________ 。
(6)用铜作电极电解NaOH溶液的总反应的化学方程式为:____________________ 。

(1)该反应的△S
(2)
 、
、 、
、 、
、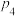 压强由大到小的顺序是:
压强由大到小的顺序是: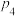 时,在y点:v正
时,在y点:v正(3)1100℃时该反应的平衡常数为
Ⅱ.常温下,0.1000 mol L-1 NaOH溶液滴定20.00 mL 0.100 0 mol﹒L-1CH3COOH溶液所得滴定曲线如下图。

(4)下列说法正确的是
A.点①所示溶液中:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
B.点②所示溶液中:c(CH3COO-)=c(Na+)=c(OH-)=c(H+)
C.点③所示溶液中离子浓度的大小关系为:
c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.水的电离程度:③>②>①
(5)若pH=2的CH3COOH与pH=12的NaOH等体积混合,离子浓度由大到小的顺序为
(6)用铜作电极电解NaOH溶液的总反应的化学方程式为:
您最近一年使用:0次
名校
5 . 下列反应中,一定不能自发进行的是
A.CO(g)=C(s)+ O2(g)ΔH=+110.5kJ·mol-1 O2(g)ΔH=+110.5kJ·mol-1 |
| B.2KClO3(s)=2KCl(s)+3O2(g)ΔH=-78.03kJ·mol-1 |
| C.4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)ΔH=-444.3kJ·mol-1 |
| D.NH4HCO3(s)+CH3COOH(aq)=CO2(g)+CH3COONH4(aq)+H2O(l)ΔH=+37.30kJ·mol-1 |
您最近一年使用:0次
2021-01-25更新
|
157次组卷
|
2卷引用:广西南宁市宾阳县宾阳中学2021-2022学年高二上学期期中考试化学(理科)试题
18-19高二下·广西桂林·期中
名校
解题方法
6 . 已知:△G=△H﹣T△S,△G为自由能变化,△H为焓变,T为热力学温度,△S熵变。当△G<0时反应能自发进行,△G>0时反应不能自发进行。据此下列叙述中正确的是
| A.熵变大于零的反应肯定能自发进行 |
| B.焓变小于零的反应肯定能自发进行 |
| C.焓变大于零的反应肯定不能自发进行 |
| D.焓变小于零且熵变大于零的反应一定能自发进行 |
您最近一年使用:0次
2021-01-12更新
|
117次组卷
|
3卷引用:【全国百强校】广西桂林市第十八中学2018-2019学年高二下学期期中段考化学试题
(已下线)【全国百强校】广西桂林市第十八中学2018-2019学年高二下学期期中段考化学试题陕西省宝鸡市渭滨中学2020-2021学年度高二上学期期中考试化学试题云南省保山第九中学2021届高三上学期开学考试化学试题
名校
7 . 下列说法错误的是
| A.ΔH<0、ΔS>0的反应在温度低时不能自发进行 |
| B.ΔH>0、ΔS<0的反应控制温度不能自发进行 |
| C.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0 |
| D.NH4HCO3(g)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57kJ·mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
您最近一年使用:0次
2021-01-03更新
|
262次组卷
|
3卷引用:广西南宁市上林县中学2020-2021学年高二上学期期末考试化学试题
8 . (1)0.5 mol气态高能燃料乙硼烷 在氧气中燃烧生成固态三氧化二硼和液态水放出1082.5 kJ的热量,其热化学方程式为
在氧气中燃烧生成固态三氧化二硼和液态水放出1082.5 kJ的热量,其热化学方程式为_________ 。已知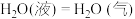
 ,则STP条件下,11.2 L乙硼烷完全燃烧生成气态水时放出的热量
,则STP条件下,11.2 L乙硼烷完全燃烧生成气态水时放出的热量____________
(2)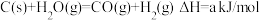 ,
,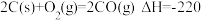
 ,又已知
,又已知 、
、 和
和 键的键能分别为
键的键能分别为 、
、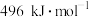 和
和 ,则a为
,则a为__________ 。
(3)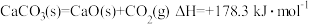 ,
, ,该反应能够自发进行,则温度所满足的条件是
,该反应能够自发进行,则温度所满足的条件是______________ 。
(4)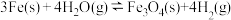 平衡常数的表达式为
平衡常数的表达式为____________ 。反应 的平衡常数为49,则该温度下反应
的平衡常数为49,则该温度下反应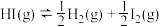 的平衡常数为
的平衡常数为____________ 。
 在氧气中燃烧生成固态三氧化二硼和液态水放出1082.5 kJ的热量,其热化学方程式为
在氧气中燃烧生成固态三氧化二硼和液态水放出1082.5 kJ的热量,其热化学方程式为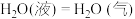
 ,则STP条件下,11.2 L乙硼烷完全燃烧生成气态水时放出的热量
,则STP条件下,11.2 L乙硼烷完全燃烧生成气态水时放出的热量(2)
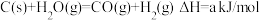 ,
,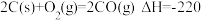
 ,又已知
,又已知 、
、 和
和 键的键能分别为
键的键能分别为 、
、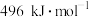 和
和 ,则a为
,则a为(3)
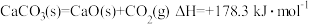 ,
, ,该反应能够自发进行,则温度所满足的条件是
,该反应能够自发进行,则温度所满足的条件是(4)
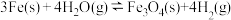 平衡常数的表达式为
平衡常数的表达式为 的平衡常数为49,则该温度下反应
的平衡常数为49,则该温度下反应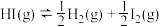 的平衡常数为
的平衡常数为
您最近一年使用:0次
2020-12-07更新
|
221次组卷
|
2卷引用:广西钦州市第四中学2020-2021学年下学期高二3月月考化学(体艺班)试题
9 . 下列说法正确的是
| A.食物在常温下腐败是自发进行 | B.凡是放热反应都是自发的 |
| C.自发反应都是熵增大的反应 | D.原电池的反应是属于不是自发反应 |
您最近一年使用:0次
2020-11-25更新
|
184次组卷
|
3卷引用:广西壮族自治区贺州市平桂高级中学(贺州市第五高级中学)2020-2021学年高二上学期第一次月考化学试题
广西壮族自治区贺州市平桂高级中学(贺州市第五高级中学)2020-2021学年高二上学期第一次月考化学试题福建省泉州市第六中学2022-2023学年高二上学期期中考化学试题(已下线)专题06 化学反应的方向及调控【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
名校
解题方法
10 . 反应CH3OH(g)+NH3(g)=CH3NH2(g)+H2O(g)在高温下才能自发向右进行,则该反应的ΔH、ΔS应为( )
| A.ΔH>0、ΔS<0 | B.ΔH<0、ΔS>0 |
| C.ΔH>0、ΔS>0 | D.ΔH<0、ΔS<0 |
您最近一年使用:0次
2020-11-24更新
|
126次组卷
|
24卷引用:2015-2016学年广西宾阳县宾阳中学高二5月月考化学试卷
2015-2016学年广西宾阳县宾阳中学高二5月月考化学试卷2015-2016学年福建省三明一中高二下第一次月考化学试卷2016-2017学年江西省赣州市十四校高二上学期期中化学试卷2016-2017学年江西省宜春市奉新一中高二上月考二化学卷(已下线)2.4 化学反应进行的方向湖北省沙市中学2017-2018学年高二上学期期中考试化学试题安徽省江淮名校2017-2018学年高二期中考试化学试题云南省中央民族大学附属中学芒市国际学校2017-2018学年高二上学期末考试化学试题内蒙古杭锦后旗奋斗中学2017-2018学年高二下学期第一次月考化学试题【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高二上学期期中联考化学试题人教版高二化学选修4 第二章 第四节 化学反应进行的方向练习题【校级联考】湖南省醴陵一中、攸县一中2018-2019学年高二(理)上学期期中联考化学试题【市级联考】吉林省吉林市普通高中2018-2019学年高二上学期期中考试化学试题贵州省思南中学2019-2020学年高二上学期期中考试化学试题福建省平和一中、南靖一中等五校2019-2020学年高二年上学期期中联考化学试题福建省漳州市第八中学2019-2020学年高二上学期期中考试化学试题甘肃省张掖市高台县第一中学2018-2019学年高二上学期期末考试理科化学试题安徽省合肥市2019—2020学年高二下学期期中考试化学试题吉林省榆树市第一高级中学2020-2021学年高二上学期期中考试化学试题贵州省北师大遵义附属高级中学2020-2021学年高二上学期期中考试化学试题甘肃省庆阳市第六中学2021-2022学年高二上学期期中考试化学(理)试题新疆哈密市第八中学2021-2022学年高二上学期期中考试化学试题江西省宜春市上高二中2023-2024学年高二上学期第三次月考化学试题 高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第四节 化学反应进行的方向 化学反应进行的方向



