1 . 下列有关反应 的说法正确的是
的说法正确的是
 的说法正确的是
的说法正确的是| A.该反应在任何温度下都能自发进行 |
| B.气体平均摩尔质量不变时,反应达平衡状态 |
| C.其他条件一定,平衡时升高温度,v(正)减小,v(逆)增大 |
D.消耗2.24 L  ,反应转移0.2 mol电子 ,反应转移0.2 mol电子 |
您最近一年使用:0次
名校
2 . 我国科研人员设计将脱除SO2的反应与制备H2O2相结合的协同转化装置如图。在电场作用下,双极膜中间层的H2O解离为OH-和H+,并向两极迁移。已知:
①单独制备H2O2:2H2O+O2=2H2O2,不能自发进行;
②单独脱除SO2:4OH-+2SO2+O2=2SO +2H2O,能自发进行。
+2H2O,能自发进行。
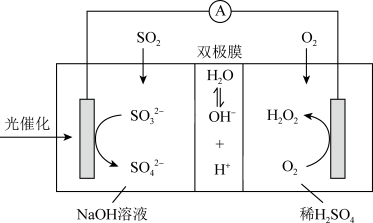
下列说法不正确的是
①单独制备H2O2:2H2O+O2=2H2O2,不能自发进行;
②单独脱除SO2:4OH-+2SO2+O2=2SO
 +2H2O,能自发进行。
+2H2O,能自发进行。
下列说法不正确的是
| A.单独脱除SO2的反应为吸热反应 |
| B.反应过程中不需补加稀H2SO4 |
| C.正极的电极反应式:O2+2e-+2H+=H2O2 |
| D.协同转化总反应:SO2+O2+2H2O=H2O2+H2SO4 |
您最近一年使用:0次
名校
3 . 下列有关化学反应的方向的说法正确的是
| A.能自发进行的反应一定能迅速发生 |
| B.2KClO3(s)=2KCl(s)+3O2(g) ΔH<0,该反应能否自发进行与温度无关 |
C.常温下,2H2O 2H2↑+O2↑,即常温下水的分解反应是自发反应 2H2↑+O2↑,即常温下水的分解反应是自发反应 |
| D.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向 |
您最近一年使用:0次
名校
4 . 恒容密闭容器中进行的反应
 ,下列说法不正确的是
,下列说法不正确的是

 ,下列说法不正确的是
,下列说法不正确的是| A.当混合气体的密度不再变化时,反应达到平衡状态 |
| B.提高反应物浓度,活化分子数增大,活化分子百分数增大,因此反应速率增大 |
| C.该反应在高温下能自发进行 |
| D.单位时间内生成1molCO2的同时生成2molCO,说明反应达到平衡状态 |
您最近一年使用:0次
解题方法
5 . 工业合成氨是人类科学技术的一项重大突破。其合成原理为:
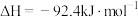
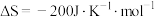
(1)下列关于工业合成氨的说法正确的是___________。
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是___________
(3)工业上合成氨的部分工艺流程如图:
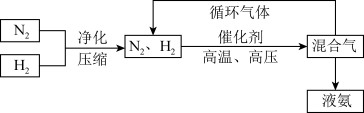
请用平衡移动原理来解释在流程中及时分离出氨气和循环使用气体的原因__________________ 。
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度)。则:
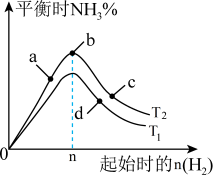
图象中T2和T1的关系是:T1___________ T2(填“>、<或=”,下同);a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是___________ (填字母)。
(5)恒温下,往一个4L的密闭容器中充入2 mol N2和5.2 mol H2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
此条件下该反应的化学平衡常数K =___________ ; 若维持容器体积不变,温度不变,往原平衡体系中加入N2、H2和NH3各4 mol,化学平衡将向___________ 反应方向移动(填“正”或“逆”)。

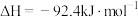
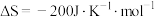
(1)下列关于工业合成氨的说法正确的是___________。
| A.因为ΔH<0,所以该反应一定能自发进行 |
| B.工业合成氨的反应是熵减小的放热反应,在常温时可自发进行 |
| C.合成氨反应选择在400~500℃进行的重要原因是此温度下氨的产率最高 |
| D.生产中在考虑动力和设备材料承受能力的前提下,压强越大转化率越大 |
| A.容器内N2、H2、NH3的浓度之比为1∶3∶2 | B.2v正(H2)=3v逆(NH3) |
| C.容器内压强保持不变 | D.混合气体的密度保持不变 |

请用平衡移动原理来解释在流程中及时分离出氨气和循环使用气体的原因
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度)。则:

图象中T2和T1的关系是:T1
(5)恒温下,往一个4L的密闭容器中充入2 mol N2和5.2 mol H2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/ mol∙L−1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
您最近一年使用:0次
名校
6 . 下列有关化学反应的方向及判据的说法不正确的是
A.反应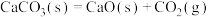 能否自发进行,主要由 能否自发进行,主要由 决定 决定 |
| B.焓变或熵变均可以单独作为反应自发性的判据 |
C. 、 、 的反应在任何温度下部能自发进行 的反应在任何温度下部能自发进行 |
| D.冰在室温下自动融化成水,是因为体系混乱度降低 |
您最近一年使用:0次
名校
7 . 对于可逆反应2NO2(g) N2O4(g),下列说法错误的是
N2O4(g),下列说法错误的是
 N2O4(g),下列说法错误的是
N2O4(g),下列说法错误的是| A.当2v(N2O4)正=v(NO2)逆时,该反应达到平衡状态 |
| B.该反应在一定条件下能自发进行,则ΔH<0 |
| C.恒温恒容条件下,达平衡状态后,再充入一定量的NO2,NO2转化率将减小 |
| D.恒温恒容条件下,若混合气体的颜色保持不变,则该反应达到平衡状态 |
您最近一年使用:0次
8 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。
I. 与
与 重整是
重整是 利用的研究热点之一、该重整反应体系主要涉及以下反应:
利用的研究热点之一、该重整反应体系主要涉及以下反应:
a)
b)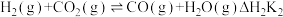
c)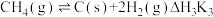
d)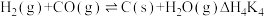
(1)根据盖斯定律,反应a的
_______ (写出一个代数式即可,下同)。
_______
(2)反应b高温自发进行,则该反应的
_______ (填“>0”或“<0”)
(3)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
(4)设 为压强平衡常数(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),反应a、c、d的
为压强平衡常数(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),反应a、c、d的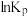 随
随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。

①反应a、c、d中,属于吸热反应的有_______ (填字母)。
②在如图中A点对应温度下、原料组成为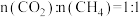 、初始总压为
、初始总压为 的恒容密闭容器中进行反应,体系达到平衡时
的恒容密闭容器中进行反应,体系达到平衡时 的分压为
的分压为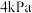 ,则
,则 的平衡转化率为
的平衡转化率为_______ 。
③反应b在如图中B点对应温度下的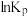 为1,请在如图中画出反应b的
为1,请在如图中画出反应b的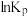 随
随 的变化趋势图
的变化趋势图_______ 。
II. 捕获和转化可减少
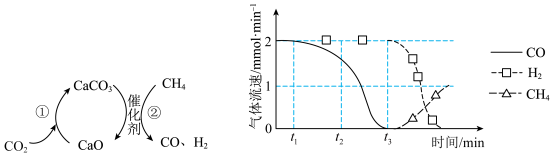
捕获和转化可减少 排放并实现资源利用,原理如左图所示,反应①完成之后,以
排放并实现资源利用,原理如左图所示,反应①完成之后,以 为载气,以恒定组成的
为载气,以恒定组成的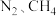 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如右图所示,反应过程中始终末检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如右图所示,反应过程中始终末检测到 ,在催化剂上有积碳。
,在催化剂上有积碳。
(5)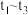 ,
, 比
比 多,且生成
多,且生成 速率不变,可能的原因是
速率不变,可能的原因是_______ 。
(6) 之后,生成
之后,生成 的速率为0,
的速率为0, 的速率逐渐增大,最终恢复到1,可能的原因是
的速率逐渐增大,最终恢复到1,可能的原因是_______ 。
I.
 与
与 重整是
重整是 利用的研究热点之一、该重整反应体系主要涉及以下反应:
利用的研究热点之一、该重整反应体系主要涉及以下反应:a)

b)
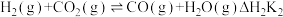
c)
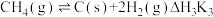
d)
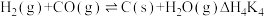
(1)根据盖斯定律,反应a的


(2)反应b高温自发进行,则该反应的

(3)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
A.移去部分 ,反应c、d的平衡均向右移动 ,反应c、d的平衡均向右移动 |
B.在体积不变的情况下,等比例地减少 和 和 的浓度,能增大 的浓度,能增大 的转化率 的转化率 |
C.降低反应温度,反应 的正反应速率减小,逆反应速率增大 的正反应速率减小,逆反应速率增大 |
D.增大体系压强,有利于吸收 |
 为压强平衡常数(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),反应a、c、d的
为压强平衡常数(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),反应a、c、d的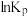 随
随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。
①反应a、c、d中,属于吸热反应的有
②在如图中A点对应温度下、原料组成为
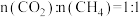 、初始总压为
、初始总压为 的恒容密闭容器中进行反应,体系达到平衡时
的恒容密闭容器中进行反应,体系达到平衡时 的分压为
的分压为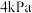 ,则
,则 的平衡转化率为
的平衡转化率为③反应b在如图中B点对应温度下的
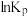 为1,请在如图中画出反应b的
为1,请在如图中画出反应b的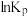 随
随 的变化趋势图
的变化趋势图II.
 捕获和转化可减少
捕获和转化可减少 排放并实现资源利用,原理如左图所示,反应①完成之后,以
排放并实现资源利用,原理如左图所示,反应①完成之后,以 为载气,以恒定组成的
为载气,以恒定组成的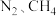 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如右图所示,反应过程中始终末检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如右图所示,反应过程中始终末检测到 ,在催化剂上有积碳。
,在催化剂上有积碳。
(5)
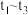 ,
, 比
比 多,且生成
多,且生成 速率不变,可能的原因是
速率不变,可能的原因是(6)
 之后,生成
之后,生成 的速率为0,
的速率为0, 的速率逐渐增大,最终恢复到1,可能的原因是
的速率逐渐增大,最终恢复到1,可能的原因是
您最近一年使用:0次
名校
解题方法
9 . 下列说法不正确的是
A.汽车尾气净化反应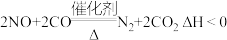 ,常温下不能自发进行 ,常温下不能自发进行 |
| B.“冰,水为之而寒于水”说明相同质量的水和冰,水的焓更高 |
| C.酸碱中和的反应热与焓变几乎无差异,而黑火药爆炸的反应热与焓变差异较大 |
| D.利用溶液的颜色变化与浓度的定量关系可以测量化学反应速率 |
您最近一年使用:0次
2023-09-17更新
|
123次组卷
|
2卷引用:浙江省海宁市高级中学2022-2023学年高二上学期10月月考化学试题
名校
10 . 随着人们的物质生活水平的不断提高和工业化快速发展,环境污染也日益加重,空气中有毒气体主要包括 SO2、CO、NOx、烃类等等。
(1)在一定条件下,CH4可与 NOx反应除去 NOx,已知有下列热化学方程式:
CH4(g)+2O2(g)=CO2(g)+2H2O(1) ΔH =-890.3kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH =+67.0kJ/mol
H2O(1)=H2O(g) ΔH =+41.0kJ/mol
CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g) ΔH =__________ kJ/mol
(2)在 2 L 的密闭容器中按物质的量之比 1∶2 充入 CO 和 H2,发生反应CO(g)+2H2(g) CH3OH(g) ΔH。测得 CO 的平衡转化率随温度及不同压强的变化如图所示,P2和 195 ℃时 n(H2)随时间的变化结果如表所示。
CH3OH(g) ΔH。测得 CO 的平衡转化率随温度及不同压强的变化如图所示,P2和 195 ℃时 n(H2)随时间的变化结果如表所示。
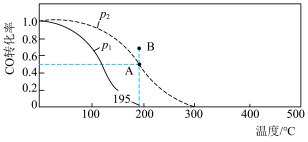
P2及195℃时n(H2)随时间变化
①该反应的ΔH___________ 0(填“>”、“<”或“=”),原因是___________ 。
②在 P2及 195 ℃时,在 0~2 min,平均反应速率 v(CH3OH)=___________ 。
③能说明该反应已达到平衡状态的是___________ 。
a.容器内混合气体压强保持不再变化 b.CO 和 H2的转化率之比不再变化
c.容器内混合气体的平均摩尔质量不再变化 d.容器内混合气体的密度不再变化
④P2及 195℃下,在 B 点时,v(正)___________ v(逆)(填“>”、“<”或“=”)。
⑤下列说法不正确的是___________ 。
a.将容器体积变为 1L,再次达平衡时,CO 的物质的量浓度为原平衡的 2 倍
b.该反应在任何条件下都能自发进行
c.充分反应后,容器内只存在 CH3OH 分子
d.升高温度,n(CH3OH)/n(CO)减小
⑥在 P2及 195 ℃时,该反应的平衡常数 Kp=___________ (用平衡分压代替平衡浓度计算, 分压=总压×物质的量分数,结果用含 P2的分式表示)。
(1)在一定条件下,CH4可与 NOx反应除去 NOx,已知有下列热化学方程式:
CH4(g)+2O2(g)=CO2(g)+2H2O(1) ΔH =-890.3kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH =+67.0kJ/mol
H2O(1)=H2O(g) ΔH =+41.0kJ/mol
CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g) ΔH =
(2)在 2 L 的密闭容器中按物质的量之比 1∶2 充入 CO 和 H2,发生反应CO(g)+2H2(g)
 CH3OH(g) ΔH。测得 CO 的平衡转化率随温度及不同压强的变化如图所示,P2和 195 ℃时 n(H2)随时间的变化结果如表所示。
CH3OH(g) ΔH。测得 CO 的平衡转化率随温度及不同压强的变化如图所示,P2和 195 ℃时 n(H2)随时间的变化结果如表所示。
P2及195℃时n(H2)随时间变化
| t/min | 0 | 1 | 2 | 3 | 4 |
| n(H2) | 8 | 6 | 5 | 4 | 4 |
②在 P2及 195 ℃时,在 0~2 min,平均反应速率 v(CH3OH)=
③能说明该反应已达到平衡状态的是
a.容器内混合气体压强保持不再变化 b.CO 和 H2的转化率之比不再变化
c.容器内混合气体的平均摩尔质量不再变化 d.容器内混合气体的密度不再变化
④P2及 195℃下,在 B 点时,v(正)
⑤下列说法不正确的是
a.将容器体积变为 1L,再次达平衡时,CO 的物质的量浓度为原平衡的 2 倍
b.该反应在任何条件下都能自发进行
c.充分反应后,容器内只存在 CH3OH 分子
d.升高温度,n(CH3OH)/n(CO)减小
⑥在 P2及 195 ℃时,该反应的平衡常数 Kp=
您最近一年使用:0次



