名校
解题方法
1 . 科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示:(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)

(1)由图可知,决定反应速率的一步是_______ 。(填a、b、c……)
(2)下列关于工业合成氨的说法正确的是_______。
(3)请用平衡移动原理来解释在合成氨中及时分离出氨的原因_______ 。
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示 物质的量,
物质的量, %表示
%表示 的百分含量)。
的百分含量)。
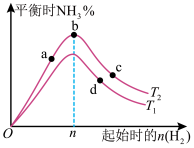
①图像中 和
和 的关系是:
的关系是:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②a、b、c、d四点所处的平衡状态中,反应物 的转化率最高的是
的转化率最高的是_______ (填字母)。
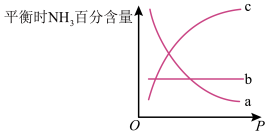
(5)其他条件不变,表示平衡时氨的百分含量随压强变化关系的曲线为_______ (填字母编号)。
(6)某温度下,向一个 的密闭容器中充入
的密闭容器中充入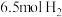 和
和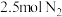 ,反应过程中对
,反应过程中对 的浓度进行检测,得到的数据如下表所示:
的浓度进行检测,得到的数据如下表所示:
此条件下该反应的化学平衡常数
_______ 。
(7)氨氧化法是工业生产中制取硝酸的主要途径。
已知:


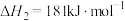

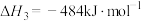
写出氨气催化氧化生成 和水蒸气的热化学方程式
和水蒸气的热化学方程式_______ 。

(1)由图可知,决定反应速率的一步是
(2)下列关于工业合成氨的说法正确的是_______。
A.因为 ,所以该反应一定能自发进行 ,所以该反应一定能自发进行 |
B.因为 ,所以该反应一定不能自发进行 ,所以该反应一定不能自发进行 |
| C.在高温下进行是为了提高反应物的平衡转化率 |
| D.使用催化剂不仅可以加快反应速率还可以降低反应所需的温度 |
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示
 物质的量,
物质的量, %表示
%表示 的百分含量)。
的百分含量)。
①图像中
 和
和 的关系是:
的关系是:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②a、b、c、d四点所处的平衡状态中,反应物
 的转化率最高的是
的转化率最高的是(5)其他条件不变,表示平衡时氨的百分含量随压强变化关系的曲线为

(6)某温度下,向一个
 的密闭容器中充入
的密闭容器中充入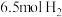 和
和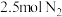 ,反应过程中对
,反应过程中对 的浓度进行检测,得到的数据如下表所示:
的浓度进行检测,得到的数据如下表所示:时间 | 5 | 10 | 15 | 20 | 25 | 30 |
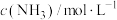 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |

(7)氨氧化法是工业生产中制取硝酸的主要途径。
已知:



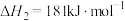

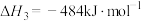
写出氨气催化氧化生成
 和水蒸气的热化学方程式
和水蒸气的热化学方程式
您最近一年使用:0次
名校
2 . 含氮物质可发生如下反应:①
②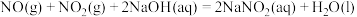
③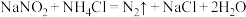
下列说法正确的是

②
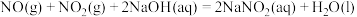
③
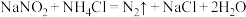
下列说法正确的是
A.常温下,NO与 混合能立即看到红棕色气体,说明该反应已达平衡 混合能立即看到红棕色气体,说明该反应已达平衡 |
B.反应②的 |
C.反应③消耗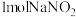 ,理论上会生成标准状况下约 ,理论上会生成标准状况下约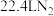 |
D.利用反应①、②、③可以同时处理 含量较高的废气和含 含量较高的废气和含 的废水 的废水 |
您最近一年使用:0次
2023-06-02更新
|
1330次组卷
|
8卷引用:江苏省清江中学、南通部分学校2023-2024学年高二下学期第一次调研(3月)化学试卷
江苏省清江中学、南通部分学校2023-2024学年高二下学期第一次调研(3月)化学试卷江苏省扬州市2023届高三下学期三模化学试题考点巩固卷08 化学反应速率与化学平衡(3大考点45题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)第13讲氮及其化合物江苏省南通市如皋市2024届高三上学期期初考试押题卷化学试题(已下线)第28讲化化学平衡的移动及反应进行的方向(已下线)考点16 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题1-5
3 . 绿色能源是未来能源发展的方向,积极发展氢能,是实现“碳达峰、碳中和”的重要举措。回答下列问题:
(1)通过生物柴油副产物甘油制取 正成为绿色能源的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应如下:
正成为绿色能源的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应如下:
Ⅰ.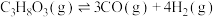
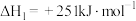
Ⅱ.
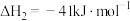
①反应I能够自发进行的条件是_______ (填“高温”、“低温”或“任何温度”)。
②重整总反应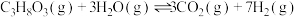 的
的
_______  。
。
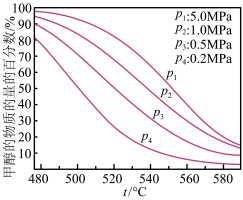
③利用合成气制备甲醇的方程式为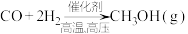 ,平衡混合物中甲醇含量与温度、压强关系如图所示,有利于化学平衡向生成甲醇的方向移动的条件是
,平衡混合物中甲醇含量与温度、压强关系如图所示,有利于化学平衡向生成甲醇的方向移动的条件是_______ 温度、_______ 压强(填“增大”或“降低”);恒容条件下,按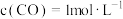 、
、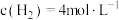 进行实验,CO的转化率为50%,则该条件下平衡常数K=
进行实验,CO的转化率为50%,则该条件下平衡常数K=_______ (只写数值,写分数)。
(2)一定温度下,向2L的恒容密闭容器中充入4.0mol 和4.0molCO,在催化剂作用下发生反应:
和4.0molCO,在催化剂作用下发生反应: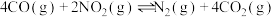
 ,测得相关数据如下:
,测得相关数据如下:
20min时,保持温度不变,继续向容器中通入1.0mol 和1.0molCO,在
和1.0molCO,在 时刻反应再次达到平衡,则
时刻反应再次达到平衡,则 的转化率相比原平衡会
的转化率相比原平衡会_______ (填“增大”“减小”或“不变”,下同),化学平衡常数K将_______ 。
(3)近年来,有研究人员用 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示。
的回收利用,其工作原理如图所示。

①请写出Cu电极上产生HCOOH的电极反应式:_________
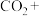 ______
______ _______
_______
②如果Cu电极上只生成0.15mol 和0.30mol
和0.30mol ,则Pt电极上产生
,则Pt电极上产生 的物质的量为
的物质的量为_______ mol。
(1)通过生物柴油副产物甘油制取
 正成为绿色能源的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应如下:
正成为绿色能源的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应如下:Ⅰ.
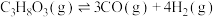
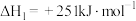
Ⅱ.

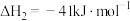
①反应I能够自发进行的条件是
②重整总反应
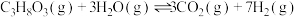 的
的
 。
。③利用合成气制备甲醇的方程式为
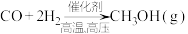 ,平衡混合物中甲醇含量与温度、压强关系如图所示,有利于化学平衡向生成甲醇的方向移动的条件是
,平衡混合物中甲醇含量与温度、压强关系如图所示,有利于化学平衡向生成甲醇的方向移动的条件是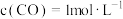 、
、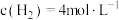 进行实验,CO的转化率为50%,则该条件下平衡常数K=
进行实验,CO的转化率为50%,则该条件下平衡常数K=
(2)一定温度下,向2L的恒容密闭容器中充入4.0mol
 和4.0molCO,在催化剂作用下发生反应:
和4.0molCO,在催化剂作用下发生反应: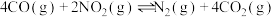
 ,测得相关数据如下:
,测得相关数据如下:| t/min | 0 | 5 | 10 | 15 | 20 |
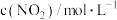 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
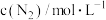 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
 和1.0molCO,在
和1.0molCO,在 时刻反应再次达到平衡,则
时刻反应再次达到平衡,则 的转化率相比原平衡会
的转化率相比原平衡会(3)近年来,有研究人员用
 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示。
的回收利用,其工作原理如图所示。
①请写出Cu电极上产生HCOOH的电极反应式:
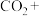 ______
______ _______
_______
②如果Cu电极上只生成0.15mol
 和0.30mol
和0.30mol ,则Pt电极上产生
,则Pt电极上产生 的物质的量为
的物质的量为
您最近一年使用:0次
名校
4 . 研发CO2利用技术、降低空气中CO2含量是实现碳中和的研究热点。为减少CO2对环境造成的影响,可采用“CO2催化加氢制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:
Ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
回答下列问题:
(1)反应Ⅰ、Ⅱ的lnK(K代表化学平衡常数)随 (温度的倒数)的变化如图1所示。反应Ⅰ自发进行的条件是
(温度的倒数)的变化如图1所示。反应Ⅰ自发进行的条件是_______ ,升高温度, 反应CO(g)+2H2(g)  CH3OH(g)的化学平衡常数
CH3OH(g)的化学平衡常数_______ (填“增大”或“减小”或“不变”)。

(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
(3)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图2。
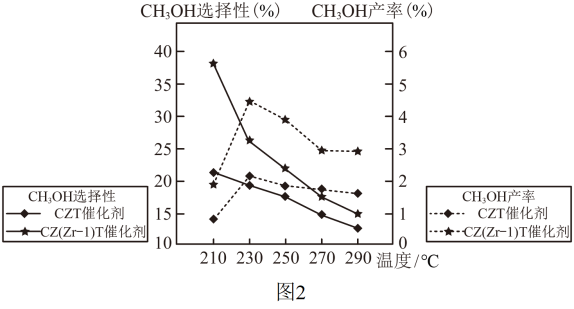
其中: CH3OH的选择性=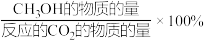
①在上述条件下合成甲醇的工业条件是_______ 。
A.210℃ B.230℃ C 催化CZT D.催化剂CZ(Zr-1)T
②在230℃以上,升高温度CO2的转化率增大,但甲醇的产率降低,原因是_______ 。
(4)恒温恒压密闭容器中,加入2molCO2和4molH2,只发生反应Ⅰ和反应Ⅱ,初始压强为p0,在300℃发生反应,反应达平衡时,CO2的转化率为50%,容器体积减小20%。则反应Ⅱ的平衡常数K=_______ (保留两位有效数字)。
Ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2回答下列问题:
(1)反应Ⅰ、Ⅱ的lnK(K代表化学平衡常数)随
 (温度的倒数)的变化如图1所示。反应Ⅰ自发进行的条件是
(温度的倒数)的变化如图1所示。反应Ⅰ自发进行的条件是 CH3OH(g)的化学平衡常数
CH3OH(g)的化学平衡常数
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
| A.增大CO的浓度,反应Ⅰ的平衡向正反应方向移动 |
| B.降低温度,反应Ⅰ和Ⅱ的正、逆反应速率都减小 |
| C.恒温恒容下充入氦气,反应Ⅰ的平衡向正反应方向移动 |
| D.增大压强,反应Ⅰ和Ⅱ重新达到平衡的时间不同 |

其中: CH3OH的选择性=
①在上述条件下合成甲醇的工业条件是
A.210℃ B.230℃ C 催化CZT D.催化剂CZ(Zr-1)T
②在230℃以上,升高温度CO2的转化率增大,但甲醇的产率降低,原因是
(4)恒温恒压密闭容器中,加入2molCO2和4molH2,只发生反应Ⅰ和反应Ⅱ,初始压强为p0,在300℃发生反应,反应达平衡时,CO2的转化率为50%,容器体积减小20%。则反应Ⅱ的平衡常数K=
您最近一年使用:0次
名校
5 . 我国明确提出2030年“碳达峰”与2060年“碳中和”目标,“碳中和”对我国意味着:一是能源转型首当其冲;二是通过工艺改造、节能等措施减少二氧化碳的排放在能源的产生、转换、消费过程。减少二氧化碳排放的方法之一是将CO2催化还原,比如:
反应1: CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
反应2: CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
都是目前处理CO2的重要方法。回答下列问题:
(1)反应1在_______ 的条件下能自发发生。(填低温、高温、任意温度)
(2)已知:①CO和H2的标准燃烧热分别为-283.0 kJ·mol-1和-285.8 kJ·mol-1
②H2O(1)=H2O(g) ΔH3=44.0 kJ·mol-1,
则 ΔH2=_______ kJ·mol-1。
(3)恒温恒容的密闭容器中,投入物质的量之比为1:3的CO2和H2发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1达到平衡,下列有关叙述正确的是_______。
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1达到平衡,下列有关叙述正确的是_______。
(4)一定条件下,在1L密闭容器中加入2molCO2和2molH2只发生反应2: CO2(g)+H2(g)  CO(g)+H2O(g),如图是随着反应的进行,CO2的浓度随时间改变的变化图。若在t1时刻再加入lmolCO2, t2时刻到达新的平衡。
CO(g)+H2O(g),如图是随着反应的进行,CO2的浓度随时间改变的变化图。若在t1时刻再加入lmolCO2, t2时刻到达新的平衡。
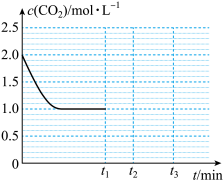
请你画出t1~t3内时刻CO2的物质的量浓度随时间改变的变化图:______
反应1: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1反应2: CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2都是目前处理CO2的重要方法。回答下列问题:
(1)反应1在
(2)已知:①CO和H2的标准燃烧热分别为-283.0 kJ·mol-1和-285.8 kJ·mol-1
②H2O(1)=H2O(g) ΔH3=44.0 kJ·mol-1,
则 ΔH2=
(3)恒温恒容的密闭容器中,投入物质的量之比为1:3的CO2和H2发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1达到平衡,下列有关叙述正确的是_______。
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1达到平衡,下列有关叙述正确的是_______。| A.升高温度,逆反应速率增加,平衡常数减小 |
| B.再加入一定量的CO2和H2, CO2和H2的转化率不可能同时都增大 |
| C.加入合适的催化剂可以提高CO2的平衡转化率 |
| D.其他条件不变,改为恒温恒压,可以提高平衡时CH3OH的百分含量 |
 CO(g)+H2O(g),如图是随着反应的进行,CO2的浓度随时间改变的变化图。若在t1时刻再加入lmolCO2, t2时刻到达新的平衡。
CO(g)+H2O(g),如图是随着反应的进行,CO2的浓度随时间改变的变化图。若在t1时刻再加入lmolCO2, t2时刻到达新的平衡。
请你画出t1~t3内时刻CO2的物质的量浓度随时间改变的变化图:
您最近一年使用:0次
解题方法
6 . 1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才,现将1mol N2和3mol H2投入1L的密闭容器,在一定条件下,利用反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g) ΔH<0。
2NH3(g) ΔH<0。
回答下列问题:
(1)合成氨反应平衡常数的表达式为_______ 。温度升高,K值_______ (填“增大”“减小”或“不变”)。
(2)反应的ΔS_______ 0(填“>”“<”或“=”)
(3)有利于提高平衡混合物中氨含量的条件有_______ (填序号)。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡_______ 移动(填“正向”“逆向”或“不”);给体系升温,v正_______ (填“增大”“减小”或“不变”),v逆_______ (填“增大”“减小”或“不变”),平衡_______ 移动(填“正向”“逆向”或“不”)。
 2NH3(g) ΔH<0。
2NH3(g) ΔH<0。回答下列问题:
(1)合成氨反应平衡常数的表达式为
(2)反应的ΔS
(3)有利于提高平衡混合物中氨含量的条件有
A.低温 B.高温 C.低压 D.高压 E.催化剂
(4)当反应达到平衡后,向体系中充入N2的,平衡
您最近一年使用:0次
名校
解题方法
7 . 以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:C(s)+H2O(g)⇌CO(g)+H2(g) ΔH=+131.3kJ•mol-1。
①该反应在常温下__ 自发进行(填“能”与“不能”);
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是__ (填字母,下同)。
a.容器中的压强不变
b.1molH—H键断裂的同时断裂2molH—O键
c.c(CO)=c(H2)
d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)⇌CO2(g)+H2(g),得到如下三组数据:
①实验1中以v(CO2)表示的反应速率为__ 。(取小数二位,下同)
②该反应为__ (填“吸”或“放”)热反应,实验2条件下平衡常数K=__ 。
③若实验3达平衡时与实验2平衡状态中各物质的质量分数分别相等,且t<3min,则a、b应满足的关系是__ (用含a、b的数学式表示)。
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,下列措施中能使c(CH3OH)增大的是__ 。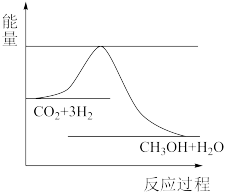
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1molCO2和3molH2
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:C(s)+H2O(g)⇌CO(g)+H2(g) ΔH=+131.3kJ•mol-1。
①该反应在常温下
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是
a.容器中的压强不变
b.1molH—H键断裂的同时断裂2molH—O键
c.c(CO)=c(H2)
d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)⇌CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 6 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
①实验1中以v(CO2)表示的反应速率为
②该反应为
③若实验3达平衡时与实验2平衡状态中各物质的质量分数分别相等,且t<3min,则a、b应满足的关系是
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化。在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,下列措施中能使c(CH3OH)增大的是

a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1molCO2和3molH2
您最近一年使用:0次
8 . I.由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
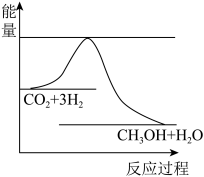
(1)关于该反应的下列说法中,正确的是_______。(填字母)
(2)该反应平衡常数K的表达式为K=_______ 。
(3)温度降低,平衡常数K_______ (填“增大”、“不变”或“减小”)。
(4)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2)为_______ mol·L-1·min-1。
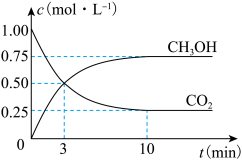
(5)下列措施中能使(4)中n(CH3OH)/n(CO2)增大的有_______ 。(填字母)
A.升高温度
B.加入催化剂
C.将H2O(g)从体系中分离
D.再充入1molCO2和3molH2
E.充入He(g),使体系总压强增大
II.在一恒容的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
回答下列问题:
(6)该反应为_______ 反应(选填“吸热”、“放热”)。
(7)能判断该反应达到化学平衡状态的依据是_______ (多选扣分)。
a.容器中压强不变 b.c(CO2)=c(CO)
c.V正(H2)=V逆(H2O) d.混合气体中 c(CO)不变
(8)830K时,各物质浓度符合下式:c(CO2)·c(H2)=2c(CO)·c(H2O),此时该反应_______ (填“正反应方向进行”、“逆反应方向进行”或“处于平衡状态”)。
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
(1)关于该反应的下列说法中,正确的是_______。(填字母)
| A.△H>0,△S>0 | B.△H>0,△S<0 | C.△H<0,△S<0 | D.△H<0,△S>0 |
(3)温度降低,平衡常数K
(4)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2)为

(5)下列措施中能使(4)中n(CH3OH)/n(CO2)增大的有
A.升高温度
B.加入催化剂
C.将H2O(g)从体系中分离
D.再充入1molCO2和3molH2
E.充入He(g),使体系总压强增大
II.在一恒容的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(6)该反应为
(7)能判断该反应达到化学平衡状态的依据是
a.容器中压强不变 b.c(CO2)=c(CO)
c.V正(H2)=V逆(H2O) d.混合气体中 c(CO)不变
(8)830K时,各物质浓度符合下式:c(CO2)·c(H2)=2c(CO)·c(H2O),此时该反应
您最近一年使用:0次
9 . 1909年德国化学家哈伯在实验室首次合成氨,合成氨技术的创立开辟了人工固氮的重要途径,其研究正是基于科学化学反应原理的指导。
(1)已知298K时,N2(g) +3H2(g) 2NH3(g),ΔH=–92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据反应进行的方向综合判据,常温下合成氨反应
2NH3(g),ΔH=–92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据反应进行的方向综合判据,常温下合成氨反应_______ (填“能”或“不能”)自发进行。
(2)反应N2(g) + 3H2(g) 2NH3(g)的化学平衡常数表达式为
2NH3(g)的化学平衡常数表达式为_______ 。
(3)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是_______ 。
(4)合成氨反应在一密闭容器中发生,如图是某一时间段反应速率与反应进程的关系曲线图。

①t4时刻,体系中是什么条件发生了变化?_______ 。
②下列时间段中,氨的百分含量最高的是_______ 。
A.0~t1 B.t2~t3 C.t3~t4 D.t4~t5
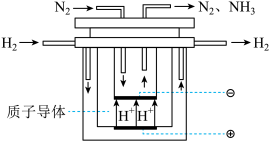
(5)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问题。因此,科学家在持续探索,寻求合成氨的新路径。下图为电解法合成氨的原理示意图,阴极的电极反应式为_______ 。
(1)已知298K时,N2(g) +3H2(g)
 2NH3(g),ΔH=–92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据反应进行的方向综合判据,常温下合成氨反应
2NH3(g),ΔH=–92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据反应进行的方向综合判据,常温下合成氨反应(2)反应N2(g) + 3H2(g)
 2NH3(g)的化学平衡常数表达式为
2NH3(g)的化学平衡常数表达式为(3)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是
| 序号 | 化学反应 | K(298K)的数值 |
| ① | N2(g) + O2(g)  2NO(g) 2NO(g) | 5×10-31 |
| ② | N2(g) + 3H2(g)  2NH3(g) 2NH3(g) | 4.1×106 |
(4)合成氨反应在一密闭容器中发生,如图是某一时间段反应速率与反应进程的关系曲线图。

①t4时刻,体系中是什么条件发生了变化?
②下列时间段中,氨的百分含量最高的是
A.0~t1 B.t2~t3 C.t3~t4 D.t4~t5
(5)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问题。因此,科学家在持续探索,寻求合成氨的新路径。下图为电解法合成氨的原理示意图,阴极的电极反应式为

您最近一年使用:0次
名校
解题方法
10 . 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g) +H2O(g)。下图表示该反应进行过程中能量的变化。关于该反应的下列说法中正确的是


| A.ΔH>0, ΔS>0 | B.ΔH>0,ΔS<0 |
| C.ΔH<0, ΔS<0 | D.ΔH<0,ΔS>0 |
您最近一年使用:0次
2022-08-18更新
|
356次组卷
|
22卷引用:安徽省六安市城南中学2020-2021学年高二上学期期中考试化学试题
安徽省六安市城南中学2020-2021学年高二上学期期中考试化学试题河南省长垣市第十中学2020-2021学年高二上学期第二次月考化学试题湖北省咸宁市通城二中2020-2021学年高二上学期10月月考化学试题内蒙古集宁新世纪中学2020-2021学年高二上学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高二上学期开学考试化学试题河北省石家庄市第一中学2021-2022学年高二上学期开学考试化学试题(已下线)第二单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)山东省烟台市招远市第二中学2021-2022学年高二10月月考化学试题安徽省蚌埠第三中学2021-2022学年高二上学期10月教学质量检测化学试题辽宁省朝阳育英高考补习学校2021-2022学年高二10月月考化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期第一次月考化学试题河南省范县第一中学2021-2022学年高二上学期第二次月考检测化学试题贵州省凯里市第一中学2021-2022学年高二上学期期中考试化学(理科)试题(已下线)必考点04 化学反应的方向和调控-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)(已下线)章末培优2 专题2 化学反应速率与化学平衡-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)贵州省毕节市金沙县第一中学2021-2022学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高二上学期期中考试化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高二上学期第一次月考化学试题福建泉州现代中学2021-2022学年高二上学期期中考试化学试题吉林省吉化第一高级中学校2021-2022学年高一下学期复课检测化学试题湖北省恩施州高中教育联盟2020-2021学年高一下学期期末考试化学试题(已下线)第20讲 化学平衡常数及转化率的计算(练)-2023年高考化学一轮复习讲练测(新教材新高考)



