名校
解题方法
1 . 在葡萄糖水溶液中,链状结构与环状结构的平衡关系及百分含量如下:不正确 的是
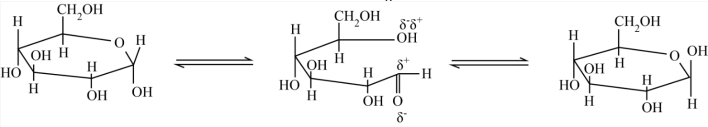

| A.链状葡萄糖成环是-OH与-CHO发生加成反应的结果 |
B.链状葡萄糖成环反应的 , , |
| C.链状葡萄糖成环后,分子中多了一个手性碳原子 |
D.水溶液中,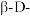 吡喃葡萄糖比 吡喃葡萄糖比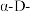 吡喃葡萄糖稳定 吡喃葡萄糖稳定 |
您最近一年使用:0次
2024-05-10更新
|
317次组卷
|
4卷引用:福建省厦门双十中学2023-2024学年高二下学期第二次月考化学试题
福建省厦门双十中学2023-2024学年高二下学期第二次月考化学试题2024届浙江省金华市义乌市高三下学期三模化学试题(已下线)江苏省苏州市2023-2024学年高三下学期第三次模拟考试化学试题(已下线)第04讲 化学反应的方向、化学反应的调控(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
2 . 生物质合成气可用于合成燃料甲醇。已知:
 。
。
已知该反应的 ,该反应的焓变和熵变随温度变化很小,可视为常数,则此反应自发进行的温度范围是
,该反应的焓变和熵变随温度变化很小,可视为常数,则此反应自发进行的温度范围是___________ (保留两位小数)。

 。
。已知该反应的
 ,该反应的焓变和熵变随温度变化很小,可视为常数,则此反应自发进行的温度范围是
,该反应的焓变和熵变随温度变化很小,可视为常数,则此反应自发进行的温度范围是
您最近一年使用:0次
2024-05-10更新
|
64次组卷
|
2卷引用:上海市向明中学2023-2024学年高二下学期期中考试化学(等级)试卷
3 . 可用焓变和熵变来判断化学反应进行的方向,下列都是能自发进行的化学反应,其中是吸热反应且反应后熵增的是
A.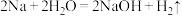 | B.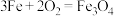 |
C. | D. |
您最近一年使用:0次
4 . 下列说法正确的是
A.用铁片和稀硫酸反应制取 时,改用铁片和浓硫酸可以加快产生 时,改用铁片和浓硫酸可以加快产生 的速率 的速率 |
B.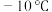 的液态水就会自动结冰成为固态,因为这是熵增的过程 的液态水就会自动结冰成为固态,因为这是熵增的过程 |
C.已知酸性: ,则等浓度等体积的 ,则等浓度等体积的 和 和 溶液中离子总数,前者大于后者 溶液中离子总数,前者大于后者 |
D.向 氨水中加入少量水,溶液中 氨水中加入少量水,溶液中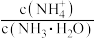 减小 减小 |
您最近一年使用:0次
名校
解题方法
5 . 苯与 在一定条件下能发生如下反应,其中部分转化历程与能量变化如图所示:
在一定条件下能发生如下反应,其中部分转化历程与能量变化如图所示:
 在一定条件下能发生如下反应,其中部分转化历程与能量变化如图所示:
在一定条件下能发生如下反应,其中部分转化历程与能量变化如图所示: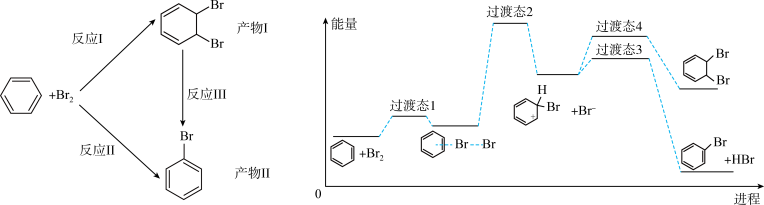
A.反应焓变:反应 >反应 >反应 |
B.在该条件下,反应 能自发进行 能自发进行 |
C.苯与 主要发生取代反应,生成有机主产物 主要发生取代反应,生成有机主产物 |
D.适当升高温度,生成产物 和产物 和产物 的速率均增大,同时可以提高产物 的速率均增大,同时可以提高产物 的选择性 的选择性 |
您最近一年使用:0次
名校
解题方法
6 . 某厂使用特定催化剂进行乙酸直接加氢制备乙醇,相关反应如下:
反应 :
:
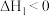
反应 :
:

回答下列问题:
(1)反应Ⅱ能自发进行的条件是___________ 。
(2)乙醇是重要的燃料,乙醇的燃烧热1366.8kJ/mol,请写出乙醇在常温常压下燃烧的热化学方程式___________ 。
(3)250℃下,恒压密闭容器中充入一定量H2(g)和CH3COOH(g),以下选项不能判断反应达到平衡状态的是___________。
(4)一定温度和压强下,向初始体积为2L的密闭容器中通入4molH2(g)和2molCH3COOH(g),同时发生两个反应,测得平衡时 ,体积减小20%,则平衡时,
,体积减小20%,则平衡时,
___________ mol/L,反应 的平衡常数
的平衡常数
___________ (mol/L)-1。
(5)在 时,发生两个反应,2MPa下,平衡时S(乙醇)和S(乙酸乙酯)随温度的变化如图一;250℃下,平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图二。
时,发生两个反应,2MPa下,平衡时S(乙醇)和S(乙酸乙酯)随温度的变化如图一;250℃下,平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图二。 。
。
①250℃下,乙醇选择性随压强变化的曲线是___________ (选填a或b)。
②请解释图一中乙醇选择性随温度升高而降低的原因___________ 。
③150℃时,在催化剂作用下H2(g)和CH3COOH(g)反应一段时间后,乙醇的选择性位于m点,不改变反应时间和温度,一定能提高乙醇选择性的措施___________ (填一条)。
反应
 :
:
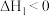
反应
 :
:

回答下列问题:
(1)反应Ⅱ能自发进行的条件是
(2)乙醇是重要的燃料,乙醇的燃烧热1366.8kJ/mol,请写出乙醇在常温常压下燃烧的热化学方程式
(3)250℃下,恒压密闭容器中充入一定量H2(g)和CH3COOH(g),以下选项不能判断反应达到平衡状态的是___________。
| A.混合气体的密度保持不变 | B. |
| C.体系的总压保持不变 | D.CH3COOH的体积分数不变 |
(4)一定温度和压强下,向初始体积为2L的密闭容器中通入4molH2(g)和2molCH3COOH(g),同时发生两个反应,测得平衡时
 ,体积减小20%,则平衡时,
,体积减小20%,则平衡时,
 的平衡常数
的平衡常数
(5)在
 时,发生两个反应,2MPa下,平衡时S(乙醇)和S(乙酸乙酯)随温度的变化如图一;250℃下,平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图二。
时,发生两个反应,2MPa下,平衡时S(乙醇)和S(乙酸乙酯)随温度的变化如图一;250℃下,平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图二。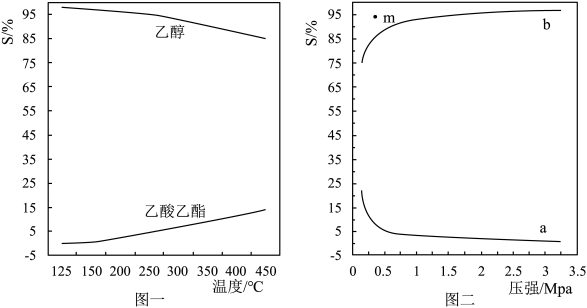
 。
。①250℃下,乙醇选择性随压强变化的曲线是
②请解释图一中乙醇选择性随温度升高而降低的原因
③150℃时,在催化剂作用下H2(g)和CH3COOH(g)反应一段时间后,乙醇的选择性位于m点,不改变反应时间和温度,一定能提高乙醇选择性的措施
您最近一年使用:0次
名校
7 . 运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
生产氢气:将水蒸气通过红热的炭即产生水煤气,其反应为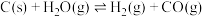
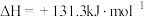 ,
,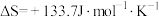
(1)试判断该反应在常温下能否自发进行_________ 。(写出计算过程)
(2)写出该反应的平衡常数表达式___________ 。
生产氢气:将水蒸气通过红热的炭即产生水煤气,其反应为
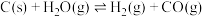
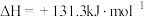 ,
,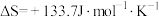
(1)试判断该反应在常温下能否自发进行
(2)写出该反应的平衡常数表达式
您最近一年使用:0次
2024·江苏·模拟预测
名校
8 . 利用碳氯化反应TiO2(s)+2Cl2(g)+2C(s) TiCl4(g)+2CO(g) ΔH =-51 kJ·mol-1,可将TiO2转化为TiCl4,再进一步还原得到金属钛,下列说法正确的是
TiCl4(g)+2CO(g) ΔH =-51 kJ·mol-1,可将TiO2转化为TiCl4,再进一步还原得到金属钛,下列说法正确的是
 TiCl4(g)+2CO(g) ΔH =-51 kJ·mol-1,可将TiO2转化为TiCl4,再进一步还原得到金属钛,下列说法正确的是
TiCl4(g)+2CO(g) ΔH =-51 kJ·mol-1,可将TiO2转化为TiCl4,再进一步还原得到金属钛,下列说法正确的是| A.碳氯化反应在高温下不能自发进行 |
| B.加压、降温均可增大生成TiCl4的速率 |
| C.反应中每消耗80g TiO2,转移电子的数目约为4×6.02×1023 |
| D.将TiO2(s)与C(s)粉碎并混合均匀后反应可提高Cl2的平衡转化率 |
您最近一年使用:0次
2024-05-01更新
|
269次组卷
|
6卷引用:江苏省泰州中学2023-2024学年高二下学期5月期中考试化学试题
江苏省泰州中学2023-2024学年高二下学期5月期中考试化学试题江苏省盐城市五校联盟2023-2024学年高二下学期5月月考化学试题(已下线)化学(江苏卷02)-2024年高考押题预测卷(已下线)江苏省连云港市2023-2024学年高三下学期三模冲刺化学试题专题7 化学反应速率与化学平衡-化学反应速率及影响因素专题7 化学反应速率与化学平衡-化学平衡状态及平衡移动
解题方法
9 . 氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。生产硝酸的尾气中主要含有NO、NO2等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO3)2、Ca(NO2)2等化工产品。工业上用氨的催化氧化生产硝酸,其热化学方程式为4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ∆H=-904kJ•mol-1。对于反应4NH3(g)+5O2(g)
4NO(g)+6H2O(g) ∆H=-904kJ•mol-1。对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列有关说法正确的是
4NO(g)+6H2O(g),下列有关说法正确的是
 4NO(g)+6H2O(g) ∆H=-904kJ•mol-1。对于反应4NH3(g)+5O2(g)
4NO(g)+6H2O(g) ∆H=-904kJ•mol-1。对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列有关说法正确的是
4NO(g)+6H2O(g),下列有关说法正确的是| A.该反应只有在高温条件下能自发进行 |
| B.该反应的正反应的活化能小于逆反应的活化能 |
| C.达到平衡时,升高温度,v(正)减小、v(逆)增加 |
| D.c(NH3):c(O2):c(NO):c(H2O)=4:5:4:6时,说明反应达到平衡 |
您最近一年使用:0次
10 . 天然气经催化重整转化成合成气(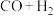 )后再合成其他化工产品,既可减少能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下两个反应:
)后再合成其他化工产品,既可减少能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下两个反应:
反应Ⅰ:

反应Ⅱ:

(1)反应Ⅰ可分为如下两步:
 裂解:
裂解: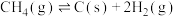
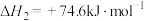
 重整:
重整: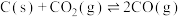
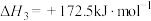
则 =
=______ 。反应Ⅰ能够自发进行的条件是______ ,判断依据是______ 。
(2) ℃时,向4L容器中通入7mol
℃时,向4L容器中通入7mol 、6mol
、6mol ,发生反应Ⅰ、Ⅱ.
,发生反应Ⅰ、Ⅱ. min后达到平衡,体系中
min后达到平衡,体系中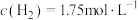 ,
,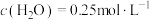 ,压强为
,压强为 。①此温度下,反应Ⅰ的平衡常数
。①此温度下,反应Ⅰ的平衡常数 =
=______ (写出计算式即可,不必化简)[对于气相反应,用某组分B的平衡压强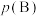 代替物质的量浓度
代替物质的量浓度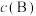 表示的平衡常数,记作
表示的平衡常数,记作 ,如
,如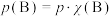 ,
, 为平衡总压强,
为平衡总压强,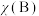 为平衡系统中B的物质的量分数]。
为平衡系统中B的物质的量分数]。
②请在图中画出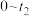 时段
时段 随时间变化曲线并标出
随时间变化曲线并标出 的平衡浓度
的平衡浓度______ 。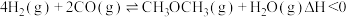
①在恒温恒压条件进行此反应,下列能说明反应已达到平衡的是______ (填标号)。
A. 、
、 、
、 、
、 的反应速率之比为4:2:1:1
的反应速率之比为4:2:1:1
B. 、
、 、
、 、
、 的物质的量之比为4:2:1:1
的物质的量之比为4:2:1:1
C.混合气体的平均摩尔质量保持不变
D.容器中气体的密度保持不变
②某温度下,将2.0mol 和4.0mol
和4.0mol 充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中
充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中 的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是
的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是______ (填标号)。 ,
,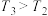 B.
B. ,
,
C. ,
, D.
D. ,
,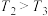
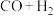 )后再合成其他化工产品,既可减少能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下两个反应:
)后再合成其他化工产品,既可减少能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下两个反应:反应Ⅰ:


反应Ⅱ:


(1)反应Ⅰ可分为如下两步:
 裂解:
裂解: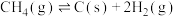
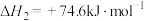
 重整:
重整: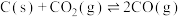
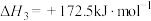
则
 =
=(2)
 ℃时,向4L容器中通入7mol
℃时,向4L容器中通入7mol 、6mol
、6mol ,发生反应Ⅰ、Ⅱ.
,发生反应Ⅰ、Ⅱ. min后达到平衡,体系中
min后达到平衡,体系中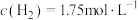 ,
,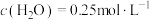 ,压强为
,压强为 。①此温度下,反应Ⅰ的平衡常数
。①此温度下,反应Ⅰ的平衡常数 =
=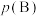 代替物质的量浓度
代替物质的量浓度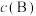 表示的平衡常数,记作
表示的平衡常数,记作 ,如
,如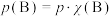 ,
, 为平衡总压强,
为平衡总压强,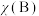 为平衡系统中B的物质的量分数]。
为平衡系统中B的物质的量分数]。②请在图中画出
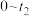 时段
时段 随时间变化曲线并标出
随时间变化曲线并标出 的平衡浓度
的平衡浓度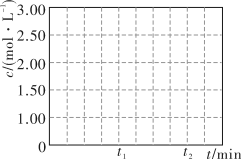
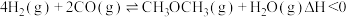
①在恒温恒压条件进行此反应,下列能说明反应已达到平衡的是
A.
 、
、 、
、 、
、 的反应速率之比为4:2:1:1
的反应速率之比为4:2:1:1B.
 、
、 、
、 、
、 的物质的量之比为4:2:1:1
的物质的量之比为4:2:1:1C.混合气体的平均摩尔质量保持不变
D.容器中气体的密度保持不变
②某温度下,将2.0mol
 和4.0mol
和4.0mol 充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中
充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中 的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是
的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是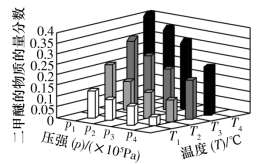
 ,
,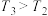 B.
B. ,
,
C.
 ,
, D.
D. ,
,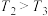
您最近一年使用:0次



