1 .  是重要的化工原料。工业合成氨,关乎到世界化工发展与粮食的安全,对其研究意义重大。自由能
是重要的化工原料。工业合成氨,关乎到世界化工发展与粮食的安全,对其研究意义重大。自由能 (单位
(单位 )可用于判断一定温度下反应的自发性,
)可用于判断一定温度下反应的自发性,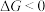 能自发,
能自发, 。工业合成氨的反应为:
。工业合成氨的反应为: 在
在 时该反应的
时该反应的 ,
,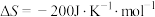 。实验研究表明,在用铁触媒作催化剂的条件下,合成氨反应速率与反应的物质的浓度关系为
。实验研究表明,在用铁触媒作催化剂的条件下,合成氨反应速率与反应的物质的浓度关系为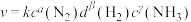 ,
, 是速率常数。下列说法不正确的是
是速率常数。下列说法不正确的是
 是重要的化工原料。工业合成氨,关乎到世界化工发展与粮食的安全,对其研究意义重大。自由能
是重要的化工原料。工业合成氨,关乎到世界化工发展与粮食的安全,对其研究意义重大。自由能 (单位
(单位 )可用于判断一定温度下反应的自发性,
)可用于判断一定温度下反应的自发性,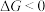 能自发,
能自发, 。工业合成氨的反应为:
。工业合成氨的反应为: 在
在 时该反应的
时该反应的 ,
,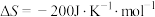 。实验研究表明,在用铁触媒作催化剂的条件下,合成氨反应速率与反应的物质的浓度关系为
。实验研究表明,在用铁触媒作催化剂的条件下,合成氨反应速率与反应的物质的浓度关系为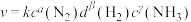 ,
, 是速率常数。下列说法不正确的是
是速率常数。下列说法不正确的是A.在 时,该反应能自发进行 时,该反应能自发进行 |
| B.合成氨反应活化能较大,需要外界提供能量才能发生 |
| C.温度升高,使用铁触媒,反应物活化分子百分数增大,反应速率加快 |
D. ,恒容容器中充入 ,恒容容器中充入 和 和 ,充分反应放出的热量为 ,充分反应放出的热量为 |
您最近一年使用:0次
名校
2 . 下列说法中错误的是
| A.分子发生有效碰撞的条件之一是能量达到活化能 |
| B.对于等物质的量的同一物质在不同状态时的熵值:气态>液态>固态 |
C.稀释明矾(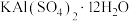 )水溶液,会使 )水溶液,会使 水解程度增大,溶液pH降低 水解程度增大,溶液pH降低 |
| D.平衡常数K值越大,则可逆反应进行越完全,反应物的转化率越大 |
您最近一年使用:0次
名校
3 . 钛被称为继铁、铝之后的第三金属,性能优越,广泛用于航天航空等领域,有人说“21世纪将是钛的世纪”。冶炼金属钛的主要原料为钛铁矿(主要成分 ,含FeO、
,含FeO、 等杂质),其冶炼过程如图所示,除了得到金属钛,还可以得到副产物绿矾(
等杂质),其冶炼过程如图所示,除了得到金属钛,还可以得到副产物绿矾( )。
)。
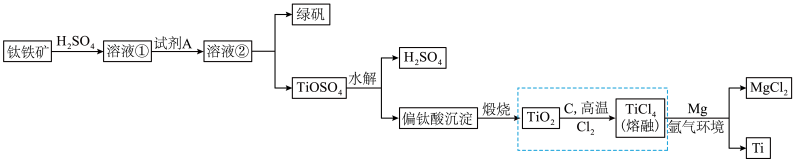
(1)Ti在元素周期表中的位置为___________ , 的键角
的键角___________  分子的键角(填“>”“<”或“=”)。
分子的键角(填“>”“<”或“=”)。
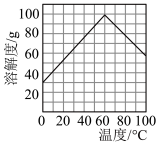
(2)试剂A为___________ 。已知绿矾的溶解度随温度变化的曲线如下图所示,获得从溶液②绿矾的操作方法为___________ ,过滤、洗涤、干燥。
(3)已知常温下,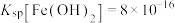 ,若溶液②中
,若溶液②中 ,为防止生成
,为防止生成 沉淀,溶液的pH不超过
沉淀,溶液的pH不超过___________ ( )。
)。
(4) 水解生成偏钛酸(
水解生成偏钛酸( )沉淀的化学方程式为
)沉淀的化学方程式为___________ 。虚线框内的流程是经过大量科学研究后得到的方法,科学家原来的设想为
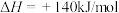 ,但无法实现,试从反应自发性角度来解释该设想无法实现的原因
,但无法实现,试从反应自发性角度来解释该设想无法实现的原因___________ 。
(5) 的水解程度很大,可以利用其稀溶液制备纳米级
的水解程度很大,可以利用其稀溶液制备纳米级 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
 ,含FeO、
,含FeO、 等杂质),其冶炼过程如图所示,除了得到金属钛,还可以得到副产物绿矾(
等杂质),其冶炼过程如图所示,除了得到金属钛,还可以得到副产物绿矾( )。
)。
(1)Ti在元素周期表中的位置为
 的键角
的键角 分子的键角(填“>”“<”或“=”)。
分子的键角(填“>”“<”或“=”)。(2)试剂A为

(3)已知常温下,
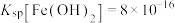 ,若溶液②中
,若溶液②中 ,为防止生成
,为防止生成 沉淀,溶液的pH不超过
沉淀,溶液的pH不超过 )。
)。(4)
 水解生成偏钛酸(
水解生成偏钛酸( )沉淀的化学方程式为
)沉淀的化学方程式为
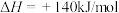 ,但无法实现,试从反应自发性角度来解释该设想无法实现的原因
,但无法实现,试从反应自发性角度来解释该设想无法实现的原因(5)
 的水解程度很大,可以利用其稀溶液制备纳米级
的水解程度很大,可以利用其稀溶液制备纳米级 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
名校
4 . 根据所学知识完成下列问题:
(1)某小组同学用量筒分别量取50mL的0.50mol∙L-1HC1溶液与50mL的0.55mol∙L-1NaOH溶液来测定中和热。
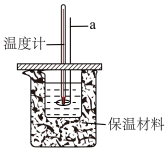
①仪器a是___________ (填名称)。
②近似认为0.55mol/L的NaOH溶液和0.50mol/L的HCl溶液的密度都是1g/mL,中和后生成溶液的比热容c=4.18J∙g-1∙℃-1,并忽略量热计的比热容;测得反应前、后体系的温度值(℃)分别为T0、T1,则所测中和热为△H=___________ kJ·mol-1(用含T0、T1的代数式表示)。
③若量取盐酸时候俯视刻度线,且其他操作无误,最终会使测得的中和热△H___________ (填“不变”、“变大”或“变小”)。
(2)研究氮和硫的氧化物的无害化处理对治理大气污染有着重要意义:
①已知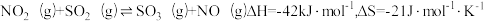 ,该反应能够自发进行的温度条件是
,该反应能够自发进行的温度条件是___________ K。
②将NO2和SO2以物质的量比1:2置于一体积不变的密闭容器中,在绝热条件下发生上述反应,下列不能说明该反应到达平衡状态的是:___________
a.每消耗1molNO2同时生成1molSO3 b.混合气体的颜色保持不变
c.体系的压强保持不变 d.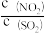 保持不变
保持不变
e.混合气体的平均摩尔质量保持不变
(3)HCN的电子式为___________ 。25℃时,HCN溶液与同浓度同体积的NaOH溶液充分反应后,最终pH为11.9,用离子方程式说明最终溶液虽碱性的原因:___________ 。
(4)阻燃剂Sb2O3(三氧化二铋)一般由SbCl3水解制备。实验室模拟制备过程如下:先将SbC13于一定条件下水解生成SbOC1白色沉淀,这一步的化学方程式为___________ ,再往其中加入少量氨水并搅拌,最终生成Sb2O3。
(1)某小组同学用量筒分别量取50mL的0.50mol∙L-1HC1溶液与50mL的0.55mol∙L-1NaOH溶液来测定中和热。

①仪器a是
②近似认为0.55mol/L的NaOH溶液和0.50mol/L的HCl溶液的密度都是1g/mL,中和后生成溶液的比热容c=4.18J∙g-1∙℃-1,并忽略量热计的比热容;测得反应前、后体系的温度值(℃)分别为T0、T1,则所测中和热为△H=
③若量取盐酸时候俯视刻度线,且其他操作无误,最终会使测得的中和热△H
(2)研究氮和硫的氧化物的无害化处理对治理大气污染有着重要意义:
①已知
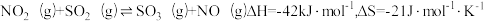 ,该反应能够自发进行的温度条件是
,该反应能够自发进行的温度条件是②将NO2和SO2以物质的量比1:2置于一体积不变的密闭容器中,在绝热条件下发生上述反应,下列不能说明该反应到达平衡状态的是:
a.每消耗1molNO2同时生成1molSO3 b.混合气体的颜色保持不变
c.体系的压强保持不变 d.
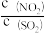 保持不变
保持不变e.混合气体的平均摩尔质量保持不变
(3)HCN的电子式为
(4)阻燃剂Sb2O3(三氧化二铋)一般由SbCl3水解制备。实验室模拟制备过程如下:先将SbC13于一定条件下水解生成SbOC1白色沉淀,这一步的化学方程式为
您最近一年使用:0次
2023-12-13更新
|
143次组卷
|
2卷引用:广东省东莞市东莞中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
5 . 通过化学的方法实现 的资源化利用是一种理想的
的资源化利用是一种理想的 减排途径,由
减排途径,由 和
和 制备
制备 (二甲醚,被誉为“21世纪的清洁燃料”)的反应原理如下:
(二甲醚,被誉为“21世纪的清洁燃料”)的反应原理如下:
a.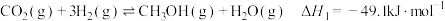
b.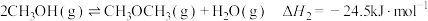
c.
已知: ,如:
,如: 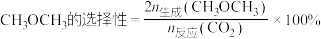 。
。
回答下列问题:
(1)写出 与
与 转化为
转化为 和
和 (反应d)的热化学方程式
(反应d)的热化学方程式______________________ 。
(2)反应a达到平衡时,若缩小体积增大压强,则 变
变____________ (填“大”或“小”)。
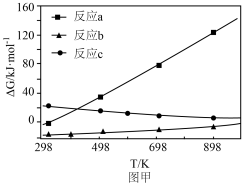
(3)反应a、b、c的吉布斯自由能随温度变化如图甲所示,298K时,能自发进行的反应有___________ ;反应c为熵______________ (填“增”或“减”)反应。
(4)向体积为 的恒压密闭容器中充入
的恒压密闭容器中充入 和
和 ,若仅考点上述反应,平衡时
,若仅考点上述反应,平衡时 和
和 的选择性及
的选择性及 的转化率随温度的变化如图乙实线所示。
的转化率随温度的变化如图乙实线所示。
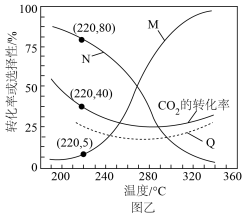
①图中曲线____________ (填“N”或“M”)表示 的选择性。
的选择性。
②平衡时 的转化率随温度的变化
的转化率随温度的变化____________ (填“可能”或“不可能”)如图中虚线Q所示。
③温度高于270℃,随着温度的升高, 的平衡转化率如图所示变化的原因是
的平衡转化率如图所示变化的原因是___________________ 。
④计算反应 在220℃下的平衡常数为
在220℃下的平衡常数为______________ (结果保留三位有效数字)。
 的资源化利用是一种理想的
的资源化利用是一种理想的 减排途径,由
减排途径,由 和
和 制备
制备 (二甲醚,被誉为“21世纪的清洁燃料”)的反应原理如下:
(二甲醚,被誉为“21世纪的清洁燃料”)的反应原理如下:a.
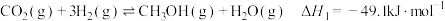
b.
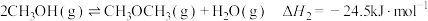
c.

已知:
 ,如:
,如: 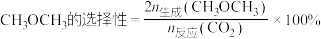 。
。回答下列问题:
(1)写出
 与
与 转化为
转化为 和
和 (反应d)的热化学方程式
(反应d)的热化学方程式(2)反应a达到平衡时,若缩小体积增大压强,则
 变
变(3)反应a、b、c的吉布斯自由能随温度变化如图甲所示,298K时,能自发进行的反应有

(4)向体积为
 的恒压密闭容器中充入
的恒压密闭容器中充入 和
和 ,若仅考点上述反应,平衡时
,若仅考点上述反应,平衡时 和
和 的选择性及
的选择性及 的转化率随温度的变化如图乙实线所示。
的转化率随温度的变化如图乙实线所示。
①图中曲线
 的选择性。
的选择性。②平衡时
 的转化率随温度的变化
的转化率随温度的变化③温度高于270℃,随着温度的升高,
 的平衡转化率如图所示变化的原因是
的平衡转化率如图所示变化的原因是④计算反应
 在220℃下的平衡常数为
在220℃下的平衡常数为
您最近一年使用:0次
2023-12-12更新
|
197次组卷
|
2卷引用:重庆市育才中学校、西南大学附中、万州中学2023-2024学年高二上学期12月联考化学试题
名校
6 . 由下列实验事实所得出的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 某温度下,向容积可变的密闭容器中加入足量CaCO3,发生反应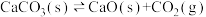 ,并达到平衡,将容器容积增大为原来的2倍 ,并达到平衡,将容器容积增大为原来的2倍 | 当体系再次达到平衡时,气体密度不变 |
| B | 恒温恒容条件下, ,增加 ,增加 的物质的量 的物质的量 | H2O的平衡转化率提高,且增大其反应速率 |
| C | 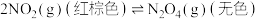  ,在反应达到平衡后,对平衡体系采取缩小容积、增大压强的措施, ,在反应达到平衡后,对平衡体系采取缩小容积、增大压强的措施, | 因为平衡向正反应方向移动,故体系颜色变浅 |
| D | 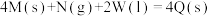 常温下,自发进行 常温下,自发进行 | 则ΔH>0 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 将CO2转化为CO、CH3OH等燃料,可以有效地缓解能源危机,同时可以减少温室气体,实现“双碳目标”。回答下列问题:
在CO2加氢合成甲醇的体系中,同时存在以下反应:
ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
已知下列物质总键能(1mol物质所含化学键的键能之和)的数据如表:
(1)①由此可求得△H=_________ kJ/mol。
②反应ⅱ△H2=+41.17 kJ/mol,△S=+42.08J/(mol·K),则反应ii在______ (填“高温”“低温”或“任意温度”)下可以自发进行。
③在恒容绝热条件下,下列说法能表明反应ii(不考虑反应i)达到平衡的是_______ (填字母)。
A.当混合气体的压强不再改变时
B.当混合气体的密度保持不变时
C.断开1molH-H键的同时断开2molH-O键
D.当混合气体的平均相对分子质量保持不变时
(2)在p=3.00MPa、原料气n(H2):n(CO2)=3:1、合适催化剂的条件下发生反应,温度对CO2转化率、CH3OH产率、CH3OH选择性的影响如图所示。已知:甲醇选择性(S-CH3OH)=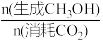 ×100%,CO2的平衡转化率(X-CO2)=
×100%,CO2的平衡转化率(X-CO2)=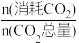 ×100%,甲醇的产率(Y-CH3OH)=X(CO2)×S(CH3OH)×100%。
×100%,甲醇的产率(Y-CH3OH)=X(CO2)×S(CH3OH)×100%。
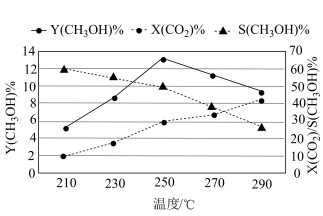
①CH3OH选择性随着温度的升高而降低的原因是__________________ 。
②根据上图,选择在________ ℃下合成CH3OH最佳,除调控合适的温度外,使CH3OH选择性增大的方法有________________ 。
③恒压,250℃条件下,在1L密闭容器中投入1molCO2和3molH2,反应ii的平衡常数K=_______ (保留两位有效数字)。
在CO2加氢合成甲醇的体系中,同时存在以下反应:
ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2已知下列物质总键能(1mol物质所含化学键的键能之和)的数据如表:
| 物质 | CO2(g) | H2(g) | CH3OH(g) | H2O(g) |
| 总键能/(kJ/mol) | 1620 | 436 | 2047 | 930 |
(1)①由此可求得△H=
②反应ⅱ△H2=+41.17 kJ/mol,△S=+42.08J/(mol·K),则反应ii在
③在恒容绝热条件下,下列说法能表明反应ii(不考虑反应i)达到平衡的是
A.当混合气体的压强不再改变时
B.当混合气体的密度保持不变时
C.断开1molH-H键的同时断开2molH-O键
D.当混合气体的平均相对分子质量保持不变时
(2)在p=3.00MPa、原料气n(H2):n(CO2)=3:1、合适催化剂的条件下发生反应,温度对CO2转化率、CH3OH产率、CH3OH选择性的影响如图所示。已知:甲醇选择性(S-CH3OH)=
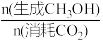 ×100%,CO2的平衡转化率(X-CO2)=
×100%,CO2的平衡转化率(X-CO2)=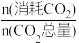 ×100%,甲醇的产率(Y-CH3OH)=X(CO2)×S(CH3OH)×100%。
×100%,甲醇的产率(Y-CH3OH)=X(CO2)×S(CH3OH)×100%。
①CH3OH选择性随着温度的升高而降低的原因是
②根据上图,选择在
③恒压,250℃条件下,在1L密闭容器中投入1molCO2和3molH2,反应ii的平衡常数K=
您最近一年使用:0次
8 . 在恒温下,向容积为2L的恒容容器中加入一定量的碳单质和2molH2O(g),初始压强为105Pa。发生反应: ∆H>0。经过2min后达到平衡,容器的压强增加了20%。
∆H>0。经过2min后达到平衡,容器的压强增加了20%。
(1)该反应自发进行的条件是__________ 。(填“高温”或“低温”或“任意条件”)
(2)2min内H2O的平均反应速率为__________ mol/(L·min)。
(3)2min平衡时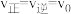 ,采取下列措施后,使
,采取下列措施后,使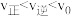 的是__________。
的是__________。
(4)平衡常数Kp=__________ Pa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)下列说法正确的是__________。
 ∆H>0。经过2min后达到平衡,容器的压强增加了20%。
∆H>0。经过2min后达到平衡,容器的压强增加了20%。(1)该反应自发进行的条件是
(2)2min内H2O的平均反应速率为
(3)2min平衡时
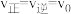 ,采取下列措施后,使
,采取下列措施后,使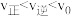 的是__________。
的是__________。| A.恒温恒容下,除去部分H2O | B.降低温度 |
| C.恒温恒容下,充入Ar | D.恒温恒压下,充入Ar |
(5)下列说法正确的是__________。
| A.增加碳单质,可以加快该反应速率 |
| B.2min时,H2O的转化率为20% |
| C.当混合气体的平均摩尔质量不再变化时,可以判断该反应达到了平衡 |
| D.平衡后向体系内补加0.4molH2O(g)和0.4molCO(g),反应向逆反应方向进行 |
您最近一年使用:0次
2023-12-11更新
|
177次组卷
|
2卷引用:浙江省绍兴市第一中学2023-2024学年高二上学期11月期中考试(平行班)化学试题
名校
9 . 下列有关叙述正确的是
①工业上通常采用铁触媒、400~500℃和10MPa~30Mpa的条件下合成氨
②等体积、等pH的盐酸和醋酸,分别与等浓度的NaOH反应,醋酸消耗的NaOH体积大
③化学平衡常数变化,化学平衡不一定发生移动
④通过压缩体积增大压强,可以提高单位体积内活化分子百分数,从而提高反应速率
⑤在中和反应反应热的测定实验中,每组实验至少三次使用温度计
⑥反应CaSO4(s)=CaO(s)+SO3(g) ∆H>0在高温下能自发进行
①工业上通常采用铁触媒、400~500℃和10MPa~30Mpa的条件下合成氨
②等体积、等pH的盐酸和醋酸,分别与等浓度的NaOH反应,醋酸消耗的NaOH体积大
③化学平衡常数变化,化学平衡不一定发生移动
④通过压缩体积增大压强,可以提高单位体积内活化分子百分数,从而提高反应速率
⑤在中和反应反应热的测定实验中,每组实验至少三次使用温度计
⑥反应CaSO4(s)=CaO(s)+SO3(g) ∆H>0在高温下能自发进行
| A.①②③⑥ | B.①②⑤⑥ | C.②④⑤⑥ | D.①③④⑤ |
您最近一年使用:0次
2023-12-06更新
|
127次组卷
|
3卷引用:内蒙古自治区优质高中联考2023-2024学年高二上学期11月期中化学试题
名校
解题方法
10 . 丁烯是石油化工基础原料,在石油化工烯烃原料中地位仅次于乙烯和丙烯,我国科学家研究不同催化剂下丁烷脱氢制丁烯,催化反应历程如图所示[注:标*的物质表示吸附在催化剂上的中间产物,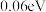 表示1个
表示1个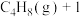 个
个 的能量)]:
的能量)]:
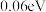 表示1个
表示1个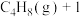 个
个 的能量)]:
的能量)]: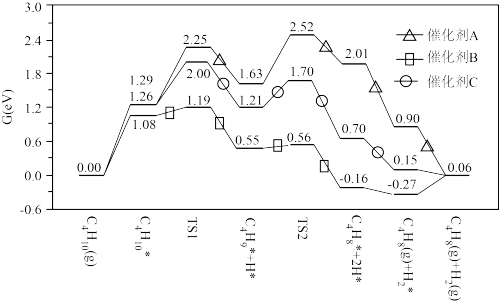
| A.图示历程中仅包含2个基元反应(一步直接转化为产物的反应) |
| B.三种催化剂催化效果最好的是催化剂B |
| C.该反应在高温条件下能自发进行 |
D.催化剂C时,决速反应的方程式为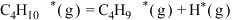 |
您最近一年使用:0次
2023-12-02更新
|
639次组卷
|
7卷引用:福建省龙岩第一中学2023-2024学年高二上学期第三次月考化学试题
福建省龙岩第一中学2023-2024学年高二上学期第三次月考化学试题贵州省贵阳市2023-2024学年高三上学期11月质量检测化学试题湖北省九师联盟2024届高三11月质检化学试题河南省部分名校2023-2024学年高三上学期11月期中化学试题江西省部分地区2023-2024学年高三上学期11月期中化学试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题06 化学反应速率与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)



