名校
解题方法
1 . 某废合金的主要成分为Sn、Cu、Pb、Fe,一种综合回收的工艺流程如图所示:
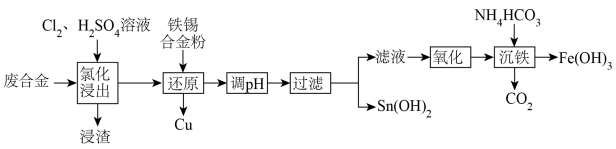
已知:常温下,Ksp(PbCl2)=1.6×10-5,Ksp(PbSO4)=1.6×10-8,Ksp[Sn(OH)2]=1.0×10-27.85。
回答下列问题:
(1)“氯化浸出”浸出液中金属阳离子主要有Sn4+、Cu2+、______ ;浸渣的主要成分为______ (填化学式)。“氯化没出”时温度不宜过高或过低的原因是_______ 。
(2)写出“还原”中Fe与SnCl4反应的化学方程式:_______ 。
(3)常温下,为使Sn2+完全沉淀,“调pH”时应使溶液pH不低于______ (结果保留1位小数)。
(4)写出“沉铁”时发生反应的离子反应方程式:_______ 。
(5)Fe(OH)3受热后可制得物质A,写出物质A的一种用途:______ 。

已知:常温下,Ksp(PbCl2)=1.6×10-5,Ksp(PbSO4)=1.6×10-8,Ksp[Sn(OH)2]=1.0×10-27.85。
回答下列问题:
(1)“氯化浸出”浸出液中金属阳离子主要有Sn4+、Cu2+、
(2)写出“还原”中Fe与SnCl4反应的化学方程式:
(3)常温下,为使Sn2+完全沉淀,“调pH”时应使溶液pH不低于
(4)写出“沉铁”时发生反应的离子反应方程式:
(5)Fe(OH)3受热后可制得物质A,写出物质A的一种用途:
您最近一年使用:0次
2 . 氯化银在水中存在沉淀溶解平衡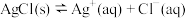 ,将足量
,将足量 分别加入下列溶液中,
分别加入下列溶液中, 最大的是,
最大的是,
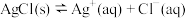 ,将足量
,将足量 分别加入下列溶液中,
分别加入下列溶液中, 最大的是,
最大的是,
A. 盐酸 盐酸 | B. 溶液 溶液 |
C. 溶液 溶液 | D.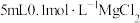 溶液 溶液 |
您最近一年使用:0次
名校
解题方法
3 . 利用炼锌钴渣[主要含 、
、 、
、 和
和 、
、 单质]协同制备
单质]协同制备 和高纯
和高纯 的流程如下。
的流程如下。 发生反应的离子方程式为
发生反应的离子方程式为____________________ 。
(2)“沉铁”过程 的作用有
的作用有____________________ 。
(3)“沉镍”过程 对溶液中
对溶液中 (Ⅱ)、
(Ⅱ)、 (Ⅱ)含量的影响如图。
(Ⅱ)含量的影响如图。
__________ 。
②该过程 可能发生的反应如下:
可能发生的反应如下:
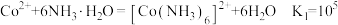
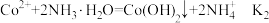
则
__________ , 为
为__________ (填“热力学”或“动力学”)产物。
(已知: 时,
时,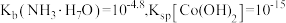 )
)
(4)“沉钴”过程生成 的离子方程式为
的离子方程式为______________________________ 。
(5)“电解”过程阴极生成 的电极反应式为
的电极反应式为____________________ 。金属 的晶胞如图,密度为
的晶胞如图,密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
_________ 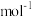 (列代数式即可,下同),晶胞空间占有率为
(列代数式即可,下同),晶胞空间占有率为__________ 。
 、
、 、
、 和
和 、
、 单质]协同制备
单质]协同制备 和高纯
和高纯 的流程如下。
的流程如下。
 发生反应的离子方程式为
发生反应的离子方程式为(2)“沉铁”过程
 的作用有
的作用有(3)“沉镍”过程
 对溶液中
对溶液中 (Ⅱ)、
(Ⅱ)、 (Ⅱ)含量的影响如图。
(Ⅱ)含量的影响如图。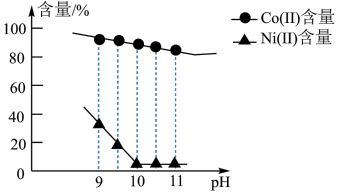

②该过程
 可能发生的反应如下:
可能发生的反应如下: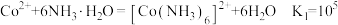
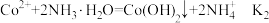
则

 为
为(已知:
 时,
时,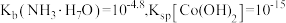 )
)(4)“沉钴”过程生成
 的离子方程式为
的离子方程式为(5)“电解”过程阴极生成
 的电极反应式为
的电极反应式为 的晶胞如图,密度为
的晶胞如图,密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
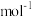 (列代数式即可,下同),晶胞空间占有率为
(列代数式即可,下同),晶胞空间占有率为
您最近一年使用:0次
2024-03-07更新
|
444次组卷
|
3卷引用:福建省厦门市2024届高三下学期第二次质检化学试题
福建省厦门市2024届高三下学期第二次质检化学试题福建省宁化市第一中学2023-2024学年高三下学期3月质量检测化学试题(已下线)大题预测卷(新七省高考专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
名校
解题方法
4 . 下列实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 快速拉伸装有 的针筒活塞,气体颜色变浅 的针筒活塞,气体颜色变浅 | 证明压强改变对平衡的影响 |
| B | 常温下,测物质的量浓度相等的HA和HB溶液的 | 比较HA与HB的酸性强弱 |
| C | 用 稀硫酸与足量纯锌反应,产生气泡速率较慢,加入 稀硫酸与足量纯锌反应,产生气泡速率较慢,加入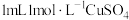 溶液后,迅速产生较多气泡 溶液后,迅速产生较多气泡 | 证明反应速率会随反应物浓度的增大而加快 |
| D | 向 硝酸银溶液中加入 硝酸银溶液中加入 溶液,出现白色沉淀,再加入几滴 溶液,出现白色沉淀,再加入几滴 的 的 溶液,有黑色沉淀生成 溶液,有黑色沉淀生成 | 证明在相同温度下的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 .  是一种治疗牙本质过敏症的牙膏添加剂。一种用工业碳酸锶(含少量
是一种治疗牙本质过敏症的牙膏添加剂。一种用工业碳酸锶(含少量 、FeO杂质)制取氯化锶晶体
、FeO杂质)制取氯化锶晶体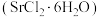 的工业流程如下
的工业流程如下错误 的是
 是一种治疗牙本质过敏症的牙膏添加剂。一种用工业碳酸锶(含少量
是一种治疗牙本质过敏症的牙膏添加剂。一种用工业碳酸锶(含少量 、FeO杂质)制取氯化锶晶体
、FeO杂质)制取氯化锶晶体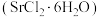 的工业流程如下
的工业流程如下
A.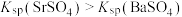 |
B.溶液I中发生了反应 |
C.工业碳酸锶的纯度为 |
| D.系列操作包括蒸发浓缩、冷却结晶等操作 |
您最近一年使用:0次
6 . 苯胺焦油是工业上催化制苯胺的副产物,主要成分为苯胺,含有少量铂族贵金属、活性炭和Na、K、Fe。回收其中贵金属Pt、Pd的工艺流程如下:
(1)“溶解”时
①溶解的目的是去除焦油中的苯胺,若采用直接焚烧的方法去除苯胺会生成______ (写一种),造成环境污染。
②苯胺易溶于乙醇的原因为______ 。
(2)“还原Ⅰ”时,PtO2、PdO被还原为金属单质。反应前后碳原子的杂化方式由______ 变为______ 。
(3)“氧化浸出”时浸出液含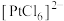 、
、 。
。
①王水是浓盐酸和浓硝酸体积比3:1的混合液,写出生成 的离子反应方程式
的离子反应方程式______ 。
②从原子结构角度分析两种配合物配位数不同的原因是______ 。
③下图为Pt、Pd浸出率与浸出温度关系图,氧化浸出需对温度适度控制,有关说法正确的是______ (选填序号)。
b.温度控制在120℃左右
c.温度越高浸出率越低的原因可能是挥发导致王水浓度降低
d.40℃时Pt的浸出率远低于Pd是因为温度低王水的氧化性弱
(4)“沉铂”时,已知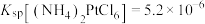 。
。
①发生反应的化学反应方程式为______ 。
②若NH4Cl的投料以固液比0.0535:1(g : mL)时 的消耗率为90%(忽略溶液体积变化),“沉铂”所得溶液中Pt元素的物质的量浓度为
的消耗率为90%(忽略溶液体积变化),“沉铂”所得溶液中Pt元素的物质的量浓度为______ mol∙L-1。
(5)“还原Ⅱ”时氧化产物为无毒气体,则该反应的氧化剂和还原剂的物质的量之比为______ 。

(1)“溶解”时
①溶解的目的是去除焦油中的苯胺,若采用直接焚烧的方法去除苯胺会生成
②苯胺易溶于乙醇的原因为
(2)“还原Ⅰ”时,PtO2、PdO被还原为金属单质。反应前后碳原子的杂化方式由
(3)“氧化浸出”时浸出液含
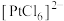 、
、 。
。①王水是浓盐酸和浓硝酸体积比3:1的混合液,写出生成
 的离子反应方程式
的离子反应方程式②从原子结构角度分析两种配合物配位数不同的原因是
③下图为Pt、Pd浸出率与浸出温度关系图,氧化浸出需对温度适度控制,有关说法正确的是
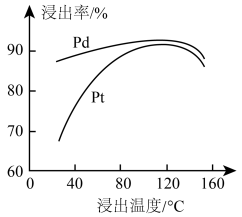
b.温度控制在120℃左右
c.温度越高浸出率越低的原因可能是挥发导致王水浓度降低
d.40℃时Pt的浸出率远低于Pd是因为温度低王水的氧化性弱
(4)“沉铂”时,已知
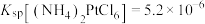 。
。①发生反应的化学反应方程式为
②若NH4Cl的投料以固液比0.0535:1(g : mL)时
 的消耗率为90%(忽略溶液体积变化),“沉铂”所得溶液中Pt元素的物质的量浓度为
的消耗率为90%(忽略溶液体积变化),“沉铂”所得溶液中Pt元素的物质的量浓度为(5)“还原Ⅱ”时氧化产物为无毒气体,则该反应的氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
名校
解题方法
7 . 硫代硫酸银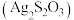 为白色固体,受热易分解且具有还原性,可用作乙烯抑制剂。某课外小组向
为白色固体,受热易分解且具有还原性,可用作乙烯抑制剂。某课外小组向 溶液中逐滴滴加
溶液中逐滴滴加 溶液制备
溶液制备 。实验记录如下。
。实验记录如下。
已知:Ⅰ.①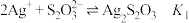
②
Ⅱ.相关物质的 :
:

(1) 中配位原子为
中配位原子为_______ ,配体阴离子的空间构型是_______ 。
(2)实验中沉淀溶解的总反应为: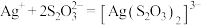 ,其平衡常数
,其平衡常数
_______ (用含 、
、 的代数式表示)。
的代数式表示)。
(3)用平衡移动原理解释实验中随 溶液滴入,又产生白色沉淀的原因是
溶液滴入,又产生白色沉淀的原因是_______ 。
(4)设计如下实验证明实验过程中产生的沉淀除了含有 外,还含有S和
外,还含有S和 。
。
取少量沉淀,加入足量_______ (填标号),充分振荡,过滤得滤液a和固体b。
A.乙醇 B.乙醚 C.丙酮 D.
i.取滤液a蒸馏可得黄色物质,证明沉淀中含有S。
ii.取固体b,_______ ,证明沉淀中含有 。(可供选择的试剂:稀硫酸、稀盐酸、稀硝酸、
。(可供选择的试剂:稀硫酸、稀盐酸、稀硝酸、 溶液)
溶液)
(5)查阅资料可知: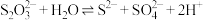 。实验证明:实验中S产生的主要原因是
。实验证明:实验中S产生的主要原因是 被
被 氧化而非被
氧化而非被 氧化。从反应速率的角度解释其原因:i.等浓度
氧化。从反应速率的角度解释其原因:i.等浓度 的氧化性大于
的氧化性大于 ,氧化
,氧化 的速率更快;ii.
的速率更快;ii._______ 。
(6)制备 时需及时分离出白色沉淀的原因是
时需及时分离出白色沉淀的原因是_______ 。
(7) 中的银元素在乙烯抑制剂中发挥重要的作用。该小组同学测定制得的白色固体中银的质量分数,具体实验过程如下。取
中的银元素在乙烯抑制剂中发挥重要的作用。该小组同学测定制得的白色固体中银的质量分数,具体实验过程如下。取 白色固体,加入适量硝酸充分反应,所得溶液加水稀释至
白色固体,加入适量硝酸充分反应,所得溶液加水稀释至 。再取
。再取 稀溶液于锥形瓶中,加入指示剂用
稀溶液于锥形瓶中,加入指示剂用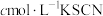 溶液进行滴定,重复滴定2~3次,平均消耗
溶液进行滴定,重复滴定2~3次,平均消耗 溶液的体积为
溶液的体积为 。已知:
。已知:
①选用的指示剂是_______ (填标号)。
A. B.
B. C.
C. D.
D.
②若未加入适量硝酸充分反应,会导致测量结果_______ (填“偏高”、“偏低”或“无影响”)。
③白色固体中银的质量分数为_______ %。
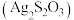 为白色固体,受热易分解且具有还原性,可用作乙烯抑制剂。某课外小组向
为白色固体,受热易分解且具有还原性,可用作乙烯抑制剂。某课外小组向 溶液中逐滴滴加
溶液中逐滴滴加 溶液制备
溶液制备 。实验记录如下。
。实验记录如下。| 操作 | 试剂a | 试剂b | 实验现象 |
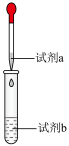 |  溶液 溶液 | 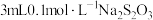 溶液 溶液 | 开始有白色沉淀,振荡后溶解,随 溶液滴入,又产生白色沉淀,而后沉淀逐渐变成黄色,最终变成黑色 溶液滴入,又产生白色沉淀,而后沉淀逐渐变成黄色,最终变成黑色 |
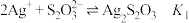
②

Ⅱ.相关物质的
 :
:| 物质 |  |  |  |
 | 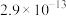 | 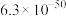 |  |

(1)
 中配位原子为
中配位原子为(2)实验中沉淀溶解的总反应为:
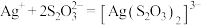 ,其平衡常数
,其平衡常数
 、
、 的代数式表示)。
的代数式表示)。(3)用平衡移动原理解释实验中随
 溶液滴入,又产生白色沉淀的原因是
溶液滴入,又产生白色沉淀的原因是(4)设计如下实验证明实验过程中产生的沉淀除了含有
 外,还含有S和
外,还含有S和 。
。取少量沉淀,加入足量
A.乙醇 B.乙醚 C.丙酮 D.

i.取滤液a蒸馏可得黄色物质,证明沉淀中含有S。
ii.取固体b,
 。(可供选择的试剂:稀硫酸、稀盐酸、稀硝酸、
。(可供选择的试剂:稀硫酸、稀盐酸、稀硝酸、 溶液)
溶液)(5)查阅资料可知:
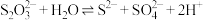 。实验证明:实验中S产生的主要原因是
。实验证明:实验中S产生的主要原因是 被
被 氧化而非被
氧化而非被 氧化。从反应速率的角度解释其原因:i.等浓度
氧化。从反应速率的角度解释其原因:i.等浓度 的氧化性大于
的氧化性大于 ,氧化
,氧化 的速率更快;ii.
的速率更快;ii.(6)制备
 时需及时分离出白色沉淀的原因是
时需及时分离出白色沉淀的原因是(7)
 中的银元素在乙烯抑制剂中发挥重要的作用。该小组同学测定制得的白色固体中银的质量分数,具体实验过程如下。取
中的银元素在乙烯抑制剂中发挥重要的作用。该小组同学测定制得的白色固体中银的质量分数,具体实验过程如下。取 白色固体,加入适量硝酸充分反应,所得溶液加水稀释至
白色固体,加入适量硝酸充分反应,所得溶液加水稀释至 。再取
。再取 稀溶液于锥形瓶中,加入指示剂用
稀溶液于锥形瓶中,加入指示剂用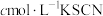 溶液进行滴定,重复滴定2~3次,平均消耗
溶液进行滴定,重复滴定2~3次,平均消耗 溶液的体积为
溶液的体积为 。已知:
。已知:
①选用的指示剂是
A.
 B.
B. C.
C. D.
D.
②若未加入适量硝酸充分反应,会导致测量结果
③白色固体中银的质量分数为
您最近一年使用:0次
名校
解题方法
8 . 一种从废钯催化剂(主要成分为 、
、 、
、 、活性炭,还含少量铁、铜等)中回收海绵钯(
、活性炭,还含少量铁、铜等)中回收海绵钯( )的工艺流程如图所示。
)的工艺流程如图所示。

(1)“焙烧”的目的___________ 。
(2)还原I中甲酸与 反应生成
反应生成 和
和 ,该反应中氧化剂和还原剂的物质的量之比为
,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(3)“酸浸”过程中 转化为
转化为 的离子方程式为
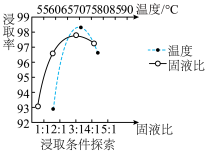
的离子方程式为___________ 。温度、固液比对酸浸浸取率的影响如图,则“酸浸”的最佳条件为___________ 。
(4)“离子交换”和“洗脱”可简单表示为: ,(
,( 为阴离子交换树脂)。试剂
为阴离子交换树脂)。试剂 的化学式为
的化学式为___________ 。流出液含有 、
、 ,设两种离子浓度均为
,设两种离子浓度均为 ,加入氨水调节
,加入氨水调节 后过滤除去铁元素,滤液经一系列操作可以得到
后过滤除去铁元素,滤液经一系列操作可以得到 。需调节
。需调节 的范围是
的范围是___________ 。(当离子浓度小于 认为已沉淀完全,常温下,
认为已沉淀完全,常温下, ,
, )。
)。
(5)“沉钯”过程钯元素主要发生如下转化:
 。
。
① 中
中 中
中 的键角
的键角___________ (填“<”、“>”或“=”) 中
中 的键角。
的键角。
② 晶体中含有的化学键有
晶体中含有的化学键有___________ 。
a.离子键 b.非极性共价键 c.配位键 d.氢键
(6)“还原Ⅱ”中产生无毒无害气体。由 制备海绵钯(
制备海绵钯( )的化学方程式为
)的化学方程式为___________ 。
(7)① 的晶胞俯视图如下所示:
的晶胞俯视图如下所示:

已知1个晶胞中含4个 原子,其中3个
原子,其中3个 原子的分数坐标是
原子的分数坐标是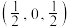 ,
,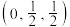 ,
, 则晶胞中
则晶胞中 的配位数为
的配位数为___________ ;某铜钯合金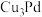 可看作上述
可看作上述 晶胞
晶胞___________ 中位置的 原子被
原子被 原子替代。
原子替代。
②有些过渡金属型氢化物能高效的储存和输送氢能源,如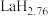 、
、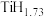 ,已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为
,已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为 ),试写出钯(
),试写出钯( )的氢化物的化学式
)的氢化物的化学式___________ 。
(8)该工艺流程中可循环利用的物质有 、
、___________ 。(填化学式)
 、
、 、
、 、活性炭,还含少量铁、铜等)中回收海绵钯(
、活性炭,还含少量铁、铜等)中回收海绵钯( )的工艺流程如图所示。
)的工艺流程如图所示。
(1)“焙烧”的目的
(2)还原I中甲酸与
 反应生成
反应生成 和
和 ,该反应中氧化剂和还原剂的物质的量之比为
,该反应中氧化剂和还原剂的物质的量之比为(3)“酸浸”过程中
 转化为
转化为 的离子方程式为
的离子方程式为
(4)“离子交换”和“洗脱”可简单表示为:
 ,(
,( 为阴离子交换树脂)。试剂
为阴离子交换树脂)。试剂 的化学式为
的化学式为 、
、 ,设两种离子浓度均为
,设两种离子浓度均为 ,加入氨水调节
,加入氨水调节 后过滤除去铁元素,滤液经一系列操作可以得到
后过滤除去铁元素,滤液经一系列操作可以得到 。需调节
。需调节 的范围是
的范围是 认为已沉淀完全,常温下,
认为已沉淀完全,常温下, ,
, )。
)。(5)“沉钯”过程钯元素主要发生如下转化:
 。
。①
 中
中 中
中 的键角
的键角 中
中 的键角。
的键角。②
 晶体中含有的化学键有
晶体中含有的化学键有a.离子键 b.非极性共价键 c.配位键 d.氢键
(6)“还原Ⅱ”中产生无毒无害气体。由
 制备海绵钯(
制备海绵钯( )的化学方程式为
)的化学方程式为(7)①
 的晶胞俯视图如下所示:
的晶胞俯视图如下所示:
已知1个晶胞中含4个
 原子,其中3个
原子,其中3个 原子的分数坐标是
原子的分数坐标是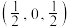 ,
,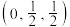 ,
, 则晶胞中
则晶胞中 的配位数为
的配位数为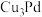 可看作上述
可看作上述 晶胞
晶胞 原子被
原子被 原子替代。
原子替代。②有些过渡金属型氢化物能高效的储存和输送氢能源,如
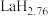 、
、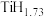 ,已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为
,已知标准状况下,1体积的钯粉大约可吸附896体积的氢气(钯粉的密度为 ),试写出钯(
),试写出钯( )的氢化物的化学式
)的氢化物的化学式(8)该工艺流程中可循环利用的物质有
 、
、
您最近一年使用:0次
9 . 向 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应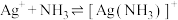 和
和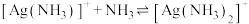 ,
, 与
与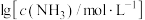 的关系如下图所示(其中
的关系如下图所示(其中 代表
代表 、
、 、
、 或
或 。
。

下列说法正确的是
 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应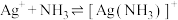 和
和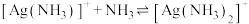 ,
, 与
与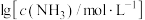 的关系如下图所示(其中
的关系如下图所示(其中 代表
代表 、
、 、
、 或
或 。
。
下列说法正确的是
A. 时, 时,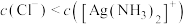 |
B. 的溶度积常数数量级为 的溶度积常数数量级为 |
C.随 的增大, 的增大, 先减小后基本不变 先减小后基本不变 |
D.向 含有 含有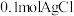 沉淀的体系中滴加氨水,消耗 沉淀的体系中滴加氨水,消耗 可将 可将 沉淀完全溶解(忽略溶液体积变化和 沉淀完全溶解(忽略溶液体积变化和 的挥发) 的挥发) |
您最近一年使用:0次
名校
10 . 关于下列实验事实的给出的解释或结论不正确的是
| 选项 | 实验事实 | 解释或结论 |
| A. |  与 与 溶液反应产生黄色沉淀和气体( 溶液反应产生黄色沉淀和气体( ) ) | 反应生成难溶的 ,增大了 ,增大了 的还原性 的还原性 |
| B. | 将 气体通入 气体通入 溶液中,溶液先变为红棕色(含 溶液中,溶液先变为红棕色(含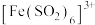 ),过一段时间又变成浅绿色 ),过一段时间又变成浅绿色 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| C. | 取一定量固体于试管中,加入浓 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 | 该固体为铵盐 |
| D. | 将变黑的银器放入装满食盐水的铝盆中,一段时间后银器恢复往日光泽 | 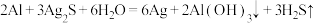 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



