名校
解题方法
1 . 铂和钯同属于铂族元素,其价格均高于黄金,在工业上有广泛的应用。电解精炼铜阳极泥中除含有较多的铂、钯和银以外,还有少量的镍、铜等元素。一种综合提取阳极泥中贵重金属的工艺流程如下:
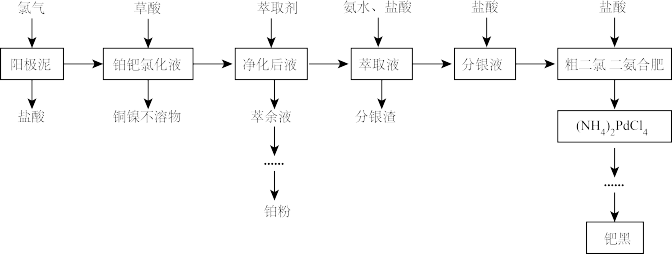
请回答以下问题。
(1)铜阳极泥中的铂和钯以游离态存在的理由是_______ 。
(2)阳极泥中的单质钯反应后转化为 请写出该反应的离子方程式
请写出该反应的离子方程式_______ 。
(3)用草酸除铜镍时,草酸用量对铜镍去除率的影响如下表1。除铜镍时的温度对去除率的影响如下表2。
表1草酸加入量对铜镍去除率的影响
表2反应温度对铜镍去除率的影响
则草酸的过量系数应为_______ 。实际工业中采用的温度为80—85℃。试分析其原因_______ 。
(4)已知 配离子存在解离平衡:
配离子存在解离平衡: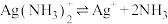 ,根据平衡移动原理说明加盐酸分银的原理
,根据平衡移动原理说明加盐酸分银的原理_______ 。
(5)分银液中加盐酸把 转化为
转化为 沉淀,过滤后用适量的盐酸溶解。则加入盐酸溶解时的化学方程式为
沉淀,过滤后用适量的盐酸溶解。则加入盐酸溶解时的化学方程式为_______ 。
(6)海绵钯具有优良的吸氢功能,其密度为 。标准状况下,吸附氢气的体积是钯体积的a倍,则此条件下海绵钯的吸附容量R=
。标准状况下,吸附氢气的体积是钯体积的a倍,则此条件下海绵钯的吸附容量R=_______  ,氢气的浓度r=
,氢气的浓度r=_______ (吸附容量R是指1g钯吸附氢气的体积;氢气的浓度r为 吸附氢气的物质的量)。
吸附氢气的物质的量)。

请回答以下问题。
(1)铜阳极泥中的铂和钯以游离态存在的理由是
(2)阳极泥中的单质钯反应后转化为
 请写出该反应的离子方程式
请写出该反应的离子方程式(3)用草酸除铜镍时,草酸用量对铜镍去除率的影响如下表1。除铜镍时的温度对去除率的影响如下表2。
表1草酸加入量对铜镍去除率的影响
| 过量系数 | 净化后液/( ) ) | 去除率/% | ||
 |  |  |  | |
| 1.0 | 16.93 | 1.47 | 68.44 | 46.15 |
| 1.5 | 4.67 | 0.61 | 91.30 | 77.66 |
| 2.0 | 0.091 | 0.031 | 99.83 | 98.86 |
| 2.5 | 0.25 | 0.042 | 99.53 | 98.46 |
| 3.0 | 0.28 | 0.040 | 99.48 | 98.53 |
| 4.0 | 0.26 | 0.035 | 99.52 | 98.72 |
| 温度 | 净化后液/( ) ) | 去除率/% | ||
 |  |  |  | |
| 70 | 0.65 | 0.130 | 98.799 | 95.24 |
| 75 | 0.26 | 0.091 | 9.52 | 96.67 |
| 80 | 0.18 | 0.043 | 99.66 | 98.42 |
| 85 | 0.15 | 0.045 | 99.72 | 98.35 |
| 90 | 0.14 | 0.042 | 99.74 | 98.46 |
| 95 | 0.14 | 0.040 | 99.74 | 98.53 |
(4)已知
 配离子存在解离平衡:
配离子存在解离平衡: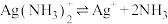 ,根据平衡移动原理说明加盐酸分银的原理
,根据平衡移动原理说明加盐酸分银的原理(5)分银液中加盐酸把
 转化为
转化为 沉淀,过滤后用适量的盐酸溶解。则加入盐酸溶解时的化学方程式为
沉淀,过滤后用适量的盐酸溶解。则加入盐酸溶解时的化学方程式为(6)海绵钯具有优良的吸氢功能,其密度为
 。标准状况下,吸附氢气的体积是钯体积的a倍,则此条件下海绵钯的吸附容量R=
。标准状况下,吸附氢气的体积是钯体积的a倍,则此条件下海绵钯的吸附容量R= ,氢气的浓度r=
,氢气的浓度r= 吸附氢气的物质的量)。
吸附氢气的物质的量)。
您最近一年使用:0次
2022-03-31更新
|
458次组卷
|
5卷引用:湖南省湘潭市第一中学2023届高三第六次月考化学试题
湖南省湘潭市第一中学2023届高三第六次月考化学试题河南省郑州市2022届高三第二次质量预测理科综合化学试题(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学-2022年高考押题预测卷02(山东卷)(已下线)押江苏卷第15题 化学工业流程综合题 -备战2022年高考化学临考题号押题(江苏卷)
解题方法
2 . 硫酸镍广泛应用于电镀工业。以粗硫酸镍(含 、
、 、
、 、
、 、
、 等)为原料,经如图1一系列除杂过程模拟精制硫酸镍工艺。回答下列问题。
等)为原料,经如图1一系列除杂过程模拟精制硫酸镍工艺。回答下列问题。

(1)为了加快溶解速率,可采取的措施是___________ 。(任答两点)
(2)写出“硫化除铜”过程生成含铜物质反应的离子方程式___________ 。
(3)“氧化除杂”时加入 主要作用是
主要作用是___________ 。
(4)已知25℃时, ;
;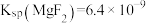 。则“氟化除杂”过后滤液3中
。则“氟化除杂”过后滤液3中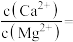
___________ 。
(5)“萃取”时使用萃取剂R在硫酸盐中对某些金属离子的萃取率与溶液pH的关系如图2,则实验时需控制的pH适宜范围是___________(填字母)。

(6)利用精制的硫酸镍用如图装置可实现在铜片上镀镍。

铜片在乙装置的___________ 处(填“c”或“d”),b极上发生的电极反应式为___________ 。
 、
、 、
、 、
、 、
、 等)为原料,经如图1一系列除杂过程模拟精制硫酸镍工艺。回答下列问题。
等)为原料,经如图1一系列除杂过程模拟精制硫酸镍工艺。回答下列问题。
(1)为了加快溶解速率,可采取的措施是
(2)写出“硫化除铜”过程生成含铜物质反应的离子方程式
(3)“氧化除杂”时加入
 主要作用是
主要作用是(4)已知25℃时,
 ;
;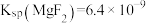 。则“氟化除杂”过后滤液3中
。则“氟化除杂”过后滤液3中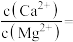
(5)“萃取”时使用萃取剂R在硫酸盐中对某些金属离子的萃取率与溶液pH的关系如图2,则实验时需控制的pH适宜范围是___________(填字母)。

| A.1~2 | B.2~3 | C.4~5 | D.5~6 |

铜片在乙装置的
您最近一年使用:0次
名校
解题方法
3 . 以黄铁矿(主要成分是FeS2,含少量SiO2)和软锰矿(主要成分是MnO2,含少量Fe2O3、Al2O3)为原料制备MnSO4·H2O的工艺流程如下。回答下列问题:

已知溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
如下表所示:
(1)混合研磨成细粉的目的是_______ 。“酸浸”过程得到的滤液中含有 ,则该过程中主要反应的离子方程式是
,则该过程中主要反应的离子方程式是_______ 。
(2)根据上表数据,计算 的
的
_______ 。若“调 ”后的溶液中
”后的溶液中 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是_______ 。
(3)“沉锰”时, 参与反应的离子方程式是
参与反应的离子方程式是_______ 。
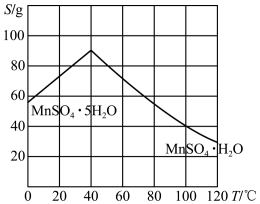
(4)结合图象,分析从“操作A”所得溶液中得到 晶体需进行的操作是
晶体需进行的操作是_______ 、洗涤、干燥.若称取一定质量的 用标准
用标准 溶液滴定(操作过程产生的误差很小可忽略),计算所得样品质量分数大于
溶液滴定(操作过程产生的误差很小可忽略),计算所得样品质量分数大于 ,分析可能的原因是
,分析可能的原因是_______ 。

已知溶液中金属离子开始沉淀和完全沉淀的
 如下表所示:
如下表所示:| 金属离子 |  |  |  |  |
开始沉淀时 的 的 | 8.1 | 7.5 | 2.2 | 3.7 |
沉淀完全时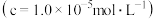 的 的 | 9.6 | 9.0 | 3.2 | 4.7 |
 ,则该过程中主要反应的离子方程式是
,则该过程中主要反应的离子方程式是(2)根据上表数据,计算
 的
的
 ”后的溶液中
”后的溶液中 浓度为
浓度为 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(3)“沉锰”时,
 参与反应的离子方程式是
参与反应的离子方程式是(4)结合图象,分析从“操作A”所得溶液中得到
 晶体需进行的操作是
晶体需进行的操作是 用标准
用标准 溶液滴定(操作过程产生的误差很小可忽略),计算所得样品质量分数大于
溶液滴定(操作过程产生的误差很小可忽略),计算所得样品质量分数大于 ,分析可能的原因是
,分析可能的原因是
您最近一年使用:0次
2022-01-17更新
|
840次组卷
|
6卷引用:湖南省湘潭市第一中学2022届2021-2022学年高三下学期月考化学试题
湖南省湘潭市第一中学2022届2021-2022学年高三下学期月考化学试题山东省烟台市2021-2022学年高三上学期期末考试化学试题(已下线)专题27 无机化工流程-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)一轮巩固卷3-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(广东专用)河北省五个一名校联盟2023届高三年级模拟底考试化学试题江西省重点校2022-2023学年高三上学期第二次联考化学试题.
名校
4 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 一段时间后,取铁电极区少量溶液于试管中,滴加铁氰化钾溶液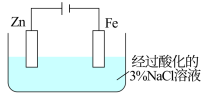 | 未出现特征蓝色的沉淀 | 锌、铁与酸化的氯化钠溶液构成原电池后,锌能够有效保护铁制品 |
| B | 向2支盛有5 mL0.1 mol·L-1H2SO4溶液的试管中分别加入5mL0.1 mol·L-1 Na2S2O3溶液,分别放入20 °C,40 °C的水浴中,并开始计时 | 40°C下出现浑浊的时间短 | 温度越高反应速率越快 |
| C | 向10 ml. 0.2 mol·L-1 NaOH 溶液中滴加2滴0.1 mol· L-1 MgCl2溶液,产生白 色沉淀后,再滴加2滴0.1 mol·L-1FeCl3溶液 | 生成红褐色沉淀 | 证明在相同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| D | 在相同条件下,用pH计分别测定0.1 mol·L-1FeCl3溶液和0.01 mol·L-1FeCl3溶液的pH | 0.1 mol·L-1FeCl3溶液的pH为1.16,0.01 mol·L-1 FeCl3溶液的pH为1.76 | 增大c(FeCl3),抑制FeCl3水解,也说明加水稀释后水解平衡右移,促进FeCl3水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-15更新
|
160次组卷
|
2卷引用:湖南省湘潭市湘乡市第一中学2021-2022学年高三下学期4月月考化学试题
解题方法
5 . 如图为从预处理后的可充电电池粉末(主要为NiO、CdO、CoO和Fe2O3等)中回收重金属的工艺流程。

回答下列问题:
(1)“浸取”过程先加入NH4HCO3溶液,再通入NH3,滤液①中主要含[Cd(NH3)4]2+、[Ni(NH3)6]2+、[Co(NH3)6]2+及CO 。写出NiO浸取时发生反应的化学方程式:
。写出NiO浸取时发生反应的化学方程式:___ 。
(2)探究“催化氧化”步骤中[Co(NH3)6]2+氧化为[Co(NH3)6]3+的实验条件,向[Co(NH3)6]2+含量为0.48g·L-1的溶液中通入空气,待反应完全后,记录[Co(NH3)6]3+浓度数据如表:
由表中数据可得,[Co(NH3)6]2+氧化的最佳条件为___ 。
(3)已知Co(OH)3为强氧化剂,向Co(OH)3中加入浓盐酸发生“反应Ⅰ”,写出该反应的离子方程式:___ 。
(4)“反萃取”的原理为NiR有机+2H+ Ni2++2HR有机,需加入的试剂X为
Ni2++2HR有机,需加入的试剂X为___ ,分离有机相和水相的操作的名称为___ 。
(5)“水相①”的主要溶质为___ (填化学式)。
(6)生成CdCO3沉淀是利用反应[Cd(NH3)4]2++CO
 CdCO3↓+4NH3↑,常温下,该反应平衡常数K=2.0×105,[Cd(NH3)4]2+
CdCO3↓+4NH3↑,常温下,该反应平衡常数K=2.0×105,[Cd(NH3)4]2+ Cd2++4NH3的平衡常数K1= 4.0×10—5,则Ksp(CdCO3)=
Cd2++4NH3的平衡常数K1= 4.0×10—5,则Ksp(CdCO3)=___ 。

回答下列问题:
(1)“浸取”过程先加入NH4HCO3溶液,再通入NH3,滤液①中主要含[Cd(NH3)4]2+、[Ni(NH3)6]2+、[Co(NH3)6]2+及CO
 。写出NiO浸取时发生反应的化学方程式:
。写出NiO浸取时发生反应的化学方程式:(2)探究“催化氧化”步骤中[Co(NH3)6]2+氧化为[Co(NH3)6]3+的实验条件,向[Co(NH3)6]2+含量为0.48g·L-1的溶液中通入空气,待反应完全后,记录[Co(NH3)6]3+浓度数据如表:
| 反应时间 | [Co(NH3)6]3+/g·L-1 | |
| 25℃ | 50℃,石墨催化 | |
| 1.5h | 0.090 | 0.15 |
| 2.5h | 0.14 | 0.48 |
| 5h | 0.25 | 0.48 |
(3)已知Co(OH)3为强氧化剂,向Co(OH)3中加入浓盐酸发生“反应Ⅰ”,写出该反应的离子方程式:
(4)“反萃取”的原理为NiR有机+2H+
 Ni2++2HR有机,需加入的试剂X为
Ni2++2HR有机,需加入的试剂X为(5)“水相①”的主要溶质为
(6)生成CdCO3沉淀是利用反应[Cd(NH3)4]2++CO

 CdCO3↓+4NH3↑,常温下,该反应平衡常数K=2.0×105,[Cd(NH3)4]2+
CdCO3↓+4NH3↑,常温下,该反应平衡常数K=2.0×105,[Cd(NH3)4]2+ Cd2++4NH3的平衡常数K1= 4.0×10—5,则Ksp(CdCO3)=
Cd2++4NH3的平衡常数K1= 4.0×10—5,则Ksp(CdCO3)=
您最近一年使用:0次
6 . 以镁铝复合氧化物(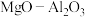 )为载体的负载型镍铜双金属催化剂(
)为载体的负载型镍铜双金属催化剂( )是一种新型高效加氢或脱氢催化剂,其制备流程如下:
)是一种新型高效加氢或脱氢催化剂,其制备流程如下:
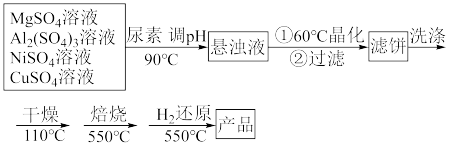
已知:常温下,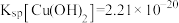 ,
,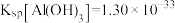 。回答下列问题:
。回答下列问题:
(1)在加热条件下,尿素 在水中发生水解反应,放出
在水中发生水解反应,放出______ 和______ 两种气体(写化学式)。
(2)“晶化”过程中,需保持恒温60℃,可采用的加热方式为______ 。
(3)“洗涤”过程中,检验滤饼是否洗净的方法是______ 。
(4)常温下,若“悬浊液”中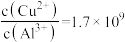 ,则溶液的
,则溶液的
______ 。
(5)“还原”过程中所发生反应的化学方程式为______ 。
(6) 在强碱溶液中被
在强碱溶液中被 氧化可得
氧化可得 ,该物质能用作碱性镍镉电池的正极材料。其电池反应式:
,该物质能用作碱性镍镉电池的正极材料。其电池反应式: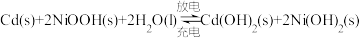
①放电一段时间后,溶液的pH将______ (填“增大”“减小”或“不变”)。
②充电时,阳极发生的电极反应式为______ 。
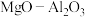 )为载体的负载型镍铜双金属催化剂(
)为载体的负载型镍铜双金属催化剂( )是一种新型高效加氢或脱氢催化剂,其制备流程如下:
)是一种新型高效加氢或脱氢催化剂,其制备流程如下:
已知:常温下,
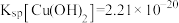 ,
,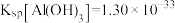 。回答下列问题:
。回答下列问题:(1)在加热条件下,尿素
 在水中发生水解反应,放出
在水中发生水解反应,放出(2)“晶化”过程中,需保持恒温60℃,可采用的加热方式为
(3)“洗涤”过程中,检验滤饼是否洗净的方法是
(4)常温下,若“悬浊液”中
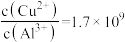 ,则溶液的
,则溶液的
(5)“还原”过程中所发生反应的化学方程式为
(6)
 在强碱溶液中被
在强碱溶液中被 氧化可得
氧化可得 ,该物质能用作碱性镍镉电池的正极材料。其电池反应式:
,该物质能用作碱性镍镉电池的正极材料。其电池反应式: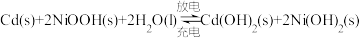
①放电一段时间后,溶液的pH将
②充电时,阳极发生的电极反应式为
您最近一年使用:0次
2021-01-25更新
|
2272次组卷
|
7卷引用:湖南省湘潭市第二中学2022届高三下学期4月月考化学试题
湖南省湘潭市第二中学2022届高三下学期4月月考化学试题湖南省2021年普通高中学业水平选择考适应性测试化学试题(已下线)2021年高考化学押题预测卷(新课标Ⅲ卷)(03)(含考试版、答题卡、参考答案、全解全析)广东省广州市华南师范大学附属中学2021届高三下学期三模化学试题(已下线)专题15 工艺流程综合题-2022年高考化学二轮复习重点专题常考点突破练广东省广州市华南师范大学附属中学2022届高三上学期综合测试(一)化学试题(已下线)微专题 无机化工流程题的解题策略
名校
解题方法
7 . 实验室以电镀废渣(Cr2O3、CuO、Fe2O3及CaO)为原料制取铜粉和K2Cr2O7的主要流程如图:

(1)“酸浸”时,所得残渣的主要成分是___________ 。
(2)“沉 CuS”时,加入的硫化钠必须适量,若过量可能产生的后果是_________ (用离子方程式表示)。
(3)一水合硫酸四氨合铜加热到650℃可分解为铜、氨气、二氧化硫和水以及一种无污染气体,写出其化学方程式___________ 。
(4)“沉CuNH4 SO3”时可用如图装置(夹持、加热仪器略):
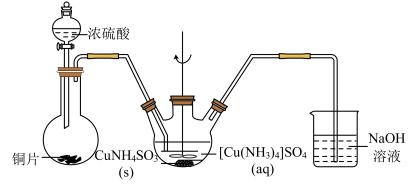
①“沉CuNH4SO3”时,反应液需控制在45℃,合适的加热方式是____________ 。
②NaOH溶液的作用是___________ 。
(5)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.0g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000mol·L–1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O72-被还原为Cr3+)
①若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL,则所得产品K2Cr2O7的纯度为_____ %。[已知M(K2Cr2O7)=294g·mol-1,计算结果保留至小数点后两位]。
②上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的 Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=2×10–5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?____________ (通过计算说明原因)。{已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31}

(1)“酸浸”时,所得残渣的主要成分是
(2)“沉 CuS”时,加入的硫化钠必须适量,若过量可能产生的后果是
(3)一水合硫酸四氨合铜加热到650℃可分解为铜、氨气、二氧化硫和水以及一种无污染气体,写出其化学方程式
(4)“沉CuNH4 SO3”时可用如图装置(夹持、加热仪器略):

①“沉CuNH4SO3”时,反应液需控制在45℃,合适的加热方式是
②NaOH溶液的作用是
(5)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.0g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000mol·L–1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O72-被还原为Cr3+)
①若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL,则所得产品K2Cr2O7的纯度为
②上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的 Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=2×10–5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?
您最近一年使用:0次
解题方法
8 . 镁合金及镁的化合物在生产、生活中有着广泛的应用。
(1)镁在元素周期表中的位置是__________________ 。
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

该工艺中可循环使用的物质有______________ 。
(3)储氢材料Mg(AlH4)2在110~200 ℃的反应为Mg(AlH4)2=MgH2+2Al+3H2↑,每转移6 mol电子生成氢气的物质的量为________ mol。
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000 g产品用适量硝酸溶解,经稀释等步骤最终配得500 mL的溶液。
a.准确量取25.00 mL 待测液,用0.100 0 mol/L AgNO3标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为________ mL。

b.
参照上表数据及信息分析,滴定时可以作指示剂的是________ (填数字序号)。
①CaCl2 ②NaBr ③NaI ④K2CrO4
(1)镁在元素周期表中的位置是
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

该工艺中可循环使用的物质有
(3)储氢材料Mg(AlH4)2在110~200 ℃的反应为Mg(AlH4)2=MgH2+2Al+3H2↑,每转移6 mol电子生成氢气的物质的量为
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.1000 g产品用适量硝酸溶解,经稀释等步骤最终配得500 mL的溶液。
a.准确量取25.00 mL 待测液,用0.100 0 mol/L AgNO3标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为

b.
| AgCl | AgBr | AgI | Ag2CrO4 | |
| Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白 | 淡黄 | 黄 | 砖红 |
①CaCl2 ②NaBr ③NaI ④K2CrO4
您最近一年使用:0次
9 . 下列实验能达到预期目的的是( )
| 实验内容 | 实验目的 | |
| A | 测同温同浓度下的Na2CO3和Na2SO3水溶液的pH | 确定碳和硫两元素非金属性强弱 |
| B | 向1ml 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,又生成红褐色沉淀 | 可以证明在相同温度下,溶解度Mg(OH)2>Fe(OH)3 |
| C | 将NaOH溶液滴入该溶液中加热,放出的气体能使湿润的红色石蕊试纸变蓝 | 证明溶液中有NH4+ |
| D | 用稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 证明氧化性:H2O2比Fe3+强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
真题
名校
10 . 在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是
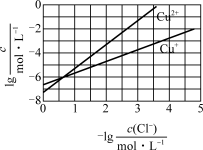

| A.Ksp(CuCl)的数量级为10-7 |
| B.除Cl-反应为Cu+Cu2++2Cl-=2CuCl |
| C.加入Cu越多,Cu+浓度越高,除Cl-效果越好 |
| D.2Cu+=Cu2++Cu平衡常数很大,反应趋于完全 |
您最近一年使用:0次
2017-08-08更新
|
11744次组卷
|
38卷引用:2020届湖南省湘潭市高三教学质量监测卷化学试题
2020届湖南省湘潭市高三教学质量监测卷化学试题河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅲ卷精编版)湖南省怀化市2018届高三上学期期末教育质量监测化学试题江西省等三省十校2018届高三下学期联考理综化学试题(已下线)《考前20天终极攻略》-5月23日 溶液中的离子平衡(已下线)解密13 沉淀溶解平衡——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】湖南省怀化市2018届高三上学期期末统一考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期期末考试化学试题【全国百强校】河南省信阳市第一高级中学2019届高三上学期期末考试化学试题四川省宜宾市叙州区第一中学2020届高三上学期第一次月考理综化学试题云南省玉溪市江川二中2019-2020学年高三上学期期中考试化学试题(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》2020届人教版高三化学二轮专题巩固练习:水溶液中的离子平衡【懂做原理题】2020届高三化学选修4二轮专题练——沉淀溶解平衡的曲线分析【精编23题】贵州省镇远县二中2019-2020学年高三上学期期末考试化学试题贵州省岑巩县第二中学2019-2020学年高三上学期期末考试化学试题(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡(已下线)福建省泉州市泉港区第一中学2018-2019学年高二年级下学期期中考化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过高考 3年真题强化闯关(已下线)小题必刷34 沉淀溶解平衡、溶度积常数及其应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)练习12 难溶电解质的溶解平衡-2020-2021学年【补习教材·寒假作业】高二化学(人教版)甘肃省白银市第十中学2019-2020学年高二上学期期中考试化学试题(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)河北正定中学2020-2021学年高三上学期第四次半月考化学试题(已下线)考向27 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点微专题(已下线)第5讲 沉淀溶解平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)四川省凉山宁南中学2019-2020学年高二下学期第一次月考化学试题云南省富宁县第一中学校2021-2022学年高三下学期开学考试理综化学试题(已下线)题型28 沉淀溶解平衡常数及其应用图像(已下线)第6讲 沉淀溶解平衡图像分析



