名校
1 . 常温下,用HCl(g)调节SrF2浊液的pH,测得在通入HCl(g)的过程中,体系中-lgc(X)(X代表Sr2+或F-)与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是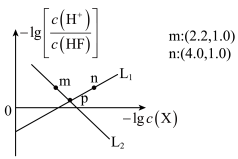
A.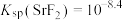 |
B.L2表示 的变化情况 的变化情况 |
| C.随着HCl的加入,SrF2溶解度逐渐增大 |
D.m、n点对应的溶液中均存在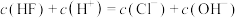 |
您最近一年使用:0次
2024-04-15更新
|
387次组卷
|
3卷引用:湖南省资兴市立中等多校联考2023-2024学年高二下学期3月月考化学试题
名校
解题方法
2 . 以废铁屑、低品位软锰矿[主要成分有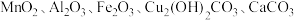 、
、 等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
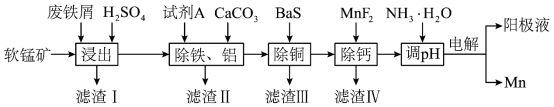
已知:I.部分金属阳离子以氢氧化物沉淀时的 如表:
如表:
Ⅱ.几种化合物的溶解性或溶度积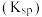 如表:
如表:
(1)基态 的价层电子排布式为
的价层电子排布式为__________ 。
(2)为去除废铁屑表面的油污可采用的方法为__________ ;“浸出”后浸出液中的 价金属阳离子有
价金属阳离子有 、
、__________ 。
(3)锰的浸出率结果如图所示。

由图可知,影响锰浸出率的因素有__________ 。
(4)“除铁、铝”过程中,浸出液需要先用试剂 处理,然后加入
处理,然后加入 ,反应后溶液的
,反应后溶液的 。试剂
。试剂 的作用是
的作用是__________ 。
(5)“除铜”过程中,当铜离子恰好完全沉淀(当离子浓度小于或等于 时视为完全沉淀)时,溶液中
时视为完全沉淀)时,溶液中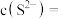
__________  。
。
(6)用惰性电极电解中性 溶液可以制得金属
溶液可以制得金属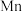 。装置如图所示。
。装置如图所示。
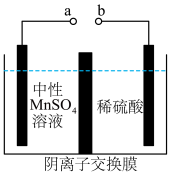
若生成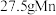 ,右室溶液中最终
,右室溶液中最终 的变化为
的变化为__________ (填“增加”或“减少”) 。
。
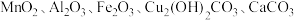 、
、 等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
等]为原料,制备硫酸锰,进一步电解制备金属锰,工艺流程如图所示:
已知:I.部分金属阳离子以氢氧化物沉淀时的
 如表:
如表:| 金属阳离子 |  |  |  |  |  |
开始沉淀的 | 6.8 | 1.8 | 3.7 | 8.6 | 5.2 |
沉淀完全的 | 8.3 | 2.8 | 4.7 | 10.1 | 6.7 |
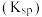 如表:
如表:| 化合物 |  |  |  |  |  |
溶解性或溶度积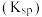 | 溶于水 | 溶于水 | 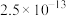 |  |  |
(1)基态
 的价层电子排布式为
的价层电子排布式为(2)为去除废铁屑表面的油污可采用的方法为
 价金属阳离子有
价金属阳离子有 、
、(3)锰的浸出率结果如图所示。

由图可知,影响锰浸出率的因素有
(4)“除铁、铝”过程中,浸出液需要先用试剂
 处理,然后加入
处理,然后加入 ,反应后溶液的
,反应后溶液的 。试剂
。试剂 的作用是
的作用是(5)“除铜”过程中,当铜离子恰好完全沉淀(当离子浓度小于或等于
 时视为完全沉淀)时,溶液中
时视为完全沉淀)时,溶液中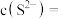
 。
。(6)用惰性电极电解中性
 溶液可以制得金属
溶液可以制得金属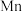 。装置如图所示。
。装置如图所示。
若生成
 ,右室溶液中最终
,右室溶液中最终 的变化为
的变化为 。
。
您最近一年使用:0次
3 . 从某废液(含有Fe3+、Fe2+、Cu2+、Cl-)中回收铜并制得纯净的FeCl3溶液。现以制得的纯净的FeCl3溶液为原料制取优良的水处理剂高铁酸钾(K2FeO4),其流程如图:
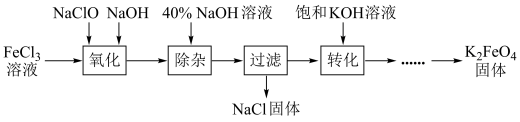
已知:高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定;具有强氧化性;与水作用产生Fe(OH)3。
(1)高铁酸钾(K2FeO4)在处理水过程中的作用是_________ 和_________ 。
(2)检验废液中含有Fe2+选用的试剂是__________ (填化学式)。
(3)“氧化”过程反应的离子方程式为__________ 。
(4)上述工艺得到的高铁酸钾常含有杂质,可用重结晶法提纯,操作是将粗产品用______ 溶解,然后______ ,过滤。
(5)用回收的铜为原料可制得粗CuSO4·5H2O晶体(含有少量的FeSO4·7H2O),除去CuSO4·5H2O晶体中杂质的方法是将该晶体溶于水,向溶液中加入H2O2,再调节溶液pH。过滤即可制得纯净的CuSO4溶液,进而可制得纯净的CuSO4·5H2O晶体。
已知:室温时一些物质的Ksp如表所示:
已知溶液中的某离子浓度小于1×10-5 mol/L时就认为该离子沉淀完全。加双氧水的目的是_________ ;若溶液中CuSO4的浓度为3.0mol/L,通过计算说明此方法可除去粗CuSO4·5H2O晶体中FeSO4·7H2O的理由:___________ 。

已知:高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定;具有强氧化性;与水作用产生Fe(OH)3。
(1)高铁酸钾(K2FeO4)在处理水过程中的作用是
(2)检验废液中含有Fe2+选用的试剂是
(3)“氧化”过程反应的离子方程式为
(4)上述工艺得到的高铁酸钾常含有杂质,可用重结晶法提纯,操作是将粗产品用
(5)用回收的铜为原料可制得粗CuSO4·5H2O晶体(含有少量的FeSO4·7H2O),除去CuSO4·5H2O晶体中杂质的方法是将该晶体溶于水,向溶液中加入H2O2,再调节溶液pH。过滤即可制得纯净的CuSO4溶液,进而可制得纯净的CuSO4·5H2O晶体。
已知:室温时一些物质的Ksp如表所示:
| 化学式 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
| Ksp | 8.0×10-16 | 8.0×10-38 | 3×10-20 |
您最近一年使用:0次
解题方法
4 . 亚硝酰氯(NOCl)为红褐色液体或黄色气体,其熔点为-64.5℃,沸点为-5.5℃,具有刺鼻恶臭味,遇水剧烈水解,易溶于浓硫酸。常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温、常压下合成。其制备装置如图所示。

(1)①用图甲中装置制备纯净干燥的原料气,试写出该装置制备氯气的离子方程式:_______ 。
②其中导管A的作用是_______ 。
(2)将制得的NO和Cl2通入图乙对应装置制备NOCl。
①装置连接顺序为a→_______ (按气流自左向右方向,用小写字母表示)。
②装置Ⅶ装无水CaCl2的仪器名称是_______ 。
③装置Ⅳ、Ⅴ的相同作用是(写两点)________ 、________ 。
(3)实验开始时,先通入氯气,再通入NO,原因是________ 。
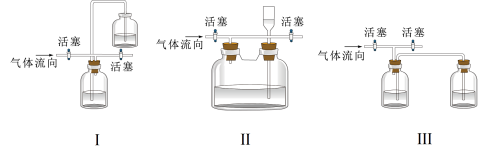
(4)有同学认为多余的氯气可以通过下列装置暂时储存然后再利用,下列可以用作氯气的储气装置的是________ (填序号)。
(5)制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:称取8.600g样品溶于NaOH配制成500.00mL溶液,用移液管取25.00mL溶液,加入几滴K2CrO4溶液作指示剂,用足量硝酸酸化的0.020mol/LAgNO3溶液进行滴定,消耗AgNO3溶液25.00mL。
已知:AgCl为白色沉淀溶解度1.34×10-6mol/L,Ksp(AgCl)=1.8×10-10;Ag2CrO4为砖红色沉淀溶解度6.5×10-5mol/L,Ksp(Ag2CrO4)=1.2×10-12。
①滴定终点的现象是________ 。
②样品的纯度为________ %(保留1位小数)。

(1)①用图甲中装置制备纯净干燥的原料气,试写出该装置制备氯气的离子方程式:
②其中导管A的作用是
(2)将制得的NO和Cl2通入图乙对应装置制备NOCl。
①装置连接顺序为a→
②装置Ⅶ装无水CaCl2的仪器名称是
③装置Ⅳ、Ⅴ的相同作用是(写两点)
(3)实验开始时,先通入氯气,再通入NO,原因是
(4)有同学认为多余的氯气可以通过下列装置暂时储存然后再利用,下列可以用作氯气的储气装置的是

(5)制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:称取8.600g样品溶于NaOH配制成500.00mL溶液,用移液管取25.00mL溶液,加入几滴K2CrO4溶液作指示剂,用足量硝酸酸化的0.020mol/LAgNO3溶液进行滴定,消耗AgNO3溶液25.00mL。
已知:AgCl为白色沉淀溶解度1.34×10-6mol/L,Ksp(AgCl)=1.8×10-10;Ag2CrO4为砖红色沉淀溶解度6.5×10-5mol/L,Ksp(Ag2CrO4)=1.2×10-12。
①滴定终点的现象是
②样品的纯度为
您最近一年使用:0次
解题方法
5 . 工业上用硫化镍矿(主要成分为NiS,含有ZnS、CuS、FeS等杂质)制备 的工艺流程如下:
的工艺流程如下:
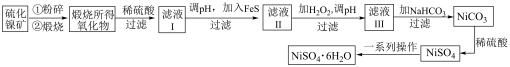
(1)将硫化镍矿粉碎的目的是___________ ,煅烧NiS生成NiO和 的化学方程式为
的化学方程式为___________ 。
(2)向滤液Ⅰ中加入FeS是为了生成难溶于水的硫化物沉淀而除去 、
、 等杂质,则除去
等杂质,则除去 的离子方程式为
的离子方程式为 ,该反应的化学平衡常数为
,该反应的化学平衡常数为___________ (已知 ,
, ,
, )。
)。
(3)往滤液Ⅲ中加入 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(4)滤液Ⅲ中溶质的主要成分是 ,加
,加 过滤后得到
过滤后得到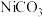 沉淀,再加适量稀硫酸溶解又生成
沉淀,再加适量稀硫酸溶解又生成 ,这两步操作的目的是
,这两步操作的目的是___________ 。
(5)用惰性电极电解 溶液时,在
溶液时,在___________ 极得到单质镍,另一电极的电极反应式为:___________ 。
 的工艺流程如下:
的工艺流程如下:
(1)将硫化镍矿粉碎的目的是
 的化学方程式为
的化学方程式为(2)向滤液Ⅰ中加入FeS是为了生成难溶于水的硫化物沉淀而除去
 、
、 等杂质,则除去
等杂质,则除去 的离子方程式为
的离子方程式为 ,该反应的化学平衡常数为
,该反应的化学平衡常数为 ,
, ,
, )。
)。(3)往滤液Ⅲ中加入
 溶液反应的离子方程式为
溶液反应的离子方程式为(4)滤液Ⅲ中溶质的主要成分是
 ,加
,加 过滤后得到
过滤后得到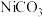 沉淀,再加适量稀硫酸溶解又生成
沉淀,再加适量稀硫酸溶解又生成 ,这两步操作的目的是
,这两步操作的目的是(5)用惰性电极电解
 溶液时,在
溶液时,在
您最近一年使用:0次
6 . 下列实验目的对应的方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 检验溶液中是否含钠元素 | 将蘸取溶液的玻璃棒放在无色火焰上灼烧 | 火焰出现黄色,说明溶液中含钠元素 |
| B | 在 时,比较 时,比较 与 与 结合 结合 能力强弱 能力强弱 | 向 溶液中,先加NaOH溶液调节 溶液中,先加NaOH溶液调节 ,再加入足量的KSCN溶液 ,再加入足量的KSCN溶液 | 红褐色沉淀不溶解,说明在 时, 时, 结合 结合 的能力更强 的能力更强 |
| C | 比较T℃时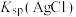 与 与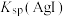 的大小 的大小 | T℃时,向等体积的饱和AgCl、AgI溶液中分别滴加足量 溶液 溶液 | 所得沉淀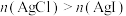 ,则 ,则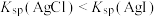 |
| D | 比较亚硫酸与碳酸的酸性强弱 | 分别测定 、 、 饱和溶液的pH 饱和溶液的pH | 前者小,说明亚硫酸酸性更强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 电镀污泥是电镀废水处理过程中产生的固体废弃物,其中含有大量的金属,如铜、镍、铬等,是一种廉价的二次可再生资源.以某厂的电镀污泥(除水干化后的成分如表所示)为原料回收铜和镍的工艺路线如图所示:
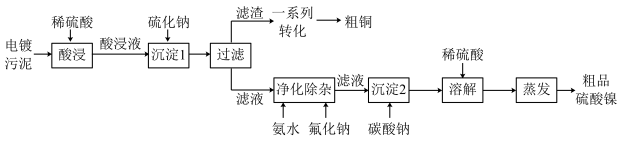
回答下列问题:
(1)若污泥中Cr元素以 ,的形式存在,则“酸浸”时
,的形式存在,则“酸浸”时 发生反应的化学方程式为
发生反应的化学方程式为______ 。
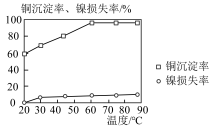
(2)“沉淀1”时,当硫化钠的加入量为理论需求量的1.2倍、沉淀时间为30min时,温度对铜沉淀率和镍损失率的影响如图所示,则“沉淀1”温度应控制为______ 。
(3)溶液中金属离子开始沉淀、沉淀完全时的pH如表所示:
“净化除杂”时,向滤液中加氨水前通常需要加入适量的双氧水,目的是______ 。为保证除杂效果,加入氨水调节溶液的pH,需要控制pH的范围为______ 。
(4)已知常温下 和
和 的溶度积常数分别为
的溶度积常数分别为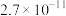 、
、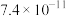 ,若添加氟化钠后溶液中
,若添加氟化钠后溶液中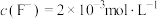 ,此时
,此时 和
和 是否除尽?
是否除尽?______ 。
(5)向“净化除杂”后的滤液中加入碳酸钠溶液,生成碱式碳酸镍[化学式为 ]沉淀,该过程中无气体生成,反应的离子方程式为
]沉淀,该过程中无气体生成,反应的离子方程式为______ 。
(6)取20.00g干化电镀污泥,进行回收处理得到粗品铜,最终转化为1.638g纯铜,则铜的回收率为______ 。
| 组成 | Cu | Ni | Cr | Al | Fe | Ca | Mg | 其他 |
| 质量分数/% | 9.10 | 8.60 | 3.04 | 2.31 | 0.76 | 5.62 | 1.34 | 69.23 |

回答下列问题:
(1)若污泥中Cr元素以
 ,的形式存在,则“酸浸”时
,的形式存在,则“酸浸”时 发生反应的化学方程式为
发生反应的化学方程式为(2)“沉淀1”时,当硫化钠的加入量为理论需求量的1.2倍、沉淀时间为30min时,温度对铜沉淀率和镍损失率的影响如图所示,则“沉淀1”温度应控制为

(3)溶液中金属离子开始沉淀、沉淀完全时的pH如表所示:
| 金属离子 |  |  |  |  |  |
| 开始沉淀时的pH | 7.2 | 4.9 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 8.7 | 6.8 | 4.7 | 3.2 | 9.0 |
(4)已知常温下
 和
和 的溶度积常数分别为
的溶度积常数分别为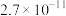 、
、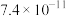 ,若添加氟化钠后溶液中
,若添加氟化钠后溶液中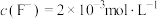 ,此时
,此时 和
和 是否除尽?
是否除尽?(5)向“净化除杂”后的滤液中加入碳酸钠溶液,生成碱式碳酸镍[化学式为
 ]沉淀,该过程中无气体生成,反应的离子方程式为
]沉淀,该过程中无气体生成,反应的离子方程式为(6)取20.00g干化电镀污泥,进行回收处理得到粗品铜,最终转化为1.638g纯铜,则铜的回收率为
您最近一年使用:0次
2023-05-27更新
|
246次组卷
|
2卷引用:湖南省郴州市九校联盟2023届高三适应考试化学试卷题
解题方法
8 . 铋(Bi)的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含
,含 、CuO、
、CuO、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
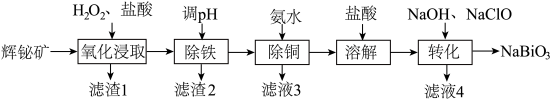
已知:
i. 易水解。
易水解。 难溶于冷水。
难溶于冷水。
ii.“氧化浸取”时,铋元素转化为 ,硫元素转化为硫单质。
,硫元素转化为硫单质。
iii.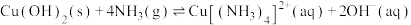
 。
。
回答下列问题:
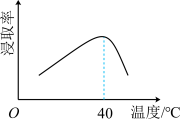
(1)为提高“浸取”速率,采取的措施有:升高温度、___________ (写出一条)。辉铋矿浸取率随温度的变化曲线如图,高于40℃时浸取率快速下降,其可能的原因是___________ 。
(2)“氧化浸取”时, 和
和 发生反应的物质的量之比为
发生反应的物质的量之比为___________ 。
(3)“除铜”时发生反应: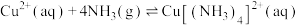
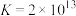 ,则
,则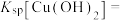
___________ 。
(4)“转化”时,生成 的离子方程式为
的离子方程式为___________ 。
(5)已知酸性环境下, 可以将
可以将 氧化成
氧化成 (
( 被还原成
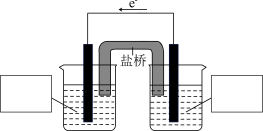
被还原成 )。请设计一个原电池装置来证明这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式
)。请设计一个原电池装置来证明这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式___________ ,并写出正极的电极反应式:___________ 。
(6)取 产品w g,加入足量稀硫酸和
产品w g,加入足量稀硫酸和 稀溶液使其完全反应,再用a mol·L
稀溶液使其完全反应,再用a mol·L
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
,当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为___________ (用含w、a、b的代数式表示)。
 ,含
,含 、CuO、
、CuO、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
已知:
i.
 易水解。
易水解。 难溶于冷水。
难溶于冷水。ii.“氧化浸取”时,铋元素转化为
 ,硫元素转化为硫单质。
,硫元素转化为硫单质。iii.
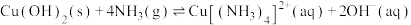
 。
。回答下列问题:
(1)为提高“浸取”速率,采取的措施有:升高温度、

(2)“氧化浸取”时,
 和
和 发生反应的物质的量之比为
发生反应的物质的量之比为(3)“除铜”时发生反应:
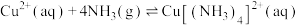
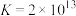 ,则
,则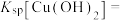
(4)“转化”时,生成
 的离子方程式为
的离子方程式为(5)已知酸性环境下,
 可以将
可以将 氧化成
氧化成 (
( 被还原成
被还原成 )。请设计一个原电池装置来证明这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式
)。请设计一个原电池装置来证明这一点,在下图中的两个方框内标出两烧杯溶液中溶质的化学式
(6)取
 产品w g,加入足量稀硫酸和
产品w g,加入足量稀硫酸和 稀溶液使其完全反应,再用a mol·L
稀溶液使其完全反应,再用a mol·L
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
,当溶液紫红色恰好褪去时,消耗b mL标准溶液。该产品的纯度为
您最近一年使用:0次
解题方法
9 . 次磷酸钠( )广泛应用于化学镀镍,在生产
)广泛应用于化学镀镍,在生产 的过程中会产生大量废渣[主要含
的过程中会产生大量废渣[主要含 和
和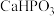 ,还含有少量
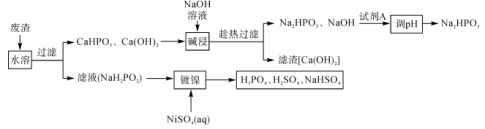
,还含有少量 ],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
已知:①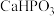 和
和 的
的 分别为
分别为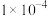 和
和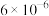 ;
;
② 为一元弱酸,
为一元弱酸, 为二元弱酸;
为二元弱酸;
③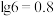 。
。
下列叙述错误的是
 )广泛应用于化学镀镍,在生产
)广泛应用于化学镀镍,在生产 的过程中会产生大量废渣[主要含
的过程中会产生大量废渣[主要含 和
和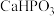 ,还含有少量
,还含有少量 ],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
已知:①
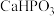 和
和 的
的 分别为
分别为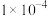 和
和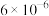 ;
;②
 为一元弱酸,
为一元弱酸, 为二元弱酸;
为二元弱酸;③
 。
。下列叙述错误的是
A.“趁热过滤”的目的是防止滤渣中的 溶解 溶解 |
B.“趁热过滤”后,要使滤液中 的浓度不小于0.01 mol⋅L 的浓度不小于0.01 mol⋅L ,则滤液的pH应不低于11.6 ,则滤液的pH应不低于11.6 |
C.试剂A可以是 , , 是正盐 是正盐 |
D.“镀镍”时,发生反应的离子方程式为 |
您最近一年使用:0次
名校
10 . 下列实验过程可以达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究H+浓度对 、 、 相互转化的影响 相互转化的影响 | 向K2CrO4溶液中加入足量稀硫酸,观察溶液颜色变化 |
| B | 比较HNO2与CH3COOH电离出H+的能力强弱 | 同温下,分别测定CH3COONa溶液和NaNO2溶液的pH |
| C | 证明AgCl的溶解度大于Ag2S | 向1mL 0.5mol/L的AgNO3溶液中滴加几滴NaCl溶液,产生白色沉淀,再滴加几滴Na2S溶液产生黑色沉淀 |
| D | 探究水的电离过程是吸热的 | 分别用pH计测定常温和沸水的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-05更新
|
165次组卷
|
2卷引用:湖南省郴州市2023-2024学年高二上学期期末教学质量监测化学试题



