名校
1 . 利用某钒废渣(主要成分为 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如图。
的工艺流程如图。 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;
Ⅱ. (有机层)
(有机层)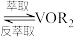 (有机层)
(有机层) ;
;
Ⅲ.溶液中 与
与 可相互转化:
可相互转化: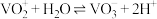 。
。
下列说法错误的是
 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如图。
的工艺流程如图。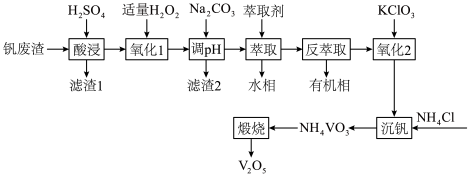
 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;Ⅱ.
 (有机层)
(有机层)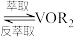 (有机层)
(有机层) ;
;Ⅲ.溶液中
 与
与 可相互转化:
可相互转化: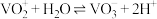 。
。下列说法错误的是
| A.“氧化1”中,不适宜用升温的方式加快转化速率 |
B.“滤渣2”的成分为 |
| C.有机萃取剂可循环使用 |
D.“沉钒”时还需通 调节溶液的酸碱性 调节溶液的酸碱性 |
您最近一年使用:0次
今日更新
|
407次组卷
|
4卷引用:2024届湖南省湖南大学附属中学高三下学期二模 化学试题
2024届湖南省湖南大学附属中学高三下学期二模 化学试题 (已下线)江苏省姜堰中学、如东中学、前黄中学三校2023-2024学年高三下学期联考化学试题福建省福州市八县市一中2024届高三下学期模拟联考化学试题江苏省部分学校2024届高三下学期高考模拟化学试题
名校
2 . 牙釉质的主要成分是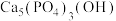 ,牙齿表面液膜的pH一般约为6.5,当液膜pH<5.2时,牙釉质会出现溶解损伤。下列说法正确的是
,牙齿表面液膜的pH一般约为6.5,当液膜pH<5.2时,牙釉质会出现溶解损伤。下列说法正确的是
已知: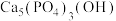 、
、 的
的 分别为
分别为 、
、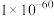 ;
;
含磷粒子在水溶液中的物质的量分数(δ)与pH的关系如图。
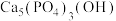 ,牙齿表面液膜的pH一般约为6.5,当液膜pH<5.2时,牙釉质会出现溶解损伤。下列说法正确的是
,牙齿表面液膜的pH一般约为6.5,当液膜pH<5.2时,牙釉质会出现溶解损伤。下列说法正确的是已知:
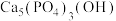 、
、 的
的 分别为
分别为 、
、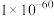 ;
;含磷粒子在水溶液中的物质的量分数(δ)与pH的关系如图。
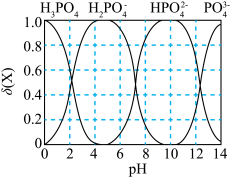
A.使用含氟牙膏时, 可转化为 可转化为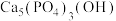 |
B.牙齿表面液膜中: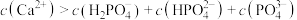 |
C. 的电离程度小于其水解程度 的电离程度小于其水解程度 |
D.当糖附着在牙齿上发酵时,会产生 ,所以多吃糖可以防治龋齿 ,所以多吃糖可以防治龋齿 |
您最近一年使用:0次
名校
解题方法
3 . 工业上采用酸性高浓度含砷废水主要以亚砷酸(H3AsO3)形式存在,提取As2O3的工艺流程如下:
Ⅰ.As2S3与过量的 存在以下反应:
存在以下反应: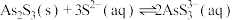 ;
;
Ⅱ.亚砷酸盐的溶解性大于相应砷酸盐。
回答下列问题:
(1)沉砷中FeSO4的作用是___________ :
(2)H2O2的作用是___________ ;滤渣I中含有FeAsO4、 、
、 和
和___________ (填化学式)。
(3)加生石灰和过氧化氢过程中,也可将砷元素转化为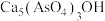 沉淀,发生的主要反应有:
沉淀,发生的主要反应有:
A.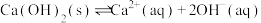

B.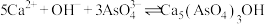

资料表明:“沉砷”的最佳温度是85℃,温度高于85℃,随温度升高沉淀率下降,从平衡移动角度分析其原因是___________ 。
(4)调节pH=0时,由Na3AsO4制备As2O3的离子方程式为___________ 。
(5)常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化曲线如图所示:___________ 。
(6)已知 的
的 ,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以
,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以 形式存在)中Fe3+的浓度为
形式存在)中Fe3+的浓度为 ,则低浓度含砷废水中
,则低浓度含砷废水中 的浓度为
的浓度为___________ mg⋅L-1,___________ (填“符合”或“不符合”)排放标准。

Ⅰ.As2S3与过量的
 存在以下反应:
存在以下反应: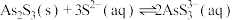 ;
;Ⅱ.亚砷酸盐的溶解性大于相应砷酸盐。
回答下列问题:
(1)沉砷中FeSO4的作用是
(2)H2O2的作用是
 、
、 和
和(3)加生石灰和过氧化氢过程中,也可将砷元素转化为
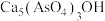 沉淀,发生的主要反应有:
沉淀,发生的主要反应有:A.
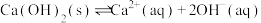

B.
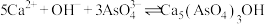

资料表明:“沉砷”的最佳温度是85℃,温度高于85℃,随温度升高沉淀率下降,从平衡移动角度分析其原因是
(4)调节pH=0时,由Na3AsO4制备As2O3的离子方程式为
(5)常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化曲线如图所示:

(6)已知
 的
的 ,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以
,含砷污染物允许排放标准为不大于0.5mg⋅L-1。若低浓度含砷废水(假设砷均以 形式存在)中Fe3+的浓度为
形式存在)中Fe3+的浓度为 ,则低浓度含砷废水中
,则低浓度含砷废水中 的浓度为
的浓度为
您最近一年使用:0次
名校
4 . 钒属于稀有金属,在天然矿物中含量很低。从硫酸厂废弃的钒触媒(主要成分为 、
、 、
、 、
、 )中回收
)中回收 的流程如图所示。
的流程如图所示。
(1)V元素在元素周期表中的位置为___________ 。
(2)“活化焙烧”的目的是使 转化为
转化为 。已知反应过程中
。已知反应过程中 能被
能被 氧化生成
氧化生成 ,
, 自身分解也可以生成
自身分解也可以生成 ,则该步骤所得尾气中硫元素的主要存在形式有
,则该步骤所得尾气中硫元素的主要存在形式有___________ (填化学式)。
(3)常温下稀 溶液的pH
溶液的pH___________ 7(填“>”“<”或“=”,已知 的
的 ,
, ,
, 的
的 )。“浸出”步骤中有
)。“浸出”步骤中有 生成,写出该步骤中
生成,写出该步骤中 转化为
转化为 的离子方程式
的离子方程式___________ 。“活化焙烧”时可能有少量的 未完全转化,推测“浸出”步骤中加入少量
未完全转化,推测“浸出”步骤中加入少量 的主要作用是
的主要作用是___________ 。
(4)“浓缩”后,溶液中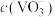 的浓度为0.2mo/L,“沉钒”步骤中钒元素的沉降率为98%,则沉钒后溶液中
的浓度为0.2mo/L,“沉钒”步骤中钒元素的沉降率为98%,则沉钒后溶液中
___________ mol/L[ ,假设沉钒过程中溶液体积不变]。
,假设沉钒过程中溶液体积不变]。
(5)含钒离子在储能领域应用广泛。如图所示的全钒液储能电池装置可实现化学能和电能相互转化,该装置储能时电势高的电极的电极反应式为___________ ,若储能时转移2mol电子,则正极液储罐中 的净变化为
的净变化为___________ mol。
 、
、 、
、 、
、 )中回收
)中回收 的流程如图所示。
的流程如图所示。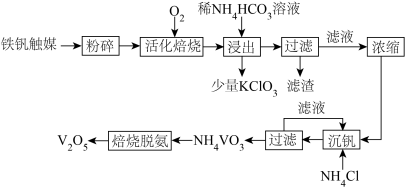
(1)V元素在元素周期表中的位置为
(2)“活化焙烧”的目的是使
 转化为
转化为 。已知反应过程中
。已知反应过程中 能被
能被 氧化生成
氧化生成 ,
, 自身分解也可以生成
自身分解也可以生成 ,则该步骤所得尾气中硫元素的主要存在形式有
,则该步骤所得尾气中硫元素的主要存在形式有(3)常温下稀
 溶液的pH
溶液的pH 的
的 ,
, ,
, 的
的 )。“浸出”步骤中有
)。“浸出”步骤中有 生成,写出该步骤中
生成,写出该步骤中 转化为
转化为 的离子方程式
的离子方程式 未完全转化,推测“浸出”步骤中加入少量
未完全转化,推测“浸出”步骤中加入少量 的主要作用是
的主要作用是(4)“浓缩”后,溶液中
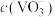 的浓度为0.2mo/L,“沉钒”步骤中钒元素的沉降率为98%,则沉钒后溶液中
的浓度为0.2mo/L,“沉钒”步骤中钒元素的沉降率为98%,则沉钒后溶液中
 ,假设沉钒过程中溶液体积不变]。
,假设沉钒过程中溶液体积不变]。(5)含钒离子在储能领域应用广泛。如图所示的全钒液储能电池装置可实现化学能和电能相互转化,该装置储能时电势高的电极的电极反应式为
 的净变化为
的净变化为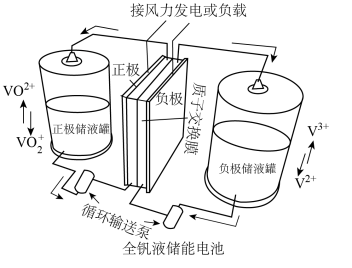
您最近一年使用:0次
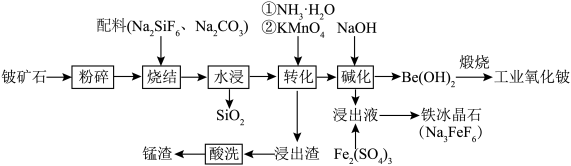
5 . 铍作为一种稀有元素,在航空航天、电子加工等领域具有重要意义。用铍矿石(含BeO及少量Ca、Mg、Mn元素)与配料生产工业氧化铍的工艺流程如下: 的还原产物为
的还原产物为 。回答下列问题:
。回答下列问题:
(1)若缺少粉碎步骤,产生的影响为_______ 。
(2)烧结时,若铍矿石中BeO恰好转化为 ,Si元素转化为
,Si元素转化为 ,则BeO发生反应的化学方程式为
,则BeO发生反应的化学方程式为_______ 。
(3)水浸后溶液中仍有未反应的 ,加入
,加入 后会转化为
后会转化为 沉淀,所得产物可除去溶液中的钙、镁元素,
沉淀,所得产物可除去溶液中的钙、镁元素, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)水浸后溶液中Mn元素以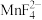 形式存在,加入稍过量
形式存在,加入稍过量 溶液煮沸50min至溶液
溶液煮沸50min至溶液______ 时说明反应结束。结合平衡移动原理解释酸洗时控制溶液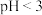 的原因:
的原因:______ 。
(5)碱化时,室温下加入NaOH,控制 ,析出颗粒状的
,析出颗粒状的 ,所得浸出液中
,所得浸出液中 ,此时溶液中
,此时溶液中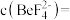
___  。已知
。已知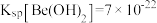 ,
,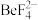 的解离常数
的解离常数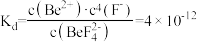
(6)碱化后浸出液中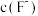 远高于排放标准,向其中加入硫酸铁生成
远高于排放标准,向其中加入硫酸铁生成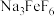 ,
, 为八面体结构,则Fe原子采取的杂化方式为
为八面体结构,则Fe原子采取的杂化方式为____ (填标号)。
A. B.
B. C.
C.
 的还原产物为
的还原产物为 。回答下列问题:
。回答下列问题:(1)若缺少粉碎步骤,产生的影响为
(2)烧结时,若铍矿石中BeO恰好转化为
 ,Si元素转化为
,Si元素转化为 ,则BeO发生反应的化学方程式为
,则BeO发生反应的化学方程式为(3)水浸后溶液中仍有未反应的
 ,加入
,加入 后会转化为
后会转化为 沉淀,所得产物可除去溶液中的钙、镁元素,
沉淀,所得产物可除去溶液中的钙、镁元素, 发生反应的离子方程式为
发生反应的离子方程式为(4)水浸后溶液中Mn元素以
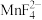 形式存在,加入稍过量
形式存在,加入稍过量 溶液煮沸50min至溶液
溶液煮沸50min至溶液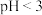 的原因:
的原因:(5)碱化时,室温下加入NaOH,控制
 ,析出颗粒状的
,析出颗粒状的 ,所得浸出液中
,所得浸出液中 ,此时溶液中
,此时溶液中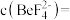
 。已知
。已知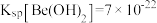 ,
,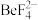 的解离常数
的解离常数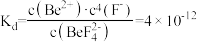
(6)碱化后浸出液中
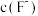 远高于排放标准,向其中加入硫酸铁生成
远高于排放标准,向其中加入硫酸铁生成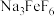 ,
, 为八面体结构,则Fe原子采取的杂化方式为
为八面体结构,则Fe原子采取的杂化方式为A.
 B.
B. C.
C.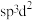
您最近一年使用:0次
名校
6 . 下列实验设计不能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A |  在水溶液中存在平衡 在水溶液中存在平衡 | 向1mL  的 的 溶液中加入1mL浓KI溶液,振荡试管,观察颜色变化 溶液中加入1mL浓KI溶液,振荡试管,观察颜色变化 |
| B | 比较AgCl和AgI的 | 向2mL 0.1 的NaCl溶液中滴加两滴等浓度的 的NaCl溶液中滴加两滴等浓度的 溶液,再滴加4滴等浓度KI溶液,观察现象 溶液,再滴加4滴等浓度KI溶液,观察现象 |
| C | 检验某卤代烃中的是否含有氯元素 | 取卤代烃少许与NaOH乙醇溶液共热后,加入稀硝酸酸化,再加入 溶液,观察是否有白色沉淀生成 溶液,观察是否有白色沉淀生成 |
| D | 比较配位键 和 和 的稳定性 的稳定性 | 向 溶液中加入少量NaCl固体,振荡,观察溶液颜色变化 溶液中加入少量NaCl固体,振荡,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 常温下,用NaOH溶液分别滴定等物质的量浓度的HX(弱酸)、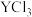 (可溶性盐)和
(可溶性盐)和 (可溶性盐)三种溶液。
(可溶性盐)三种溶液。 [M表示
[M表示 、
、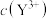 、
、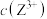 ]随溶液pH的变化如图所示。已知:
]随溶液pH的变化如图所示。已知: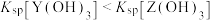 。下列说法错误的是
。下列说法错误的是
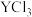 (可溶性盐)和
(可溶性盐)和 (可溶性盐)三种溶液。
(可溶性盐)三种溶液。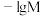 [M表示
[M表示 、
、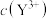 、
、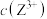 ]随溶液pH的变化如图所示。已知:
]随溶液pH的变化如图所示。已知: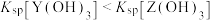 。下列说法错误的是
。下列说法错误的是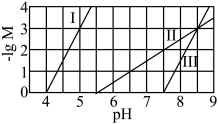
A.曲线I代表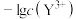 随溶液pH的变化关系 随溶液pH的变化关系 |
B. 的数量级是 的数量级是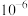 |
C. 固体能完全溶解在 固体能完全溶解在 溶液中 溶液中 |
D.滴定HX溶液至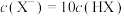 时,溶液中: 时,溶液中: |
您最近一年使用:0次
名校
8 . 以菱镁矿(主要成分为 ,还含有
,还含有 、
、 和
和 等杂质)为原料制取高纯
等杂质)为原料制取高纯 的流程如图所示。下列说法错误的是
的流程如图所示。下列说法错误的是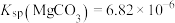 ,
,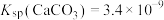
下列说法错误的是
 ,还含有
,还含有 、
、 和
和 等杂质)为原料制取高纯
等杂质)为原料制取高纯 的流程如图所示。下列说法错误的是
的流程如图所示。下列说法错误的是
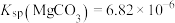 ,
,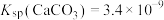
下列说法错误的是
| A.为提高“酸浸”速率,可采取矿石粉碎、搅拌等措施 |
B.“浸渣”为 ,“滤渣”为 ,“滤渣”为 、 、 |
C.“浓缩、部分脱水”时,可能有 沉淀生成 沉淀生成 |
| D.该流程涉及复分解反应、化合反应、分解反应和置换反应 |
您最近一年使用:0次
9 . 下列实验中的颜色变化与氧化还原反应有关的是
A. 通入品红溶液中,溶液由红色变为无色 通入品红溶液中,溶液由红色变为无色 |
| B.苯酚长时间放置在空气中,晶体由无色变为粉红色 |
| C.KI溶液滴入AgCl浊液中,沉淀由白色变为黄色 |
D.稀硫酸滴入 溶液中,溶液由黄色变为橙色 溶液中,溶液由黄色变为橙色 |
您最近一年使用:0次
10 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下 中含有的 中含有的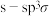 键数为 键数为 |
B. 葡萄糖 葡萄糖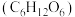 含羟基 含羟基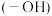 数目为 数目为 |
C.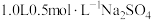 水溶液中含有的氧原子数为 水溶液中含有的氧原子数为 |
D.25℃时, ,则 ,则 饱和溶液中 饱和溶液中 数目为 数目为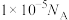 |
您最近一年使用:0次



