1 . 化学是一门实验的科学,滴定法是一种常用的化学定量分析的方法。室温下,用 溶液分别滴定体积均为20.00mL、浓度均为
溶液分别滴定体积均为20.00mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
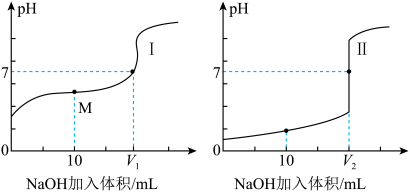
(1)滴定醋酸溶液的曲线是___________ 。(填“Ⅰ”或“Ⅱ”)。
(2)若采用氨水滴定醋酸,写出氨水与醋酸反应的离子反应方程式___________ 。
(3)滴定开始前,三种溶液中由水电离出的 最大的是
最大的是______ 。
A. 溶液 B.
溶液 B. 盐酸 C.
盐酸 C. 醋酸
醋酸
(4)该 溶液的pH为
溶液的pH为______ ;给该溶液加热,pH______ (填“变大”“变小”或“不变”)。
(5)在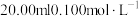 的盐酸中,滴加
的盐酸中,滴加 溶液后,此时溶液的pH=
溶液后,此时溶液的pH=___________ 。
(6)取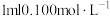 的盐酸稀释1000倍后,溶液pH=
的盐酸稀释1000倍后,溶液pH=___________ ,此时水电离出的 浓度为
浓度为___________ 。
(7)下列离子一定能大量共存的是___________。
(8)下列叙述正确的是___________。
(9)下列有关实验的说法,正确的是___________。
 溶液分别滴定体积均为20.00mL、浓度均为
溶液分别滴定体积均为20.00mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
(1)滴定醋酸溶液的曲线是
(2)若采用氨水滴定醋酸,写出氨水与醋酸反应的离子反应方程式
(3)滴定开始前,三种溶液中由水电离出的
 最大的是
最大的是A.
 溶液 B.
溶液 B. 盐酸 C.
盐酸 C. 醋酸
醋酸(4)该
 溶液的pH为
溶液的pH为(5)在
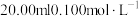 的盐酸中,滴加
的盐酸中,滴加 溶液后,此时溶液的pH=
溶液后,此时溶液的pH=(6)取
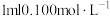 的盐酸稀释1000倍后,溶液pH=
的盐酸稀释1000倍后,溶液pH= 浓度为
浓度为(7)下列离子一定能大量共存的是___________。
A.甲基橙呈黄色的溶液中: 、 、 、 、 、 、 |
B.加入铝粉后产生大量氢气的溶液中: 、 、 、 、 、 、 |
C.石蕊呈蓝色的溶液中: 、 、 、 、 、 、 |
D.pH=1的溶液中: 、 、 、 、 、 、 |
(8)下列叙述正确的是___________。
A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下其 |
B.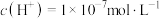 的溶液一定是中性溶液 的溶液一定是中性溶液 |
C.向水中加入少量固体 ,水的电离平衡逆向移动, ,水的电离平衡逆向移动, 减小 减小 |
D.将水加热, 增大,pH不变 增大,pH不变 |
(9)下列有关实验的说法,正确的是___________。
| A.测定HClO溶液pH时,用玻璃棒蘸取溶液,点在干燥pH试纸上 |
| B.等体积、等pH的硫酸与醋酸溶液分别与足量锌反应,醋酸产生的氢气多 |
| C.等体积、等浓度的盐酸和醋酸分别与相同大小的锌粒反应,醋酸初始反应速率快 |
| D.使用pH试纸测定溶液的pH时,若先润湿,则测得溶液的pH一定有误差 |
您最近一年使用:0次
2 . 常温下,向含有 、
、 、
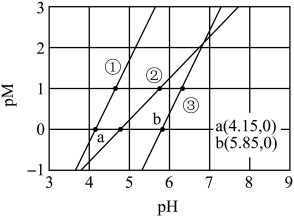
、 的工业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示
的工业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示 或
或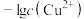 或
或 ]。
]。
已知: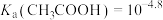 ,
,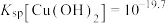 。若溶液中离子浓度小于
。若溶液中离子浓度小于 ,认为该离子沉淀完全。下列说法不正确的是
,认为该离子沉淀完全。下列说法不正确的是
 、
、 、
、 的工业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示
的工业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示 或
或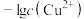 或
或 ]。
]。已知:
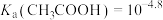 ,
,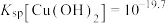 。若溶液中离子浓度小于
。若溶液中离子浓度小于 ,认为该离子沉淀完全。下列说法不正确的是
,认为该离子沉淀完全。下列说法不正确的是
A.曲线①表示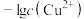 与pH的关系 与pH的关系 |
B. 时,溶液中 时,溶液中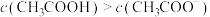 |
C. 时,可认为 时,可认为 沉淀完全 沉淀完全 |
D. 时, 时,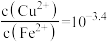 |
您最近一年使用:0次
2023-04-19更新
|
1580次组卷
|
5卷引用:广东省广州市2023届高三二模考试化学试题
广东省广州市2023届高三二模考试化学试题(已下线)押题密卷 03-【热题狂飙】2023年高考化学样卷(全国卷专用)辽宁省沈阳市第二中学2023届高三下学期第六次模拟考试化学试题广东省肇庆市德庆县香山中学2023-2024学年高三上学期9月月考化学试题四川省泸州市泸县第四中学2023-2024学年高二上学期12月月考化学试题
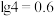
3 .  时,某实验小组利用虚拟感应器技术探究用
时,某实验小组利用虚拟感应器技术探究用 的碳酸钠溶液滴定
的碳酸钠溶液滴定 的
的 溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中
溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中 的逸出)如图所示。下列说法正确的是
的逸出)如图所示。下列说法正确的是
已知: 时,
时, 的
的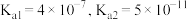 ;
; 。
。
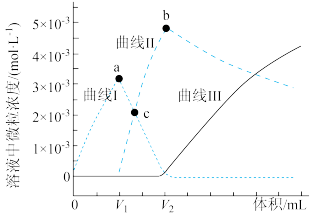
 时,某实验小组利用虚拟感应器技术探究用
时,某实验小组利用虚拟感应器技术探究用 的碳酸钠溶液滴定
的碳酸钠溶液滴定 的
的 溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中
溶液,得到反应过程中的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中 的逸出)如图所示。下列说法正确的是
的逸出)如图所示。下列说法正确的是已知:
 时,
时, 的
的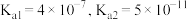 ;
; 。
。
A.碳酸钠的水解常数 |
B.曲线I为 浓度变化曲线, 浓度变化曲线, |
| C.a点和b点溶液中,水的电离程度较大的是a点 |
D.c点溶液 |
您最近一年使用:0次
2023-01-12更新
|
512次组卷
|
3卷引用:湖南省益阳市2022-2023学年高三上学期期末质量检测化学试题
解题方法
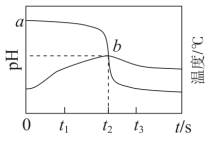
4 . 向 溶液中持续滴加稀盐酸,记录溶液
溶液中持续滴加稀盐酸,记录溶液 及温度随时间的变化如图所示。下列说法正确的是
及温度随时间的变化如图所示。下列说法正确的是
 溶液中持续滴加稀盐酸,记录溶液
溶液中持续滴加稀盐酸,记录溶液 及温度随时间的变化如图所示。下列说法正确的是
及温度随时间的变化如图所示。下列说法正确的是
A. 溶液的起始浓度为 溶液的起始浓度为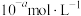 |
| B.在滴定至终点的过程中,水的电离程度不断减小 |
C. 对应的溶液中均存在: 对应的溶液中均存在: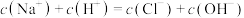 |
D.由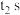 后溶液的温度变化可推知, 后溶液的温度变化可推知, 与 与 的反应是吸热反应 的反应是吸热反应 |
您最近一年使用:0次
2023-01-06更新
|
455次组卷
|
2卷引用:北京市东城区2022-2023学年高三上学期1月期末统一检测化学试卷
5 . 常温下,下列关于溶液的说法错误的是
A.某盐溶液pH<7,则此溶液中水电离的 浓度大于 浓度大于 |
B.pH均为3的 和HCl溶液的导电能力基本相同 和HCl溶液的导电能力基本相同 |
C.0.1mol/L的氨水pH约为11,则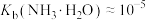 |
D.将 溶液稀释,pH减小 溶液稀释,pH减小 |
您最近一年使用:0次
6 . 常温下,向20mL1mol·L-1CuCl2溶液中滴加2mol·L-1Na2S溶液的滴定曲线如图所示。已知:pCu=-lgc(Cu2+),lg2.5=0.4,常温下Ksp(FeS)=6.3×10-18;Kal(H2S)=1.2×10-7,Ka2(H2S)=7.1×10-15。下列说法中正确的是
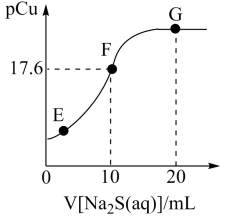

| A.常温下,S2-的水解常数Kh(S2-)约为8.3×10-8 |
| B.E→F→G的过程中,水的电离度一直在减小 |
| C.向1mol·L-1FeSO4(aq)中加入足量CuS固体,产生FeS沉淀 |
| D.25℃时,Cu2++H2S=CuS↓+2H+的K约为1.36×1014 |
您最近一年使用:0次
7 . 常温下,有以下五种溶液:
请回答以下问题:
(1)向等体积的①和②溶液中分别加入形状、大小一样的锌块(足量),反应一段时间后的速率v①_______ (填“>”、“<”或“=”)v②,若收集等体积的 ,则消耗时间更短的是
,则消耗时间更短的是_______ (填化学式),醋酸和锌反应的离子方程式为_______ 。
(2)若向⑤溶液中加入少量④,⑤的 将
将_______ (填“增大”、“减小”或“不变”,下同);若加入少量②,⑤的水解程度将_______ 。
(3)将等体积的①,②,③,④溶液分别加水稀释至原来的100倍,溶液的 由大到小的顺序是
由大到小的顺序是_______ (填编号)。
(4)分别向等体积的③和④溶液中加入②至恰好完全反应,消耗②更多的是_______ (填化学名称)。
(5)将等体积的①和②溶液混合后,加入 蒸馏水,溶液中
蒸馏水,溶液中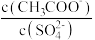 将
将_______ (填“增大”、“减小”或“不变”)。
(6)①,②,③,④,⑤五种溶液中由水电离出的 浓度由大到小的顺序是
浓度由大到小的顺序是_______ (填编号)。
| 编号 | ① | ② | ③ | ④ | ⑤ |
| 溶液 | 醋酸 | 硫酸 | 氨水 | 氢氧化钠 | 氯化铵 |
 | 3 | 3 | 11 | 11 | 3 |
(1)向等体积的①和②溶液中分别加入形状、大小一样的锌块(足量),反应一段时间后的速率v①
 ,则消耗时间更短的是
,则消耗时间更短的是(2)若向⑤溶液中加入少量④,⑤的
 将
将(3)将等体积的①,②,③,④溶液分别加水稀释至原来的100倍,溶液的
 由大到小的顺序是
由大到小的顺序是(4)分别向等体积的③和④溶液中加入②至恰好完全反应,消耗②更多的是
(5)将等体积的①和②溶液混合后,加入
 蒸馏水,溶液中
蒸馏水,溶液中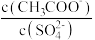 将
将(6)①,②,③,④,⑤五种溶液中由水电离出的
 浓度由大到小的顺序是
浓度由大到小的顺序是
您最近一年使用:0次
2022-01-15更新
|
164次组卷
|
2卷引用:河北省定州市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
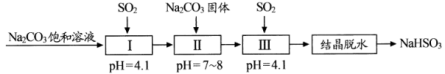
8 . 利用烟道气中的 生产
生产 晶体的工艺流程如下所示。下列说法错误的是
晶体的工艺流程如下所示。下列说法错误的是
 生产
生产 晶体的工艺流程如下所示。下列说法错误的是
晶体的工艺流程如下所示。下列说法错误的是
A. 时,步骤Ⅰ中溶液为 时,步骤Ⅰ中溶液为 溶液 溶液 |
B.步骤Ⅲ所得溶液中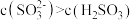 |
C.向 饱和溶液中通入 饱和溶液中通入 的过程,水的电离程度先增大后减小 的过程,水的电离程度先增大后减小 |
D.步骤Ⅱ中发生的反应之一为: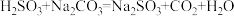 ,则 ,则 的 的 大于 大于 的 的 |
您最近一年使用:0次
名校
9 . 图中表示两种等体积的碱性溶液在稀释过程中pH的变化,下列相关说法正确的是
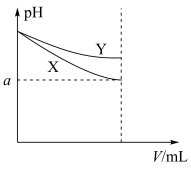

| A.两溶液稀释相同倍数,水电离的OH-浓度可能X>Y,也可能是X<Y |
| B.若图中曲线分别表示CH3COONa溶液和NaClO溶液,则X为CH3COONa溶液[已知Ka(CH3COOH)> Ka(HClO)] |
| C.加水稀释到任何程度,图中a一定大于7 |
| D.若图中曲线分别表示NaOH溶液和氨水,则起始时NaOH溶液浓度更大 |
您最近一年使用:0次
2021-11-15更新
|
884次组卷
|
6卷引用:浙江省A9协作体2021-2022学年高二上学期期中联考化学试题
浙江省A9协作体2021-2022学年高二上学期期中联考化学试题(已下线)期末综合测试卷01-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)浙江省桐庐中学2021-2022学年高二12月阶段性测试化学试题浙江省衢温“5+1”联盟2021-2022学年高一下学期期中考试化学(创新班)试题浙江省杭州市浙江大学附属中学2021-2022学年高二上学期期末考试化学试题安徽省池州市江南中学2021-2022学年高二上学期12月月考化学试题
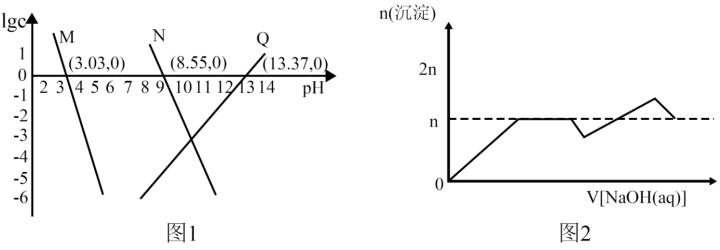
10 . 已知:①离子浓度为10-5mol/L时可认为沉淀完全;② 。向
。向 和AlCl3混合溶液中加入NaOH溶液,Mg和Al两种元素在水溶液中的存在形式与pH的关系如图所示,纵轴lg=lgc(Mn+)或lgc([Al(OH)4]-)。
和AlCl3混合溶液中加入NaOH溶液,Mg和Al两种元素在水溶液中的存在形式与pH的关系如图所示,纵轴lg=lgc(Mn+)或lgc([Al(OH)4]-)。
下列说法正确的是:
 。向
。向 和AlCl3混合溶液中加入NaOH溶液,Mg和Al两种元素在水溶液中的存在形式与pH的关系如图所示,纵轴lg=lgc(Mn+)或lgc([Al(OH)4]-)。
和AlCl3混合溶液中加入NaOH溶液,Mg和Al两种元素在水溶液中的存在形式与pH的关系如图所示,纵轴lg=lgc(Mn+)或lgc([Al(OH)4]-)。
下列说法正确的是:
| A.图1中M代表Mg2+ |
B. |
| C.[Al(OH)4]-完全沉淀时,溶液pH=6.37 |
| D.该实验中,沉淀的物质的量随NaOH溶液体积变化图象如图2 |
您最近一年使用:0次
2021-10-13更新
|
2307次组卷
|
2卷引用:湖北省武昌实验中学2022届高三十月阶段性测试化学试题



