1 . 常温下,用 盐酸分别逐滴加入到
盐酸分别逐滴加入到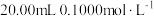 的三种一元碱溶液中,溶液的
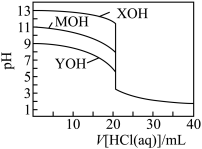
的三种一元碱溶液中,溶液的 随加入盐酸体积的变化如图所示。下列叙述错误的是
随加入盐酸体积的变化如图所示。下列叙述错误的是
 盐酸分别逐滴加入到
盐酸分别逐滴加入到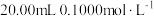 的三种一元碱溶液中,溶液的
的三种一元碱溶液中,溶液的 随加入盐酸体积的变化如图所示。下列叙述错误的是
随加入盐酸体积的变化如图所示。下列叙述错误的是
A.一元碱电离常数大小关系为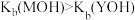 |
B.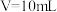 时, 时,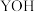 溶液中 溶液中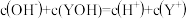 |
C.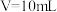 时,三种溶液中阳离子总浓度大小顺序为 时,三种溶液中阳离子总浓度大小顺序为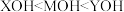 |
D. 时,三种溶液中水的电离程度最大的是 时,三种溶液中水的电离程度最大的是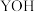 |
您最近一年使用:0次
2022-02-03更新
|
267次组卷
|
2卷引用:山东省青岛市黄岛区2021-2022学年高二上学期期末考试化学试题
解题方法
2 . 人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系(H2CO3/HCO ),该体系的主要作用是维持血液中pH保持稳定。在人体正常体温时,H2CO3
),该体系的主要作用是维持血液中pH保持稳定。在人体正常体温时,H2CO3 HCO
HCO +H+的Ka=10−6.1,正常人的血液中c(HCO
+H+的Ka=10−6.1,正常人的血液中c(HCO ):c(H2CO3)≈20:1,则下列判断正确的是(已知lg2=0.3)
):c(H2CO3)≈20:1,则下列判断正确的是(已知lg2=0.3)
 ),该体系的主要作用是维持血液中pH保持稳定。在人体正常体温时,H2CO3
),该体系的主要作用是维持血液中pH保持稳定。在人体正常体温时,H2CO3 HCO
HCO +H+的Ka=10−6.1,正常人的血液中c(HCO
+H+的Ka=10−6.1,正常人的血液中c(HCO ):c(H2CO3)≈20:1,则下列判断正确的是(已知lg2=0.3)
):c(H2CO3)≈20:1,则下列判断正确的是(已知lg2=0.3)| A.正常人血液内Kw=10-14 |
B.当过量的碱进入血液中时,只发生反应HCO +OH-=CO +OH-=CO +H2O +H2O |
C.正常人血液中存在:c(HCO )+c(OH-)+2c(CO )+c(OH-)+2c(CO )=c(H+)+c(H2CO3) )=c(H+)+c(H2CO3) |
| D.由题给数据可算得正常人血液的pH约为7.4 |
您最近一年使用:0次
2022-01-26更新
|
194次组卷
|
2卷引用:浙江省绍兴柯桥区2021-2022学年高二上学期期末教学质量调测化学试题
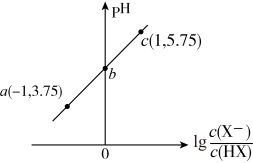
3 . 室温下,向20.00mL0.10mol·L-1HX溶液中滴加0.10mol·L-1NaOH溶液,溶液pH随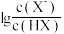 变化关系如图所示。下列说法正确的是
变化关系如图所示。下列说法正确的是
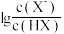 变化关系如图所示。下列说法正确的是
变化关系如图所示。下列说法正确的是
| A.室温下,HX的电离平衡常数Ka的数量级为10-5 |
| B.b点时,加入NaOH溶液的体积为10mL |
| C.c点溶液中:c(Na+)=10c(HX) |
| D.溶液中水的电离程度:c>b>a |
您最近一年使用:0次
名校
解题方法
4 . 常温下,向20 mL某浓度的硫酸溶液中滴入0.1 mol·L-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图。下列分析正确的是
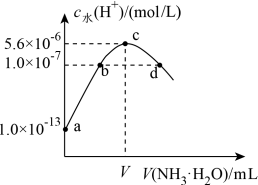

| A.V=40 |
| B.c点所示溶液中:c(H+)-c(OH-)=2c(NH3·H2O) |
| C.NH3·H2O的电离常数K=10-4 |
D.d点所示溶液中:c(NH )=2c(SO )=2c(SO ) ) |
您最近一年使用:0次
2022-01-21更新
|
539次组卷
|
16卷引用:2015-2016学年福建省厦门市海沧中学高二下学期期末化学试卷
2015-2016学年福建省厦门市海沧中学高二下学期期末化学试卷2016-2017学年辽宁省沈阳铁路中学高二上第一次月考化学试卷江西省景德镇市第一中学2016-2017学年高二(素质班)下学期期末考试化学试题【全国百强校】山西省长治市第二中学2018-2019学年高二上学期第二次月考(期中)化学试题江西省南昌市南昌县莲塘第三中学2020-2021学年高二上学期第二次月考化学试题新疆乌鲁木齐市第七十中学2022-2023学年高二上学期期中考试化学试题2016届山东省临沂市高三下学期教学质检一模化学试卷百所名校联考-水溶液中的离子平衡夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解中三大守恒的应用2020届高三化学选修4二轮专题练——混合溶液中微粒浓度大小的比较专题【精编23题】(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)第6讲 离子平衡坐标图像-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练
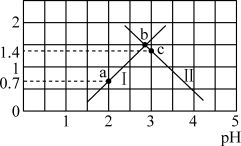
5 . 草酸 是二元弱酸,常温下,用NaOH溶液滴定草酸溶液,溶液中
是二元弱酸,常温下,用NaOH溶液滴定草酸溶液,溶液中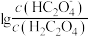 或
或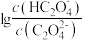 与混合溶液pH关系如图所示。下列说法错误的是
与混合溶液pH关系如图所示。下列说法错误的是
 是二元弱酸,常温下,用NaOH溶液滴定草酸溶液,溶液中
是二元弱酸,常温下,用NaOH溶液滴定草酸溶液,溶液中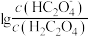 或
或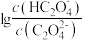 与混合溶液pH关系如图所示。下列说法错误的是
与混合溶液pH关系如图所示。下列说法错误的是
A.曲线Ⅰ为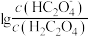 随溶液pH的变化曲线 随溶液pH的变化曲线 |
B.b点时,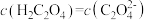 |
C.常温下,草酸的电离常数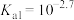 , ,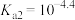 |
| D.a、b、c三点,水的电离程度先增大后减小 |
您最近一年使用:0次
2022-01-21更新
|
460次组卷
|
3卷引用:山东省日照市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
6 . 常温下,将NaOH溶液滴加到某二元弱酸 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
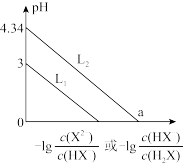
 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列说法正确的是
A.NaHX溶液中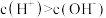 |
B.当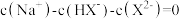 时, 时, |
C.水的电离程度: 上的点大于 上的点大于 上的点 上的点 |
D.a点溶液中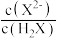 的数量级为 的数量级为 |
您最近一年使用:0次
2022-01-17更新
|
455次组卷
|
5卷引用:山东省济南市2021-2022上学期高二上学期期末考试化学试题
名校
解题方法
7 . 常温下,往20mL0.1mol·L-1NH4HSO4溶液中逐滴加入0.1mol·L-1的NaOH溶液,溶液中由水电离的c水(H+)与所加NaOH溶液体积的关系如图所示(假设:混合后溶液体积的变化忽略不计,整个过程无氨气的逸出)。下列分析正确的是
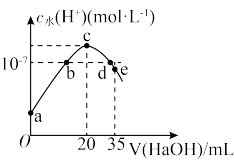
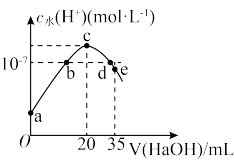
A.a~c之间,主要反应为NH +OH—=NH3·H2O +OH—=NH3·H2O |
| B.b点、d点对应溶液的pH均为7 |
C.d~e之间,溶液中c(Na+)+c(SO )=0.05mol/L )=0.05mol/L |
D.pH=7时,溶液中c(Na+)>c(SO )>c(NH )>c(NH )>c(OH—)=c(H+) )>c(OH—)=c(H+) |
您最近一年使用:0次
2022-01-16更新
|
467次组卷
|
3卷引用:重庆市缙云教育联盟2021-2022学年高二下学期4月质量检测化学试题
8 . 常温下,有以下五种溶液:
请回答以下问题:
(1)向等体积的①和②溶液中分别加入形状、大小一样的锌块(足量),反应一段时间后的速率v①_______ (填“>”、“<”或“=”)v②,若收集等体积的 ,则消耗时间更短的是
,则消耗时间更短的是_______ (填化学式),醋酸和锌反应的离子方程式为_______ 。
(2)若向⑤溶液中加入少量④,⑤的 将
将_______ (填“增大”、“减小”或“不变”,下同);若加入少量②,⑤的水解程度将_______ 。
(3)将等体积的①,②,③,④溶液分别加水稀释至原来的100倍,溶液的 由大到小的顺序是
由大到小的顺序是_______ (填编号)。
(4)分别向等体积的③和④溶液中加入②至恰好完全反应,消耗②更多的是_______ (填化学名称)。
(5)将等体积的①和②溶液混合后,加入 蒸馏水,溶液中
蒸馏水,溶液中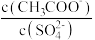 将
将_______ (填“增大”、“减小”或“不变”)。
(6)①,②,③,④,⑤五种溶液中由水电离出的 浓度由大到小的顺序是
浓度由大到小的顺序是_______ (填编号)。
| 编号 | ① | ② | ③ | ④ | ⑤ |
| 溶液 | 醋酸 | 硫酸 | 氨水 | 氢氧化钠 | 氯化铵 |
 | 3 | 3 | 11 | 11 | 3 |
(1)向等体积的①和②溶液中分别加入形状、大小一样的锌块(足量),反应一段时间后的速率v①
 ,则消耗时间更短的是
,则消耗时间更短的是(2)若向⑤溶液中加入少量④,⑤的
 将
将(3)将等体积的①,②,③,④溶液分别加水稀释至原来的100倍,溶液的
 由大到小的顺序是
由大到小的顺序是(4)分别向等体积的③和④溶液中加入②至恰好完全反应,消耗②更多的是
(5)将等体积的①和②溶液混合后,加入
 蒸馏水,溶液中
蒸馏水,溶液中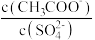 将
将(6)①,②,③,④,⑤五种溶液中由水电离出的
 浓度由大到小的顺序是
浓度由大到小的顺序是
您最近一年使用:0次
2022-01-15更新
|
164次组卷
|
2卷引用:河北省定州市2021-2022学年高二上学期期末考试化学试题
9 . 下列说法正确的是
| A.电解、电离、电镀、电化学腐蚀这些过程都需要通电后才能进行 |
B.298K时,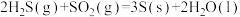 能自发进行,则其△H<0 能自发进行,则其△H<0 |
| C.镀锌铁板是利用了外加电流的阴极保护法来达到防止腐蚀的目的 |
| D.将纯水加热至较高温度,Kw变大、pH变小、呈酸性 |
您最近一年使用:0次
名校
解题方法
10 . 25 ℃时,将0.10 mol·L-1 CH3COOH溶液滴加到10 mL 0.10 mol·L-1 NaOH溶液中,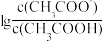 与pH的关系如图所示,C点坐标是(6,1.7)。下列说法
与pH的关系如图所示,C点坐标是(6,1.7)。下列说法不正确 的是
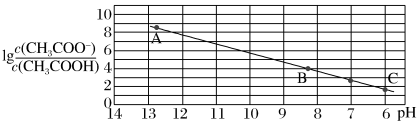
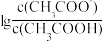 与pH的关系如图所示,C点坐标是(6,1.7)。下列说法
与pH的关系如图所示,C点坐标是(6,1.7)。下列说法
A.pH=11时, 的数量级为106 的数量级为106 |
| B.溶液中,水的电离程度:C >A |
| C.B点存在c(Na+)-c(CH3COO-)=(10-5.8-10-8.2)mol·L-1 |
| D.CH3COONa的水解常数Kh=10-9.7 |
您最近一年使用:0次
2022-01-14更新
|
922次组卷
|
2卷引用:山东省青岛第一中学2023-2024学年高二上学期第二次月考化学试卷



