解题方法
1 . 室温时,用0.200mol•L-1盐酸滴定 20.00mL 0.200 mol•L-1的 NaY 溶液,溶液中水的电离程度随所加盐酸的体积变化如图所示(忽略滴定过程中溶液体积变化),则下列有关说法正确的是[已知 Ka(HY)=5.0×10-11]
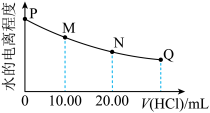

| A.可选取酚酞作为滴定指示剂 | B.M 点溶液的 pH>7 |
| C.Q 点水的电离程度最小,Kw<l0-14 | D.M点,c(Na+)=c (HY)+c (Y-)+c (Cl-) |
您最近一年使用:0次
解题方法
2 . 下列说法正确的是
| A.升高温度可以使纯水中的 c ( H+) >c(OH-) |
| B.常温下 pH=3的盐酸和 pH=ll 的氨水等体积混合:c(C1-)+c( H+) =c(NH4+ )+c( OH-) |
| C.可用 MgO 固体除去 MgCl2 溶液中的 FeCl3杂质 |
| D.常温下,l ×10-8mol• L-1 的极稀盐酸的 pH 等于8 |
您最近一年使用:0次
解题方法
3 . 下列关于水的叙述错误的是
| A.做溶剂溶解其他物质时会参与水合的化学反应 |
| B.温度一定时,离子积为常数,和溶液的酸碱性无关 |
| C.当溶液呈酸性时,可能会抑制水的电离平衡 |
| D.当溶液呈碱性时,水电离出的OH-浓度就减小 |
您最近一年使用:0次
名校
4 . 常温下,向 浓度均为
浓度均为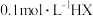 和
和 的混合溶液中滴加
的混合溶液中滴加 的
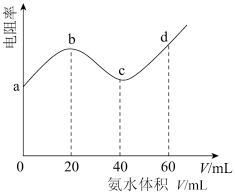
的 ,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积
,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积 的关系如图所示(忽略混合时体积变化),下列说法正确的是
的关系如图所示(忽略混合时体积变化),下列说法正确的是
 浓度均为
浓度均为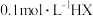 和
和 的混合溶液中滴加
的混合溶液中滴加 的
的 ,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积
,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积 的关系如图所示(忽略混合时体积变化),下列说法正确的是
的关系如图所示(忽略混合时体积变化),下列说法正确的是
A.常温下,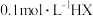 的 的 比同浓度 比同浓度 的 的 大 大 |
B.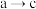 过程中水的电离程度先减小后增大 过程中水的电离程度先减小后增大 |
C. 点溶液中, 点溶液中,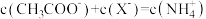 |
D. 点时, 点时,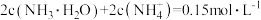 |
您最近一年使用:0次
2020-05-09更新
|
374次组卷
|
3卷引用:安徽省宣城市2020届高三二模理综化学试题
名校
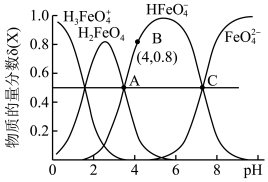
5 . 高铁酸钾(K2FeO4)是一种优良的水处理剂。25℃,其水溶液中加酸或碱改变溶液的pH时,含铁粒子的物质的量分数δ(X)随pH的变化如图所示[已知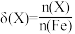 ]。下列说法正确的是( )
]。下列说法正确的是( )
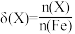 ]。下列说法正确的是( )
]。下列说法正确的是( )
| A.K2FeO4、H2FeO4都属于强电解质 |
| B.由B点数据可知,H2FeO4的第一步电离常数Ka1=4.0×10-4 |
C.25℃,H2FeO4(aq)+H+ H3FeO4+(aq)的平衡常数K>100 H3FeO4+(aq)的平衡常数K>100 |
| D.A、C两点对应溶液中水的电离程度不相等 |
您最近一年使用:0次
2020-05-07更新
|
477次组卷
|
6卷引用:山东省淄博市2020届高三第一次模拟化学试题
山东省淄博市2020届高三第一次模拟化学试题山东省济南外国语学校2021届高三10月月考化学试题安徽师范大学附属中学2020-2021学年高二上学期期中考查化学试题(已下线)2021年高考化学押题预测卷(河北卷)(03)(含考试版、答题卡、参考答案、全解全析)河北省石家庄市第二中学2021届高三3月学情考试化学试题山东省济南外国语学校2021-2022学年高三上学期11月月考化学试题
6 . 将25℃时浓度均为0.1mol/L的HA溶液和BOH溶液按体积分别为Va和Vb混合,保持Va+Vb=100mL,且生成的BA可溶于水。已知Va、Vb与混合液pH关系如图所示。下列说法错误的是( )
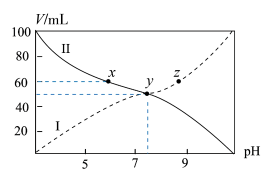

| A.曲线II表示HA溶液的体积 |
| B.x点存在c(A-)+c(OH-)=c(B+)+c(H+) |
| C.电离平衡常数:K(HA)>K(BOH) |
| D.x、y、z三点对应的溶液中,y点溶液中水的电离程度最大 |
您最近一年使用:0次
7 . 25℃时,改变某醋酸溶液的pH,溶液中c(CH3COO-)与c(CH3COOH)之和始终为0.1mol·L-1,溶液中H+、OH-、CH3COO-及CH3COOH浓度的常用对数值(lgc)与pH的关系如图所示。下列说法错误的是( )
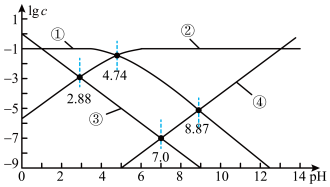

| A.图中③表示lgc(H+)与pH的关系曲线 |
| B.0.1mol·L-1CH3COOH溶液的pH约为2.88 |
| C.lgK(CH3COOH)=4.74 |
| D.向0.10mol·L-1醋酸钠溶液中加入0.1mol醋酸钠固体,水的电离程度变大 |
您最近一年使用:0次
8 . 草酸(H2C2O4)是一种二元弱酸。常温下,向H2C2O4溶液中逐滴加入NaOH溶液,混合溶液中lgX[X为 或
或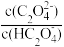 ]与pH的变化关系如图所示。下列说法一定正确的是
]与pH的变化关系如图所示。下列说法一定正确的是

 或
或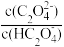 ]与pH的变化关系如图所示。下列说法一定正确的是
]与pH的变化关系如图所示。下列说法一定正确的是
A.Ⅰ表示lg 与pH的变化关系 与pH的变化关系 |
| B.pH=1.22的溶液中:2c(C2O42-)+c(HC2O4-)=c(Na+) |
| C.根据图中数据计算可知,Ka2(H2C2O4)的数量级为10-4 |
| D.pH 由1.22到4.19的过程中,水的电离程度先增大后减小 |
您最近一年使用:0次
名校
9 . 常温下,分别调节浓度均为0.1 mol·L-1 HA溶液、HB的溶液的pH,所得溶液中酸分子的百分含量ω%(如HA的百分含量为 ×100%)与pH的变化关系如图所示。已知调节pH时不影响溶液总体积。下列说法
×100%)与pH的变化关系如图所示。已知调节pH时不影响溶液总体积。下列说法不正确 的是
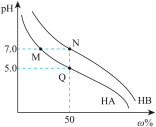
 ×100%)与pH的变化关系如图所示。已知调节pH时不影响溶液总体积。下列说法
×100%)与pH的变化关系如图所示。已知调节pH时不影响溶液总体积。下列说法
| A.常温下,Ka(HA)=1.0×10-5 | B.M、N两点对应离子浓度:c(A-)=c(B-) |
| C.将M、N两点溶液等体积混合,溶液呈中性 | D.水的电离程度:M=N>Q |
您最近一年使用:0次
2020-04-27更新
|
293次组卷
|
3卷引用:(山东新高考)2020年高考考前45天大冲刺卷 化学一
解题方法
10 . NaCl是我们生活中必不可少的物质。将NaCl溶于水配成1mol·L-1的溶液,溶解过程如图所示,下列说法正确的是


| A.b的离子为Cl- |
| B.溶液中含有NA个Na+ |
| C.水合b离子的图示不科学 |
| D.40℃时该溶液的pH小于7,是由于Na+水解所致 |
您最近一年使用:0次



