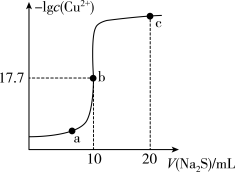
1 . 某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,已知:lg2=0.3,Ksp(ZnS)=3×10-25mol2/L2,下列有关说法正确的是( )

| A.a、b、c三点中,水的电离程度最大的为b点 |
| B.如不考虑CuS的溶解,则c点溶液有:2[c(S2-)+c(HS-)+c(H2S)]═c(Cl-) |
| C.该温度下Ksp(CuS)=2×10-18mol2/L2 |
D.该温度下,反应: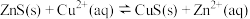 的平衡常数为 的平衡常数为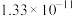 |
您最近一年使用:0次
名校
解题方法
2 . 室温下,向25.00 mL 0.1000 mol∙L−1氨水中滴加0.1000 mol∙L−1盐酸,溶液的pH随盐酸体积的变化如图。下列说法不正确的是( )
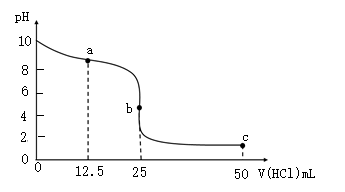

| A.如选甲基橙为指示剂,终点的判断为溶液颜色由黄色恰好变为橙色且半分钟不变色 |
| B.a→b,水的电离程度逐渐增大 |
C.a点溶液中, c(H+) c(H+) |
D.c点溶液中,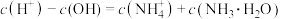 |
您最近一年使用:0次
2020-06-18更新
|
311次组卷
|
2卷引用:浙江省温州市2020届高三适应性测试(三模)化学试题
解题方法
3 . 室温下,向10mL 0.1mol/LHX溶液中逐滴加入0.2mol⋅L−1YOH溶液,混合溶液的pH变化情况如图所示(温度和体积变化忽略不计)。则下列结论正确的是
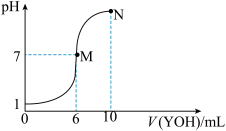
| A.M点不存在:c(Y+)=c(X-) |
| B.N点水的电离程度大于M点水的电离程度 |
C.25℃时pH=4的YX溶液中电离出的c(H+)=1.0×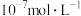 |
D.N点对应溶液中粒子浓度关系存在: |
您最近一年使用:0次
解题方法
4 . 已知草酸(H2C2O4)为二元弱酸,25℃时,Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5。用NaOH溶液滴定草酸氢钾(KHC2O4)溶液,混合溶液的相对导电能力随加入NaOH体积的变化如图所示(忽略混合时溶液温度的变化),其中N点为反应终点。下列有关描述中正确的是
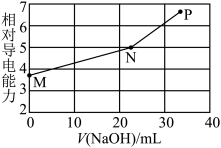

A.M点粒子浓度:c(K+)>c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
B.N点时存在:c(Na+)+c(K+)<2c( )+2c( )+2c( ) ) |
C.从N点到P点的过程中溶液中一定存在:c(Na+)+c(H2C2O4)>c( ) ) |
| D.水的电离程度大小顺序:P>N>M |
您最近一年使用:0次
5 . 常温下,用 NaOH溶液滴定NH4HSO4溶液 ,混合溶液的相对导电能力变化曲线如图所示,已知: Kb(NH3• H2O) =10-5,下列叙述正确的是


A.X→Y 过程中发生反应的离子方程式为: +OH-= NH3• H2O +OH-= NH3• H2O |
B.Y点满足:c( ) +c(Na+) =2c( ) +c(Na+) =2c( ) ) |
| C.水的电离程度:X>Y>Z |
| D.若Z点溶液pH=1l,则此时溶液中氨水浓度约为0.1 mol•L-1 |
您最近一年使用:0次
名校
解题方法
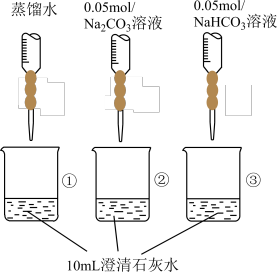
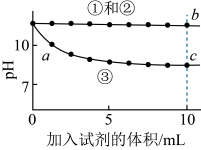
6 . 实验小组利用传感器探究Na2CO3和NaHCO3的性质。
下列分析不正确 的是
| 实验操作 | 实验数据 |
| 测量下述实验过程的pH变化
|
|
下列分析
| A.①与②的实验数据基本相同,说明②中的OH-未参与该反应 |
| B.加入试剂体积相同时,②所得沉淀质量大于③所得沉淀质量 |
| C.从起始到a点过程中反应的离子方程式为:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
| D.b点对应溶液中水的电离程度小于c点对应溶液中水的电离程度 |
您最近一年使用:0次
2020-06-13更新
|
387次组卷
|
3卷引用:北京市东城区2020届高三第二次模拟考试化学试题
7 . 常温下,向10mL0.1mol/L的HR溶液中逐滴加入0.1mol/L的氨水,所得溶液pH及导电能力变化如图。下列分析正确的是( )
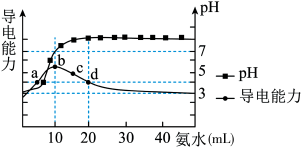

| A.溶液中的阳离子浓度总和最大的是d点 |
| B.常温下,HR的电离平衡常数数量级为10-8 |
| C.b点和d点溶液中,水的电离程度不相等 |
| D.d点的溶液中,微粒浓度关系:c(R-)+2c(HR)=c(NH3∙H2O) |
您最近一年使用:0次
名校
解题方法
8 . 物质的量浓度相等的三种溶液:①H2CO3 ②NaOH ③Na2CO3溶液,下列说法不正确的是
| A.水电离出的c(H+):③>①>② |
| B.溶液的pH:②>③>① |
C.①和②等体积混合后的溶液: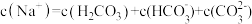 |
D.①和③等体积混合后的溶液: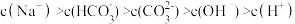 |
您最近一年使用:0次
名校
解题方法
9 . 某些难溶性铅盐可用作涂料,如秦俑彩绘中使用的铅白(PbCO3)和黄金雨中黄色的PbI2。室温下,PbCO3和 PbI2在不同的溶液中分别达到溶解平衡时-lgc(Pb2+)与-lgc(CO32-)或-lgc(I-)的关系如图所示。下列说法错误的是


| A.Ksp(PbCO3)的数量级为 10-14 |
| B.相同条件下,水的电离程度 p 点大于 q 点 |
| C.L1对应的是-lgc(Pb2+)与-lgc(I-)的关系变化 |
| D.p 点溶液中加入 Na2CO3浓溶液,可得白色沉淀 |
您最近一年使用:0次
2020-05-22更新
|
997次组卷
|
9卷引用:广东省茂名市2020届高三二模化学试题
广东省茂名市2020届高三二模化学试题(已下线)学科网2020年高三11月大联考考后强化卷(新课标Ⅲ卷)(已下线)专题10 水溶液中的离子平衡-2020年高考真题和模拟题化学分项汇编广东省汕头市金山中学2019-2020学年高二6月月考化学试题广东省广州市广大附中、广外2020-2021学年高二上学期期中考试化学试题河南省鹤壁高中2020-2021学年高二下学期第一次段考化学试题(已下线)2021年秋季高三化学开学摸底考试卷02(山东专用)甘肃省天水市第一中学2021-2022学年高二下学期开学检测化学试题四川省内江市第三中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
10 . 常温下,向20mL 0.05mol·L-1的某稀酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是


| A.NaHB溶液可能为酸性,也可能为碱性 |
| B.A、B、 C三点溶液的pH是逐渐减小,D、E、F三点溶液的pH是逐渐增大 |
| C.B点溶液c(NH4+)=2c(B2-) |
| D.E溶液中离子浓度大小关系:c(NH4+)> c(B2-)> c(H+)>c(OH-) |
您最近一年使用:0次
2020-05-20更新
|
516次组卷
|
3卷引用:黑龙江哈尔滨第三中学2020届高三下学期第二次模拟考试理科综合化学试题