名校
解题方法
1 . 常温下,向20.00mL0.1mol·L-1氨水中滴入0.1mol·L-1盐酸,溶液中由水电离出的c(H+)的负对数[-1gc水(H+)]与所加盐酸体积的关系如图所示,下列说法正确的是( )

| A.常温下,Kb(NH3·H2O)约为1×10-3 |
| B.b=20.00 |
| C.R、Q两点对应溶液均呈中性 |
| D.R到N、N到Q所加盐酸体积相等 |
您最近一年使用:0次
2020-01-04更新
|
578次组卷
|
4卷引用:2019年湖南省永州市高三上学期第一次模拟考试化学试卷
名校
2 . 下列说法正确的是( )
| A.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
| B.恒温时,向水中加入少量固体硫酸氢钠,水的电离程度增大 |
| C.2CO(g)+2NO(g)=N2(g)+2CO2(g)在298K时能自发进行,则它的ΔH<0 |
| D.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐 酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
您最近一年使用:0次
2020-01-04更新
|
298次组卷
|
3卷引用:2019年湖南省永州市高三上学期第一次模拟考试化学试卷
3 . 实验测得 0.5ml・L-1CH3COONa 溶液和 H2O 的 pH 随温度变化的曲线如图所示。下用说法正确的是


| A.随温度升高,CH3COONa 溶液的 c(OH-)增大 |
| B.随温度升高,H2O 的 pH 逐渐减小,是因为水中 c(H+)>c(OH-) |
| C.随温度升高,CH3COONa 溶液的 pH 变化是 Kw改变不大和水解平衡移动共同作用的结果 |
| D.随温度升高, CH3COONa 溶液的 pH 降低是因为 CH3COO-水解平衡向逆反应方向移动的结果 |
您最近一年使用:0次
名校
4 . 能促进水的电离平衡,并使溶液中的c(H+)>c(OH﹣)的操作是( )
| A.将水加热煮沸 | B.将明矾溶于水 |
| C.将NaHSO4固体溶于水 | D.将NaHCO3固体溶于水 |
您最近一年使用:0次
2019-12-30更新
|
209次组卷
|
6卷引用:2019届上海奉贤区高考第一次模拟化学试题
2019届上海奉贤区高考第一次模拟化学试题2020届上海市奉贤区高考化学一模试卷(已下线)考点11 弱电解质的电离及溶液pH-2020年高考化学命题预测与模拟试题分类精编(已下线)课时40 水的电离与溶液的酸碱性-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第08练 水的电离和溶液的pH-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)广西南宁市第三中学2020-2021学年高二下学期期末考试化学试题
14-15高二上·江西赣州·期末
名校
解题方法
5 . 25 ℃时,水的电离达到平衡:H2O H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是
 H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是| A.将纯水加热到95 ℃时,Kw变大,pH不变,水仍呈中性 |
| B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 |
| C.向纯水中加入少量碳酸钠固体,影响水的电离平衡,c(H+)减小,Kw不变 |
| D.向纯水中加入醋酸钠固体或盐酸,均可抑制水的电离,Kw不变 |
您最近一年使用:0次
2019-12-25更新
|
183次组卷
|
16卷引用:2014高考名师推荐化学水的电离及影响因素
(已下线)2014高考名师推荐化学水的电离及影响因素(已下线)2014高考名师推荐化学水的电离及影响因素(已下线)2013-2014学年江西赣州市四所重点中学高二上学期期末联考化学试卷(已下线)2014届高考化学二轮专题复习 电解质溶液与电离平衡练习卷(已下线)2014高考化学二轮复习限时集训 专题8电解质溶液练习卷A(已下线)2013-2014学年内蒙古包头三十三中高二下学期期中考试理科化学试卷(已下线)2014高考名师推荐化学水的电离与溶液酸碱性(已下线)2014届内蒙古包钢一中高二下学期期中Ⅰ考试化学试卷2015-2016学年山西省怀仁一中高二上期中考试化学试卷天津市耀华中学2018届高三上学期第一次月考化学试题河北省唐山市第一中学2018-2019学年高二上学期10月月考化学试题陕西省咸阳百灵中学2019-2020学年高二上学期第二次月考化学(理)试题黑龙江省哈尔滨市第三十二中学2020-2021学年高二上学期期末考试化学试题吉林省乾安县第七中学2021-2022学年高二上学期第三次质量检测化学试题江西省乐平中学2022-2023学年高二上学期11月期中考试化学试题湖南省衡阳市衡阳县第二中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
6 . 下列图示与对应的叙述相符的是
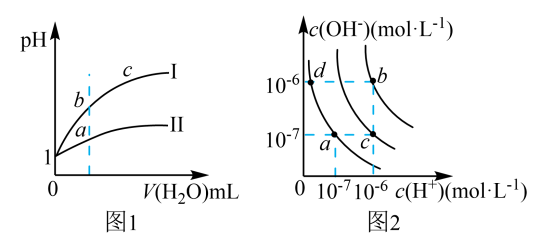

| A.图1表示相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图1中,中和等体积的两种酸,消耗等浓度的NaOH溶液体积V(Ⅰ)>V(Ⅱ) |
| C.图2中纯水仅升高温度,就可以从a点变到c点 |
| D.图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性 |
您最近一年使用:0次
2019-11-26更新
|
430次组卷
|
3卷引用:广东省广州市第八十九中学2019-2020学年高二上学期期中考试化学试题
名校
7 . 常温下,有关0.1mol/LCH3COONa溶液(pH>7),下列说法不正确的是( )
| A.根据以上信息,可推断CH3COOH为弱电解质 |
| B.加水稀释过程中,c(H+)⋅c(OH−) 的值增大 |
| C.加入NaOH固体可抑制 CHCOO−的水解 |
| D.同pH的CH3COONa溶液和NaOH溶液,由水电离出的c(H+)前者大 |
您最近一年使用:0次
2019-10-24更新
|
253次组卷
|
2卷引用:上海市奉贤中学2016年高三模拟考试(三模)化学试题
名校
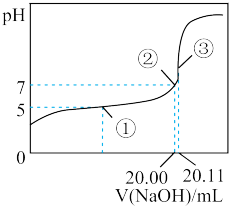
8 . 常温下,用0.1000 NaOH溶液滴定20.00mL某未知浓度的CH3COOH溶液,滴定曲线如右图所示。已知在点③处恰好中和。下列说法
NaOH溶液滴定20.00mL某未知浓度的CH3COOH溶液,滴定曲线如右图所示。已知在点③处恰好中和。下列说法不正确 的是( )
 NaOH溶液滴定20.00mL某未知浓度的CH3COOH溶液,滴定曲线如右图所示。已知在点③处恰好中和。下列说法
NaOH溶液滴定20.00mL某未知浓度的CH3COOH溶液,滴定曲线如右图所示。已知在点③处恰好中和。下列说法
| A.点①②③三处溶液中水的电离程度依次增大 |
B.该温度时CH3COOH的电离平衡常数约为 |
| C.点①③处溶液中均有c(H+)=c(CH3COOH)+c(OH-) |
| D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
您最近一年使用:0次
2019-09-02更新
|
615次组卷
|
5卷引用:山东省实验中学2020届高三线上诊断测试化学试题
山东省实验中学2020届高三线上诊断测试化学试题浙江省名校新高考研究联盟(Z20联盟)2020届高三第一次联考化学试题吉林省长春市榆树市第一高级中学2020届高三上学期期末考试化学试题山东省六地市部分学校2020届高三下学期3月2日线上考试化学试题(已下线)考点12 盐类水解及其应用-2020年高考化学命题预测与模拟试题分类精编
9 . 研究NO2、NO、SO2 、CO等大气污染气体的处理具有重要意义。利用反应6NO2(g)+8NH3(g)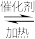 7N2(g)+12H2O(g)可处理NO2。
7N2(g)+12H2O(g)可处理NO2。
(1)在2L的密闭容器中,2分钟内,上述反应混合物的物质的量增加了0.25mol,则2分钟内v(NH3)=______ 。
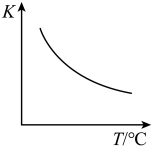
(2)该反应的化学平衡常数表达式K=______ ;已知该反应平衡常数(K)与温度(T)的关系如图所示,若升高温度,则v正反应______ v逆反应(填“大于”、“小于”或“等于”);反应达到平衡后若缩小反应容器体积,其它条件不变,则混合气体的平均式量将______ (填“变大”、“变小”或“不变”)。
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组同学收集某地的雨水进行实验,每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
(3)请写出上述pH变化的原因______ 。
(4)有物质的量浓度相等的三种铵盐溶液:①NH4Cl ②NH4HCO3 ③NH4HSO4,这三种溶液中水的电离程度由大到小的顺序是______ (填编号)。
(5)向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀,用电离平衡原理解释上述现象。______ 。
 7N2(g)+12H2O(g)可处理NO2。
7N2(g)+12H2O(g)可处理NO2。(1)在2L的密闭容器中,2分钟内,上述反应混合物的物质的量增加了0.25mol,则2分钟内v(NH3)=
(2)该反应的化学平衡常数表达式K=
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组同学收集某地的雨水进行实验,每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
(3)请写出上述pH变化的原因
(4)有物质的量浓度相等的三种铵盐溶液:①NH4Cl ②NH4HCO3 ③NH4HSO4,这三种溶液中水的电离程度由大到小的顺序是
(5)向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀,用电离平衡原理解释上述现象。
您最近一年使用:0次
2019-08-19更新
|
314次组卷
|
2卷引用:上海市青浦区2019届高三高三第二次学业质量调研(二模)化学试题
名校
10 . 25℃时,将浓度均为0.1 mol·L-1、体积分别为Va和Vb的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是


| A.Ka(HX)的值与Kb(NH3·H2O)的值相等 |
| B.b点,c(NH4+)+c(HX)=0.05 mol·L-1 |
C.a→c点过程中, 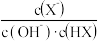 值不变 值不变 |
| D.a、b、c三点,c点时水电离出的c(H+)最大 |
您最近一年使用:0次



