解题方法
1 . 室温下,在20 mL新制氯水中滴加pH=13的NaOH溶液,溶液中水电离的c(H)与 NaOH溶液体积的关系如图所示。已知:K(HClO)=3×108,H2CO3:Ka1=4.3×107,Ka2=5.6×1011。下列说法正确的是


| A.m一定等于20 |
| B.b、d点对应的溶液显中性 |
| C.c点溶液中c(Na)=2c(ClO)+2c(HClO) |
| D.向c点溶液中通入少量CO2:2ClO+H2O+CO2=2HClO+CO32 |
您最近一年使用:0次
解题方法
2 . 298 K时,向20 mL 0.1 mol/L某酸HA溶液中逐滴加入0.1 mol/L NaOH溶液,混合溶液的pH变化曲线如图所示。下列说法错误的是
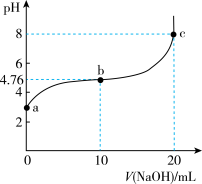

| A.a点溶液的pH为2.88 |
| B.b点溶液中:c(Na+)>c(A-)>c(HA) |
| C.b、c之间一定存在c(Na+)=c(A-)的点 |
| D.a、b、c三点中,c点水的电离程度最大 |
您最近一年使用:0次
名校
3 . 室温下,向100mL饱和的H2S溶液中通入SO2气体(气体体积换算成标准状况),发生反应:2H2S+SO2=3S↓+2H2O,测得溶液pH与通入SO2的关系如图所示。下列有关说法正确的是


| A.整个过程中,水的电离程度逐渐增大 |
| B.该温度下H2S的Ka1数量级为10-7 |
| C.曲线y代表继续通入SO2气体后溶液pH的变化 |
D.a点之后,随SO2气体的通入, 的值始终减小 的值始终减小 |
您最近一年使用:0次
2020-04-20更新
|
474次组卷
|
4卷引用:湖北省襄阳市第五中学,夷陵中学2020届高三下学期联考理综化学试题
解题方法
4 . 往10mL0.1mol/L的Ba(OH)2溶液中滴加等浓度NaHSO4溶液,溶液的导电能力随滴入溶液体积变化的曲线如图。下列说法正确的是
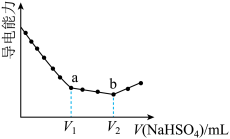

| A.a点对应的溶液呈碱性 |
| B.V2=10mL |
| C.水的电离程度:a> b |
| D.b点后的溶液满足c(Na+)>2c(SO42-) |
您最近一年使用:0次
2020-04-20更新
|
230次组卷
|
2卷引用:广东省东莞市2020届普通高中毕业班4月模拟自测(全国I卷)理综化学试题
名校
5 . 室温下,将 0.10 mol·L-1 盐酸滴入 20.00 mL 0.10 mol·L-1 氨水中,溶液中 pH 和 pOH 随加入盐酸体积变化曲线如图所示。已知:pOH=—lgc(OH−),下列正确的是


| A.M 点所示溶液中可能存在:c(Cl−)>c(NH4+) |
| B.M 点到Q点所示溶液中水的电离程度先变大后减小 |
| C.Q 点盐酸与氨水恰好中和 |
| D.N 点所示溶液中可能存在:c(NH4+)+c(NH3·H2O)=c(Cl−) |
您最近一年使用:0次
2020-04-18更新
|
181次组卷
|
11卷引用:【校级联考】安徽省皖中名校联盟2019届高三上学期10月联考化学试题
【校级联考】安徽省皖中名校联盟2019届高三上学期10月联考化学试题【全国百强校】新余四中、上高二中2019届高三第一次联考化学试题【全国百强校】山东省实验中学(中心校区)2019届高三11月模拟考试理科综合化学试题【全国百强校】四川省成都外国语学校2019届高三上学期期中考试理科综合化学试题四川省广安市邻水实验学校2018-2019学年高二上学期第三次月考化学试题【全国百强校】福建省厦门双十中学2018-2019学年高二下学期第二次月考化学试题湖南省娄底市娄星区2019-2020学年高二上学期期中考试化学试题四川省邻水市实验中学2019-2020学年高二12月月考化学试题甘肃省天水市第一中学2020届高三上学期第五次(期末)考试化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过素养 学科素养拓展训练浙江省天台县育才中学2021-2022学年高二上学期第一次月考试卷化学试题
名校
6 . 已知常温下HF酸性强于HCN,分别向1Ll mol/L的HF和HCN溶液中加NaOH固体调节pH(忽略温度和溶液体积变化),溶液中 (X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是
(X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是
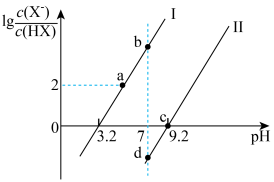
 (X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是
(X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是
A.直线I对应的是 |
| B.I中a点到b点的过程中水的电离程度逐渐增大 |
C.c点溶液中: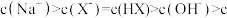  |
| D.b点溶液和d点溶液相比:cb(Na+)<cd(Na+) |
您最近一年使用:0次
2020-04-17更新
|
976次组卷
|
5卷引用:河南省六市2020届高三第一次联合调研监测(全国I卷)理综化学试题
解题方法
7 . 向等物质的量浓度的K2S、KOH混合溶液中滴加稀盐酸至过量。其中主要含硫各物种(H2S、HS−、S2−)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出)。下列说法不正确的是


| A.A曲线表示S2-随盐酸加入量增加时的分布分数改变情况 |
| B.X、Y为曲线两交叉点。若已知Y点处的pH,则可计算Ka1(H2S) |
| C.X、Y点对应溶液中水的电离程度大小关系为:X<Y |
| D.Y点对应溶液中c(K+)与含硫各微粒浓度的大小关系为:c(K+)=3[c(H2S)+c(HS−)+c(S2−)] |
您最近一年使用:0次
名校
8 . 下列有关说法正确的是
| A.MgO(s)+C(s)=CO(g)+Mg(g)高温下能自发进行,则该反应ΔH>0、ΔS>0 |
| B.常温下等物质的量浓度的CH3COOH溶液和HCl溶液中,水的电离程度相同 |
C.0.1 mol·L-1 NH4Cl溶液加水稀释,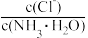 的值增大 的值增大 |
| D.对于反应2SO2+O2⇌2SO3,使用催化剂能加快反应速率并提高SO2的平衡转化率 |
您最近一年使用:0次
2020-04-14更新
|
280次组卷
|
2卷引用:江苏省苏锡常镇四市2020届高三教学情况调查(一) 化学试题
名校
9 . 已知某二元酸H2MO4在水中电离分以下两步:H2MO4⇌H++HMO4-,HMO4-⇌H++MO42-。常温下向20 mL0.1mol/L NaHMO4溶液中滴入cmol/LNaOH溶液,溶液温度与滴入NaOH溶液体积关系如图。下列说法正确的是
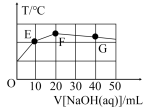

| A.该氢氧化钠溶液pH=12 |
| B.图像中F点对应的溶液中c(OH-)>c(HMO4-) |
| C.滴入NaOH溶液过程中水的电离程度一直增大 |
| D.图像中G点对应的溶液中c(Na+)=c(HMO4-)+2c(MO42-) |
您最近一年使用:0次
2020-04-10更新
|
469次组卷
|
3卷引用:河北省保定市2020届高三第一次模拟考试(全国I卷)理综化学试题
解题方法
10 . 对下列溶液的分析正确的是
| A.常温下pH=12的NaOH溶液,升高温度,其pH增大 |
B.向0.1mol/L NaHSO3溶液通入氨气至中性时 |
| C.0.01 mol/L醋酸溶液加水稀释时,原溶液中水的电离程度增大 |
D.在常温下,向二元弱酸的盐NaHA溶液中加入少量NaOH固体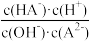 将增大 将增大 |
您最近一年使用:0次



