名校
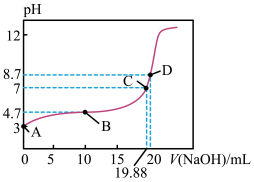
1 . 已知常温下,向20 mL 0.1000 mol/L  溶液中滴入0.1000 mol/L NaOH溶液,忽略温度变化,所得曲线如图所示。下列说法正确的是
溶液中滴入0.1000 mol/L NaOH溶液,忽略温度变化,所得曲线如图所示。下列说法正确的是
 溶液中滴入0.1000 mol/L NaOH溶液,忽略温度变化,所得曲线如图所示。下列说法正确的是
溶液中滴入0.1000 mol/L NaOH溶液,忽略温度变化,所得曲线如图所示。下列说法正确的是
| A.若A点pH=3.0,醋酸的电离度为10% |
B.若B点pH=4.7,该点电荷守恒式为 |
C.若C点加入NaOH溶液的体积为19.88 mL,离子浓度大小关系是 |
D.D点pH=8.7,溶液的物料守恒关系式是 |
您最近一年使用:0次
2023-02-16更新
|
242次组卷
|
4卷引用:江西省宜春市宜丰中学2023届高三模拟预测化学试题
2 . 根据水溶液中的离子平衡有关知识回答下列问题:
(1)纯水在100℃时, ,该温度下
,该温度下 的NaOH溶液中,由水电离出的
的NaOH溶液中,由水电离出的
_______  。
。
(2)常温下,将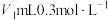 的稀盐酸与
的稀盐酸与 的NaOH溶液混合,所得溶液的pH为1,则
的NaOH溶液混合,所得溶液的pH为1,则
_______ (溶液体积变化忽略不计)。
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
①25℃时,等浓度的a:NaCN溶液、b: 溶液和c:
溶液和c: 溶液,三种溶液的pH由大到小的顺序为
溶液,三种溶液的pH由大到小的顺序为_______ 。(大小用a、b、c表示)
②向NaCN溶液中通入少量的 ,发生反应的化学方程式为
,发生反应的化学方程式为_______ 。
(4)常温下,用0.1000 mol∙L−1的NaOH溶液滴定20.00mL0.1000 mol∙L−1的 溶液,滴定过程中,溶液的pH与消耗NaOH溶液的体积的关系如图所示:
溶液,滴定过程中,溶液的pH与消耗NaOH溶液的体积的关系如图所示:

①该滴定过程应该选择_______ (填“酚酞”或“甲基橙”)作指示剂。
②a_______ 20mL(填“>”“<”或“=”)。
③C点溶液中离子浓度由大到小的顺序为_______ 。
(1)纯水在100℃时,
 ,该温度下
,该温度下 的NaOH溶液中,由水电离出的
的NaOH溶液中,由水电离出的
 。
。(2)常温下,将
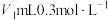 的稀盐酸与
的稀盐酸与 的NaOH溶液混合,所得溶液的pH为1,则
的NaOH溶液混合,所得溶液的pH为1,则
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN |  |
 |  |
 |   |
 溶液和c:
溶液和c: 溶液,三种溶液的pH由大到小的顺序为
溶液,三种溶液的pH由大到小的顺序为②向NaCN溶液中通入少量的
 ,发生反应的化学方程式为
,发生反应的化学方程式为(4)常温下,用0.1000 mol∙L−1的NaOH溶液滴定20.00mL0.1000 mol∙L−1的
 溶液,滴定过程中,溶液的pH与消耗NaOH溶液的体积的关系如图所示:
溶液,滴定过程中,溶液的pH与消耗NaOH溶液的体积的关系如图所示:
①该滴定过程应该选择
②a
③C点溶液中离子浓度由大到小的顺序为
您最近一年使用:0次
名校
解题方法
3 . 常温下,向 的NaA溶液中通入HF(g),溶液中
的NaA溶液中通入HF(g),溶液中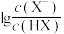 (X代表A或F)的值和pH的关系如图所示,已知酸性:
(X代表A或F)的值和pH的关系如图所示,已知酸性: ,忽略溶液体积的变化,下列叙述错误的是
,忽略溶液体积的变化,下列叙述错误的是
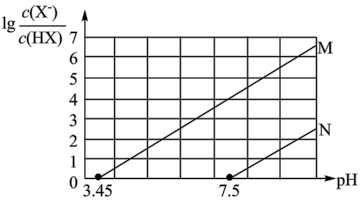
 的NaA溶液中通入HF(g),溶液中
的NaA溶液中通入HF(g),溶液中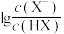 (X代表A或F)的值和pH的关系如图所示,已知酸性:
(X代表A或F)的值和pH的关系如图所示,已知酸性: ,忽略溶液体积的变化,下列叙述错误的是
,忽略溶液体积的变化,下列叙述错误的是
A.HA的电离常数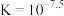 |
B.当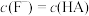 时,混合溶液 时,混合溶液 |
C.通入0.01molHF时,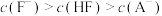 |
| D.随着HF的通入,溶液导电性先增大后减小 |
您最近一年使用:0次
2023-02-08更新
|
135次组卷
|
2卷引用:江西赣州市2022~2023学年高二上学期期末考试化学试题
名校
4 . 下列各选项均有两个数据,其中前者大于后者的是
A.盐酸中滴加氨水至中性时溶液中的c( )与c(Cl-) )与c(Cl-) |
B.盐酸中滴加氨水至恰好中和时溶液中的c( )与c(Cl-) )与c(Cl-) |
| C.25℃和60℃时纯水的pH |
| D.25℃和60℃时水的离子积Kw |
您最近一年使用:0次
2022-12-20更新
|
63次组卷
|
2卷引用:江西省丰城市第九中学2021-2022学年高二上学期第一次月考化学试题
名校
5 . 设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.将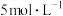 的 的 溶液滴加到沸水中,形成胶体粒子数小于 溶液滴加到沸水中,形成胶体粒子数小于 |
B. 与浓盐酸反应生成 与浓盐酸反应生成 时,转移电子数为 时,转移电子数为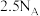 |
C.过量铁粉与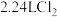 (标准状况)完全反应生成 (标准状况)完全反应生成 转移电子数为 转移电子数为 |
D.将 通入NaOH溶液中,二者恰好完全反应,则 通入NaOH溶液中,二者恰好完全反应,则 、 、 的数目之和为 的数目之和为 |
您最近一年使用:0次
6 . 常温下,向20mL0.1mol/L一元碱MOH溶液中滴加等浓度的一元酸HX溶液,滴定过程中溶液pH值的变化曲线如下图所示,已知4<m<6,下列说法正确的是


| A.该滴定过程中应选用酚酞作指示剂 | B.一元酸HX的Ka=5×10-6 |
| C.溶液中水的电离程度:b>a>c | D.c点溶液中: |
您最近一年使用:0次
7 . 25℃时,下列说法错误的是
| A.pH=2的醋酸和pH=2的盐酸溶液等体积混合后溶液pH不再为2 |
B.浓度均为  溶液和 溶液和 溶液等体积混合: 溶液等体积混合: |
C. 和 和 混合溶液: 混合溶液: |
D.pH=3的 和pH=11的 和pH=11的 溶液等体积混合后,溶液pH=7 溶液等体积混合后,溶液pH=7 |
您最近一年使用:0次
8 . 回答下列问题:
(1)Ⅰ.已知:在相同条件下醋酸与氨水电离程度相同,现有浓度均为 的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
①、②、③、④四种溶液中由水电离出的 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号) ___ ;
④、⑤、 、⑦、⑧五种溶液中
、⑦、⑧五种溶液中 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号) ___ 。
Ⅱ.已知 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(2)物质的量浓度均为 的四种溶液:
的四种溶液: 由小到大排列的顺序是
由小到大排列的顺序是___ (用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:___
(4)25℃时, 与
与 的混合溶液,若测得混合液
的混合溶液,若测得混合液 ,则溶液中
,则溶液中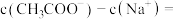
_____ (填准确数值)。
(5)25℃时,将 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用
氢氧化钠等体积混合,反应后溶液恰好显中性,用 、
、 表示醋酸的电离平衡常数为
表示醋酸的电离平衡常数为___
(6)标准状况下,将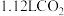 通入
通入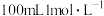 的
的 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式: 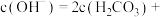
___________
(1)Ⅰ.已知:在相同条件下醋酸与氨水电离程度相同,现有浓度均为
 的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。①、②、③、④四种溶液中由水电离出的
 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号) ④、⑤、
 、⑦、⑧五种溶液中
、⑦、⑧五种溶液中 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号) Ⅱ.已知
 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 |  |  |  |
| 电离平衡常数 |  | 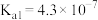  | 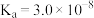 |
 的四种溶液:
的四种溶液: 由小到大排列的顺序是
由小到大排列的顺序是a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,
 与
与 的混合溶液,若测得混合液
的混合溶液,若测得混合液 ,则溶液中
,则溶液中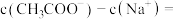
(5)25℃时,将
 的醋酸与
的醋酸与 氢氧化钠等体积混合,反应后溶液恰好显中性,用
氢氧化钠等体积混合,反应后溶液恰好显中性,用 、
、 表示醋酸的电离平衡常数为
表示醋酸的电离平衡常数为(6)标准状况下,将
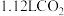 通入
通入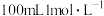 的
的 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式: 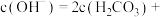
您最近一年使用:0次
9 . 已知NA为阿伏加德罗常数的值,下列说法正确的是
| A.一定条件下,1 mol H2与足量碘蒸汽充分反应,转移电子总数为2NA |
B.C4H8和C3H6的混合物的质量为a g,所含C—H键数目为 |
| C.常温下,56 g铁片与足量浓硫酸反应生成NA个SO2分子 |
D.常温常压下,将22.4 L NH3通入足量水中,溶液中N(NH3)+N(NH )+N(NH3·H2O) =NA )+N(NH3·H2O) =NA |
您最近一年使用:0次
2022-01-05更新
|
126次组卷
|
2卷引用:江西省宜春市上高二中2021-2022学年高三上学期第五次月考理综化学试题
解题方法
10 . 常温下,用0.100mol·L−1NaOH溶液分别滴定20.00mL0.100mol·L−1的HX和HY溶液,滴定曲线如图所示。下列说法正确的是
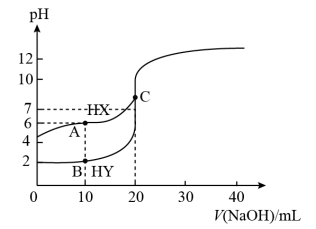

| A.Ka(HX)和Ka(HY)的数量级分别为10−8和10−4 |
| B.B点满足2c(H+)+c(HY)=2c(OH-)+c(Y-) |
| C.HX曲线上的A与C点混合,则存在c(X-)+c(HX)=2c(Na+) |
| D.A、B、C三点中由水电离出的c(H+)顺序为C>A>B |
您最近一年使用:0次
2021-12-31更新
|
333次组卷
|
5卷引用:江西稳派2022-2023学年高三上学期期中联考化学试题



